Йодное число, или так называемый коэффициент непредельности, характеризует степень ненасыщенности жира и выражается количеством йода в граммах, которое требуется для полного насыщения жирных кислот, содержащихся в 100 г жира (г I2/100 г жира). Это наиболее важная из констант жира. По величине этого показателя судят о преобладании в жирах насыщенных или ненасыщенных жирных кислот. Чем выше в жире содержание ненасыщенных жирных кислот, тем выше йодное число. Тугоплавкие жиры имеют низкое йодное число, легкоплавкие – высокое.
Йодное число дает возможность судить о склонности жира к различным изменениям (окислению, присоединению водорода и т. д.), происходящим при хранении и переработке пищевых жиров. Оно позволяет судить о чистоте и натуральности исследуемого жира. Кроме того, йодное число характеризует степень свежести жиров. При окислении жиров в процессе хранения йодное число снижается.
|
Йодное число |
г I2/100 г жира: |
|
подсолнечное масло |
– 119,0–145,0; |
|
кукурузное масло |
– 111,0–133,0; |
|
соевое масло |
– 120,0–140,0; |
|
китовый жир (покровное сало) |
– 107,4–161,5; |
|
рапсовое масло |
– 95,0–106,0; |
|
оливковое масло |
– 86,0–88,0; |
|
свиной жир |
– 46,0–66,0; |
|
молочный жир |
– 26,0–46,0; |
|
говяжий жир |
– 32,0–47,0; |
|
бараний жир |
– 31,0–46,0. |
Йодное число является показателем консистенции сливочного масла и должно учитываться при выборе температурных режимов обработки сливок в процессе их созревания и перемешивания. Этот показатель молочного жира зависит от кормовых рационов, стадии лактации, времени года, породы животного и т. д. Оно повышается летом и понижается зимой и лежит в пределах 28–45 г/100 г. Йодное число сливочного масла определяют при подозрении на наличие в нем примесей растительных масел.
Метод определения йодного числа основан на способности галогенов (йода, хлористого йода, бромистого йода) присоединяться по кратным связям. Непрореагировавший галоген оттитровывают тиосульфатом натрия в присутствии крахмала в качестве индикатора.
Кратные связи в полиненасыщенных жирных кислотах, входящих в состав жиров, насыщаются последовательно, причем время реакции присоединения возрастает по сравнению с мононенасыщенными. Насыщению галогенами в первую очередь подвержены кратные связи, наиболее удаленные от карбоксильной группы. Используя галогены, невозможно достичь полного насыщения сопряженных кратных связей. Величина йодного числа зависит:
§от числа этиленовых связей в ненасыщенных жирных кислотах (с увеличением количества этиленовых связей в углеродной цепи жирных кислот при одном и том же числе углеродных атомов йодное число увеличивается);
§от длины углеродной цепи в жирных кислотах (или от молекулярного веса);
§от положения этиленовых связей в углеродной цепи (с приближением этиленовой связи к карбоксильной группе жирных кислот их йодное число уменьшается);
§от наличия сопряженных связей (сопряженные этиленовые связи при использовании обычных методов определения йодного числа насыщаются не полностью).
Рекомендуемыми ГОСТ Р ИСО 3961–2010 «Жиры и масла животные и растительные. Определение йодного числа» являются следующие методы определения йодного числа: Гюбля (с хлорйодом), Кауфмана (с NaBr×Br2), Гануса (с бромйодом). Методы Гюбеля и Гануса дают одинаковые и близкие к теоретическим результаты. Названные методы рекомендуются для исследовательских целей, идентификации жиров и контроля производства. Метод Гануса неприемлем для анализа жиров с сопряженными кратными связями. Результаты определения йодных чисел по методу Кауфмана обычно на 1–3% выше, чем по методу Гюбля.
Метод Гюбля основан на присоединении по кратным связям хлористого йода (раствор Гюбля), который образуется при взаимодействии сулемы с йодом в спиртовых растворах:
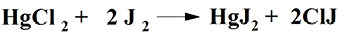
Хлористый йод практически полностью насыщает кратные связи жирнокислотных радикалов в жирах:

Избыток непрореагировавшего хлористого йода оттитровывают тиосульфатом натрия. Предварительно в реакционную среду необходимо внести йодид калия и воду для выделения эквивалентного количества йода из хлористого йода по следующей реакции:
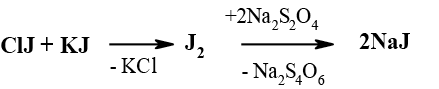
Ход анализа. В предварительно высушенную колбу для титрования вместимостью 500 мл с пришлифованной пробкой внести пробу анализируемого жира в зависимости от величины йодного числа. Пробу жира растворить в 15 мл хлороформа и добавить 25 мл (пипеткой) раствора Гюбля. Закрыть колбу пробкой, смоченной в растворе йодида калия, и оставить при температуре около 20 оС в темном месте на 18–24 часа. Время настаивания анализируемого раствора и величину навески анализируемого жира выбрать в зависимости от предполагаемой величины йодного числа (табл. 1.3.7).
Таблица 1.3.7. Рекомендуемая масса пробы и время настаивания
в зависимости от величины йодного числа
|
Значение йодного числа, г I2/100 г |
Масса пробы, г |
Время настаивания, ч |
|
от 5 до 20 включительно |
1,0 |
6 |
|
свыше 20 до 50 включительно |
0,6 |
8 |
|
свыше 50 до 100 включительно |
0,3 |
12 |
|
свыше 100 до 150 включительно |
0,2 |
18 |
|
свыше 150 до 200 включительно |
0,15 |
24 |
|
свыше 200 |
0,10 |
24 |
По истечении вышеуказанного времени до титрования в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды, смесь перемешать. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желто-соломенной окраски. В конце добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов в аналогичных условиях, но без добавления жира: 15 мл хлороформа, 25 мл раствора Гюбля. Колбу закрыть пробкой, смоченной в растворе йодида калия, и оставить в темном месте на 18–24 часа. Перед титрованием в колбу для анализа внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды и оттитровать.
Йодное число (ЙЧ, г I2/100 г или %) вычислить по формуле:
где VK – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование контрольного образца, мл;
VO – количество 0,1 н раствора тиосульфата натрия, израсходованного на титрование опытного образца, мл;
0, 01269 – титр 0,1 н раствора тиосульфата натрия, мг/мл;
m – масса исследуемого жира, г;
100 – коэффициент пересчета на 100 г анализируемого жира.
Метод Гануса основан на использовании бромистого йода, растворенного в безводной уксусной кислоте (реактив Гануса), который количественно присоединяется по кратным связям. Бромистый йод получают посредством смешения брома с йодом в безводной уксусной среде:
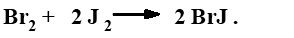
Бромистый йод присоединяется по кратным связям ненасыщенных жирных кислот.
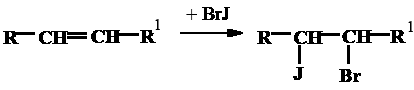
Избыток бромистого йода после введения йодида калия и воды оттитровывают тиосульфатом натрия.
Ход анализа. В колбу для титрования на 500 мл с пришлифованной пробкой внести пробу анализируемого жира в количестве 0,1–0,2 г и растворить в 15 мл хлороформа. Пипеткой внести 25 мл раствора Гануса, закрыть пробкой, смоченной в растворе йодида калия и оставить в темном месте на один час. Перед титрованием в колбу для титрования внести 20 мл 10%-го раствора йодида калия и 100 мл дистиллированной воды.
Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный. Контрольный опыт проделать в аналогичных условиях с тем же количеством реагентов, но без добавления жира.
Метод Кауфмана основан на применении в качестве реагента непрочного соединения NaBr×Br2, которое образуется при растворении в метиловом спирте соответствующих количеств брома и бромистого натрия:
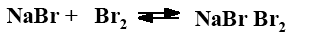
Бром из соединения NaBr×Br2 отщепляется и присоединяется к этиленовым связям жирных кислот, причем активность его недостаточна для замещения водорода:
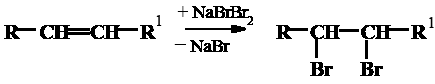
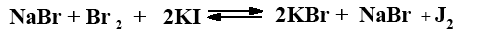
При прибавлении к раствору Кауфмана йодистого калия выделяется эквивалентное количество йода, который оттитровывают тиосульфатом натрия.
Ход анализа. Анализ аналогичен методу Гюбля. В колбу для титрования на 500 мл с пришлифованной пробкой внести пробу анализируемого жира в таких же количествах, как и в методе Гюбля и добавить 10 мл хлороформа. Пипеткой прилить 20 мл раствора Кауфмана, закрыть пробкой, смоченной в растворе йодида калия, оставить колбу с реакционной смесью в темном месте на 1–1,5 часа. Время зависит от предполагаемой величины йодного числа (на 1 час для масел с йодным числом до 100; на 1,5 часа – больше 100).
По истечении указанного времени в колбу прилить 10–15 мл 10%-го раствора йодистого калия и 50–60 мл дистиллированной воды. Избыток выделившегося йода оттитровать 0,1 н раствором тиосульфата натрия до появления желтой окраски. В конце титрования добавить несколько капель 1%-го раствора крахмала и продолжить титрование до перехода цвета анализируемого раствора из фиолетового в бесцветный.
Контрольный опыт проделать с тем же количеством реагентов, но без добавления жира.
Метод Маргошеса является ускоренным методом определения йодного числа. Хотя он и уступает по точности вышеописанным методам, но может использоваться для анализа жиров, содержащих жирные кислоты с сопряженными кратными связями. В качестве реагента используется раствор Маргошеса, содержащий йодноватистую кислоту.
В спиртовых растворах образование из йода йодноватистой кислоты происходит в ничтожных количествах, но ускоряется в присутствии ненасыщенных связей и особенно в избытке воды. Образующаяся йодноватистая кислота взаимодействует по этиленовым связям быстрее галоидов:
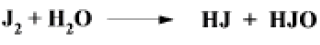

Избыток непрореагировавшего йода оттитровывают тиосульфатом натрия.
Ход анализа. В сухую колбу для титрования вместимостью 500 мл с пришлифованной пробкой взвесить на аналитических весах 0,1–0,15 г растительного масла или 0,2–0,25 г животного жира. Для растворения навески жира добавить 10 мл смеси этилового спирта и хлороформа (10:1). Если проба жира плохо растворяется, следует закрыть колбу воздушным холодильником и нагреть на водяной бане с температурой 50–60 оС в течение 15–20 минут. По истечении указанного срока колбу охладить до комнатной температуры и добавить пипеткой к анализируемой пробе 25 мл раствора Маргошеса (0,2 н спиртовой раствор йода). Оставить полученный раствор в темном месте. Спустя ровно 5 минут влить 200 мл дистиллированной воды, закрыть колбу пробкой и хорошо перемешать. Полученную смесь через 5 минут оттитровать 0,1 н раствором тиосульфата натрия до перехода коричневой окраски в желтую. Затем добавить индикатор – 1%-ный раствор крахмала – и продолжить титрование до исчезновения фиолетовой окраски (опыт).
Контрольный опыт проделать с теми же реактивами. К 10 мл смеси этилового спирта и хлороформа (10:1) добавить 25 мл 0,2 н раствора Маргошеса и оставить полученный раствор в темном месте. Спустя ровно 5 минут влить 200 мл дистиллированной воды и тщательно перемешать. Полученную эмульсию оттитровать 0,1 н раствором тиосульфата натрия в присутствии крахмала.
|
Необходимые реактивы, посуда, оборудование: §реактивы Гюбля, Гануса, Кауфмана, Маргошеса, 1%-ный раствор крахмала (индикатор), 0,1 н раствор йода, 0,1 н, 0,01 н растворы тиосульфата натрия, 10%-ный раствор йодида калия, диэтиловый эфир, хлороформ, спиртово-эфирная смесь (для рефрактометра); §колбы для титрования с пришлифованными пробками (500 мл), пипетки, бюретки, мерные цилиндры; §водяная баня, аналитические весы, термостат. |
Реактив Гюбля. В 500 мл 96%-го этанола растворить 30 г сулемы. В 500 мл 96%-го этанола растворить 25 г кристаллического йода. Растворы хранить раздельно в темной посуде, смешать за двое суток (48 часов) до анализа. При необходимости раствор сулемы перед смешением фильтруют.
Реактив Гануса. В мерной колбе на 1 л растворить 13 г кристаллического йода в 700 мл ледяной уксусной кислоты, добавить 8,2 г брома (2,61 мл, r20 = 3,14 г/мл) и довести объем раствора уксусной кислоты до метки.
Раствор бромистого натрия и брома в метиловом спирте (метод Кауфмана). В 1 л метилового спирта (перегнанного над окисью кальция) растворить 140 г бромида натрия (NaBr), высушенного при 130 °С. Раствор хорошо перемешать и оставить на 24 часа. По истечении указанного срока к раствору прибавляют 5,1 мл брома. Через 10–15 минут раствор готов к употреблению.
Раствор Маргошеса. В 1000 мл 96%-го этилового спирта растворить 25 г дважды возогнанного йода. Раствор можно использовать в течение 14 дней. К 30 дню титр раствора меняется более чем на 3%.

