В основе флуоресцентного анализа фолиевой кислоты лежит специфическая реакция окисления перманганатом калия в кислой или щелочной среде с образованием птериновой (2-амино-4-гидрокси-птеридин-6-карбоновокислоты) и пара-аминобензоилглутаминовой кислот. Избыток перманганата калия удаляют путем добавления пероксидом водорода, при этом образовавшийся диоксида марганца отфильтровывают.
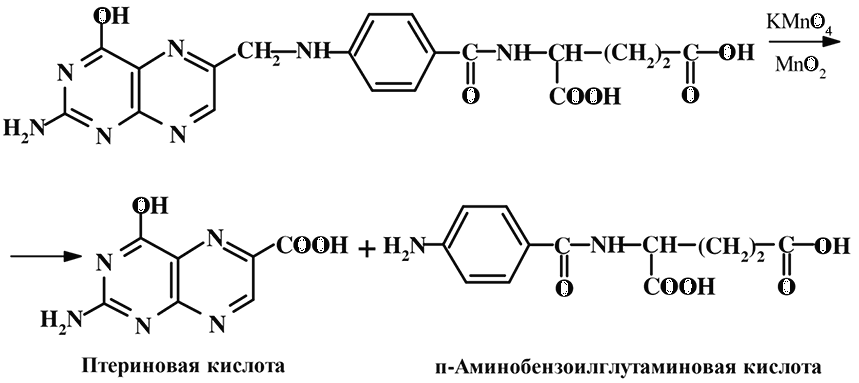
Полученный фильтрат, содержащий птериновую кислоту, имеет голубую флуоресценцию в ультрафиолетовом свете при длине волны 365 нм. Флуоресцентный метод определения фолатов в пищевых продуктах требует предварительной очистки экстрактов путем хроматографирования. Чувствительность данного метода составляет 0,01 мкг/мл.
Ход анализа. В плоскодонную колбу вместимостью 200 мл отмерить 35 мл молока, 45 мл дистиллированной воды и добавить несколько капель 15%-го раствора серной кислоты до достижения рН 3,5–4,0 (по индикаторной бумаге). Подсоединить воздушный холодильник и поместить колбу на кипящую водяную баню на 45 минут. Содержимое колбы охладить до температуры 32 оС и довести рН среды до рН 4,5–5,0, добавив 15%-ный раствор гидрооксида натрия.
В кислотный гидролизат внести 0,1 г ферментного препарата (амилоризина), 0,5 мл толуола и выдержать смесь в термостате при температуре 37 оС в течение 16–18 часов. Гидролизат охладить до комнатной температуры и количественно перенести в мерную колбу вместимостью 100 мл. Довести объем раствора дистиллированной водой до метки и отфильтровать через складчатый фильтр.
В плоскодонную колбу вместимостью 250 мл отмерить 50 мл фильтрата, подкислить смесь 15%-ным раствором серной кислоты (рН 3), внести 0,1 г активированного угля. Смесь прокипятить под тягой при аккуратном помешивании в течение 5 мин. Затем охладить до комнатной температуры и отфильтровать на воронке Бунзена при небольшом разряжении.
Для элюирования фолиевой кислоты заменить приемную колбу и промыть осадок на фильтре пять раз небольшими порциями нагретым до кипения 3%-ным спиртовым раствором аммиака. Общий расход элюата 70 мл (первый раз – 20 мл, второй, третий – 15 мл, четвертый и пятый – 10 мл).
Объединенные элюаты собрать в круглодонную колбу на шлифе и сконцентрировать на вакуумном испарителе до объема 10–15 мл. Остаток количественно перенести в мерную колбу вместимостью 25 мл, подкислить до рН 3, добавив 2%-ный раствор серной кислоты. По каплям прилить 4%-ный раствор перманганата калия до появления розового окрашивания, не исчезающего в течение 10 минут. Для удаления избытка перманганата калия внести по каплям 3%-ный раствор пероксида водорода. После обесцвечивания раствора довести рН среды до 4–4,5, используя 15%-ный раствор гидроксида натрия. Общий объем смеси довести до метки дистиллированной водой и отфильтровать.
Измерить интенсивность флуоресценции анализируемого образца и контрольного опыта на флуорометре относительно раствора сравнения. Длина волны первичного облучения 363 нм, вторичного излучения 460 нм. Массовую долю витамина В9 (СВ9, млн–1) рассчитать по формуле
где А, А1, Ар – среднеарифметическое значение показаний флуорометра для анализируемого образца, контрольного опыта, раствора сравнения, соответственно;
2 – масса фолиевой кислоты 1 мл рабочего раствора, мкг;
m – масса навески анализируемого продукта, г;
V – объем фильтрата взятого для адсорбции, 50 мл;
V1 – объем гидролизата, взятого на определение, 25 мл;
V2 – объем гидролизата после разбавления, 100 мл.
Контрольный опыт. В плоскодонную колбу вместимостью 100 мл отмерить 50 мл рабочего раствора фолиевой кислоты (2 мкг/мл), подкислить смесь 15%-ным раствором серной кислоты (до рН 3) и внести 0,1 г активированного угля. Дальнейшая обработка контрольного опыта аналогична обработке опытного образца. Раствор сравнения приготовить из рабочего раствора фолиевой кислоты без обработки.
Стандартный раствор фолиевой кислоты (0,2 мг/мл). Навеску перекристаллизованной фолиевой кислоты (0, 020 г) взвесить в стаканчике, растворить в 40 мл дистиллированной воды, подщелоченной тремя каплями 10%-го раствора гидроксида натрия. Раствор количественно перенести в мерную колбу вместимостью 100 мл и довести объем до метки.
Рабочий раствор фолиевой кислоты (2 мкг/мл) готовят непосредственно перед началом анализа. Для этого в мерную колбу вместимостью 100 мл отмерить пипеткой 1 мл стандартного раствора фолиевой кислоты и довести объем раствора до метки.
|
Необходимые реактивы, посуда, оборудование: §2, 5%-ные растворы серной кислоты, 10%-ный раствор гидрокисида натрия, 3%-ный спиртовой раствор аммиака (на 70%-ном этиловом спирте), 3%-ный раствор пероксида водорода, перекристаллизованная фолиевая кислота, ферментный препарат амилоризина, толуол, активированный уголь; §пипетки, делительные воронки, мерные колбы, колбы плоскодонные со шлифами, холодильники, воронки Шотта, воронка Бунзена, колбы круглодонные на шлифе; §аналитические весы, флуорометр (с набором светофильтров), водяная баня, термостат, вакуммный испаритель. |

