Общей цветной реакцией для производных пиридина или его незамещенных в a-положениях производных с хлор- и бромцианом является образование цианпиридиниевых солей, последующий гидролиз которых идет с раскрытием пиридинового цикла и образованием глутаконового альдегида.
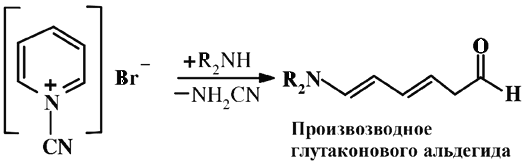
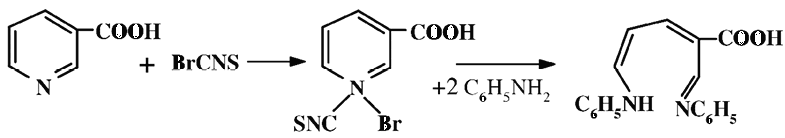
Производные глутаконового альдегида в реакции с нуклеофилами, например аминами, дают ярко окрашенные соединения, используемые при фотоколориметрическом определении как цианидов, так и a-незамещенных придинов. Так, например, при взаимодействии никотиновой кислоты с бромистым цианидом образуется цианбромидное производное никотиновой кислоты, которое в присутствии ароматических аминов дает интенсивно окрашенное соединение – дианилид. В аналитической практике вместо цианида используют роданбромид.
Метод стандартизирован – ГОСТ 30627.4–98 «Методы измерения массовой доли витамина РР (ниацина)».
Ход анализа. В круглодонную колбу вместимость 250 мл отмерить точную навеску измельченного анализируемого продукта (1–20 г) с содержанием никотиновой кислоты в пределах 100–150 мкг. Добавить 100 мл 1 н раствора соляной кислоты, подсоединить воздушный холодильник и выдержать колбу на кипящей водяной бане в течение 1 ч.
Охлажденный гидролизат нейтрализовать 40%-ным раствором гидроксида натрия до рН 6,5 (по индикатору – фенолфталеину) и охладить до комнатной температуры. К нейтрализованному гидролизату добавить 100 мл 96%-го этилового спирта при постоянном перемешивании. Выпавший осадок отфильтровать на воронке Бюхнера с использованием водоструйного насоса.
К прозрачному фильтрату добавить 2 г асканита и выдержать на вибросмесителе при постоянном перемешивании в течение 5 минут. Осадок – асконита и адсорбированную на нем никотиновую кислоту – отфильтровать через бумажный фильтр на воронке Бюхнера. Осадок вместе фильтром перенести в колбу, в которой фильтрат обрабатывали асканитом, и добавить мерным цилиндром 25 мл 1 н раствора гидроксида натрия (для элюирования никотиновой кислоты). Время элюирования – 3–5 минут.
Элюат перенести в центрифужную кювету и центрифугировать при скорости вращения 3000 об/мин (15 минут). Отфильтрованный элюат перелить в мерный цилиндр, которым отмеряли щелочь, замерить объем жидкости и перенести без потерь в мерный стакан. Затем добавить в стакан насыщенный раствор сернокислого цинка (1:1) до достижения рН 6,5 (по индикатору – фенолфталеину). Полученный густой осадок гидроксида цинка отфильтровать на воронке Бюхнера. Объем фильтрата измерить и количественно перенести в коническую колбу.
Фильтрат нагреть на электрической плитке и добавить 1 н раствор перманганата калия по каплям (около 5–6 капель) до получения прозрачного раствора с целью окисления посторонних примесей. Смесь охладить и разделить на центрифуге. Фугат перелить в химический стакан, внести 2–3 капели раствора фенолфталеина и прибавить несколько кристалликов фосфорнокислого калия (K3PO4) до появления розового окрашивания. Вновь довести рН среды до рН 6,5, добавив раствор разбавленной соляной кислоты (1:1) до обесцвечивания смеси. Образовавшийся осадок отфильтровать на воронке Бюхнера.
Для проведения цветной реакции отмерить пипеткой в круглодонную колбу 5 мл полученного бесцветного фильтрата и подсоединить воздушный холодильник. Колбу поместить на водяную баню и нагреть до температуры 70 оС. После чего прилить 2 мл горячего свежеприготовленного раствора роданбромида и 7 мл спиртового раствора анилина. Дать смеси отстояться в течение 0,5–1 ч при комнатной температуре и отфильтровать. Фильтрат колориметрировать в кювете с длиной оптического пути 10 мм при длине волны 440 нм относительно разбавленного раствора этилового спирта (1:1). Массовую долю никотиновой кислоты (СНК, млн–1) в анализируемой пробе рассчитать по формуле
где СК – содержание никотиновой кислоты в анализируемом растворе, найденное по калибровочному графику, мкг/мл;
m – масса навески анализируемого продукта, г;
V1 – объем элюата после добавления раствора сернокислого цинка, мл;
V2 – объем элюата после извлечения никотиновой кислоты раствором гидроксида натрия и центрифугирования, мл;
25 – объем 1 н раствора гидроксида натрия, взятого для элюирования никотиновой кислоты, мл.
Построение калибровочного графика. Для приготовления стандартного раствора никотиновой кислоты (50 мкг/мл) в мерную колбу вместимостью 100 мл отмерить пипеткой 5 мл рабочего раствора никотиновой кислоты (1 мг/мл) и довести объем до метки дистиллированной водой.
В плоскодонную коническую колбу вместимостью 100 мл отмерить 4 мл приготовленного стандартного раствора, добавить 25 мл 0,1 н раствора серной кислоты, 2 г асканита. Полученную смесь выдержать на встряхивателе 3 минуты, а затем отфильтровать через бумажный фильтр на воронке Бюхнера. Фильтр с асканитом перенести в коническую колбу, в которой обрабатывали стандартный раствор асканитом. Для элюирования никотиновой кислоты добавить 25 мл 1 н раствора гидроксида натрия, поместить колбу на встряхиватель на 3 минуты. Элюат перенести в центрифужную кювету и центрифугировать.
Объем фугата измерить с помощью мерного цилиндра, которым отмеряли щелочь, и перенести фугат без потерь в мерный стакан вместимостью 100 мл. Прилить в стакан насыщенный раствор сернокислого цинка до достижения рН 6,5 (по иономеру или индикатору). Полученный густой осадок гидроксида цинка отфильтровать на воронке Бюхнера, фильтрат перелить в коническую колбу. При нагревании на электрической плитке к полученному раствору добавить 1 н раствор перманганата калия по каплям (4–6 капель) до обесцвечивания раствора. Полученный прозрачный раствор довести до кипения, охладить и отделить осадок на центрифуге.
Фугат перенести в стакан, добавить несколько капель раствора фенолфталеина и внести кристаллический фосфорнокислый калий (K3PO4) до образования розового окрашивания. Довести рН раствора до 6,5 путем добавления разбавленного раствора соляной кислоты (1:1) и отфильтровать.
В четыре градуированные пробирки со шлифом отмерить пипеткой соответственно 2, 3, 4, 5 мл фильтрата, объем каждого раствора довести до 5 мл дистиллированной водой. Подсоединить воздушные холодильники и поместить пробирки в кипящую водяную баню на 5 минут. Цветную реакцию провести так же, как и для анализируемого раствора, добавив в каждую градуированную пробирку по 2 мл раствора роданбромида и 7 мл спиртового раствора анилина. Спустя 30–60 минут калибровочные растворы отфильтровать и измерить оптическую плотность при длине волны 440 нм в кювете с длиной оптического пути 10 мм относительно разбавленного раствора этилового спирта (1:1).
На основе полученных результатов построить калибровочный график в координатах: оптическая плотность (А440) – содержание никотиновой кислоты (СНК, мкг/мл).
|
Необходимые реактивы, посуда, оборудование: §1 н раствор соляной кислоты, 20%-ный раствор гидроксида натрия, 48 и 96%-ный растворы этилового спирта, асканит (отбеливающая глина), 1 н раствор гидроксида натрия, 50%-ный раствор сульфата цинка, индикаторный раствор фенолфталеина, 1 н раствор перманганата калия (KMnO4), кристаллический безводный фосфат калия (K3PO4)), 18%-ный раствор соляной кислоты, раствор роданбромидного реактива (BrCNS), спиртовой раствор анилина, рабочий раствор никотиновой кислоты (1 мг/мл); §круглодонные колбы (250 мл), конические плоскодонные колбы (100 мл), воздушные холодильники, водяная баня, колбы Бунзена и воронки Бюхнера, мерные цилиндры (50 мл), мерные стаканы (100 мл), пипетки, калиброванные пробирки (20 мл); §аналитические весы, центрифуга, встряхиватель, фотоэлектороколориметр, иономер, электрическая плитка. |
Рабочий раствор никотиновой кислоты (1 мг/мл). Точную навеску никотиновой кислоты (0,1 г) растворить в 20 мл 96%-го этилового спирта и количественно перенести в мерную колбу вместимостью 100 мл, объем раствора довести до метки дистиллированной водой.
Раствор роданбромидного реактива. В стаканчике вместимостью 50 мл растворить 1 г кристаллического бромистого калия (KBr) в 10 мл 0,1 н раствора роданида калия (KCNS), добавить 1 мл 18%-го раствора соляной кислоты и по каплям прилить 2 мл брома (r=3,14 г/мл). Раствор использовать сразу, не давая ему остыть.
Спиртовой раствор анилина (1:6). В стаканчике вместимостью 100 мл растворить 10 г анилина (свежеперегнанного) в 60 мл 96%-го этилового спирта. Полученный бесцветный раствор хранить в холодильнике в темной склянке с притертой пробкой.

