Спектрофотометрический метод применим для количественного анализа окисленной и восстановленной форм рибофлавина в растительных продуктах. Для разрушения коферментных форм используют кислотный гидролиз, а в качестве окислителя восстановленной формы рибофлавина – гексацианоферрат калия (красная кровяная соль).
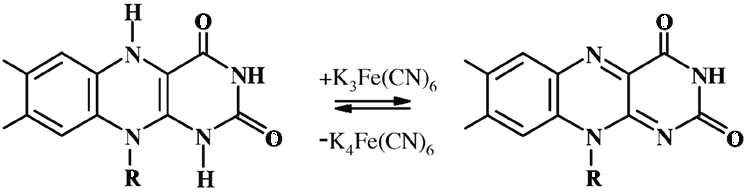
Ход анализа. Навеску анализируемого растительного продукта (около 1 г) тщательно растереть в фарфоровой ступке с добавлением 15 мл 0,1 н раствора соляной кислоты. Гомогенизированную массу количественно перенести в мерную колбу вместимостью 100 мл, с таким расчетом, чтобы общий объем составил 75 мл. Колбу выдержать на кипящей водяной бане в течение 45 минут. Содержимое колбы охладить, довести объем кислотного гидролизата до метки 0,1 н раствором соляной кислоты и отфильтровать.
Измерить оптическую плотность гидролизованного анализируемого раствора при 445 нм в кюветах с длиной оптического пути 10 мм, в качестве раствора сравнения использовать 0,1 н раствор соляной кислоты. По величине оптической плотности и по калибровочному графику определить концентрацию рибофлавина. Массовую долю окисленной формы витамина В2 (, млн–1) рассчитать по формуле
где СК – количество рибофлавина, найденного по калибровочному графику, мкг/мл;
V – общий объем кислотного гидролизата, 100 мл;
m – навеска исследуемого материала, г.
Определение общего содержания рибофлавина. В пробирку с притертой пробкой отмерить 5 мл отфильтрованного гидролизата и нейтрализовать его до рН 7 путем добавления 0,1 н раствор гидроксида натрия. К нейтрализованному гидролизату прилить окислитель – 0,5 мл 0,05 н щелочного раствора красной кровяной соли до появления красного окрашивания. Для разрушения избытка красной кровяной соли прилить около 1,5 мл 18%-го раствора глюкозы при непрерывном перемешивании до обесцвечивания. Обесцвеченный раствор выдержать на кипящей водяной бане в течение 30 минут. Суммарную массовую долю окисленной и восстановленной форм витамина В2 (СВ2, млн–1) рассчитать по формуле
где СК – количество рибофлавина, найденного по калибровочному графику, мкг/мл;
V – общий объем кислотного гидролизата, 100 мл;
V1 – объем гидролизата, взятого на окисление восстановленной формы рибофлавина, 5 мл;
m – навеска исследуемого материала, г.
Построение калибровочного графика. Точную навеску кристаллического рибофлавина (0,02 г) растворить в 100 мл дистиллированной воды и количественно перенести в мерную колбу вместимостью 500 мл (с таким расчетом, чтобы содержание витамина составляло 0,04 мг/мл). Из стандартного раствора приготовить пять калибровочных растворов с массовой концентрацией рибофлавина 2–12 мкг/мл по схеме, приведенной в табл. 2.2.10.
Таблица 2.2.10. Схема приготовления калибровочных растворов рибофлавина
|
Номер калибровочного раствора |
1 |
2 |
3 |
4 |
5 |
|
Объем стандартного раствора В2, мл |
2,5 |
5,0 |
7,5 |
10,0 |
15,0 |
|
Содержание витамина В2 в калибровочном растворе (мкг/мл) |
2,0 |
4,0 |
6,0 |
8,0 |
12,0 |
В мерные колбы вместимостью 50 мл отмерить соответствующее количество стандартного раствора витамина В2, довести объем до метки. Измерить оптическую плотность калибровочных растворов при 445 нм в кюветах с длиной оптического пути 10 мм относительно 0,1 н раствора соляной кислоты. Построить калибровочный график в координатах: оптическая плотность (А445) – содержание витамина В2 (СВ2, мкг/мл).
|
Необходимые реактивы, посуда, оборудование: §стандартный раствор витамина В2 (0,04 г/мл), 0,1 н раствор соляной кислоты, щелочной раствор железосинеродистого калия (красной кровяной соли), 18%-ный раствор глюкозы; §пипетки, фарфоровые ступки с пестиками, мерные колбы, пробирки с притертыми пробками; §аналитические весы, спектрофотометр (λ=445 нм), водяная баня, термостат. §Щелочной раствор железосинеродистого калия (K3Fe(CN)6). Навеску железосинеродистого железа (16,5 г) и карбоната калия (70 г) растворить в 500 мл объем дистиллированной воды в мерной колбе вместимостью 1000 мл. Объем раствора довести до метки. |

