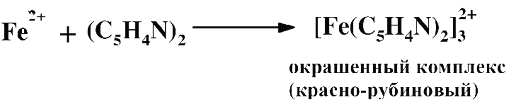
В основе определения токоферолов с использованием в качестве окислителя хлорида железа (III) лежит измерение интенсивности окраски комплекса восстановленного токоферолом хлорида железа (II) и 2, 2'-дипиридила в кислой среде (рН 1–2). Последний образует с ионами железа (II) устойчивый комплекс красно-рубинового цвета.
Определение витамина Е в пищевых продуктах с использованием колориметрических методов осложнено невысокой специфичностью метода. Многие вещества, содержащиеся в исследуемых объектах, при окислении способны подобно α-токоферолу давать окрашенные продукты с аналогичным аналитическим сигналом. С целью повышения селективности определения посторонние вещества (каротиноиды, стеролы, витамин А) удаляют, применяя щелочное омыление спиртовым раствором гидроксида калия с добавлением антиоксидантов (пирогаллола, аскорбиновой кислоты), с последующей экстракцией токоферола из неомыленной части диэтиловым эфиром.
Для определения токоферолов в продуктах питания и продуктах, обогащенных витамином Е, используют стандартизированный метод (ГОСТ 30627.3–98 – «Продукты молочные для детского питания»), для которого обязательной стадией является предварительное выделение жировой фракции путем экстракции. Применяют и другие способы выделения, а также прямое омыление навески.
Ход анализа. Анализируемую пробу (жидкую или пастообразную) выдержать при температуре 37 оС в течение 20–30 минут для равномерного распределения жировой фракции. На аналитических весах в круглодонную колбу со шлифом вместимостью 100 мл взвесить навеску (около 15 г) жидкого или пастообразного продукта и растворить в 10 мл дистиллированной воды. При анализе сухих продуктов массу навески выбрать в зависимости от количества содержащегося витамина (табл. 2.1.19).
Таблица 2.1.19. Зависимость массы навески жиросодержащего продукта
от массовой доли витамина Е
|
Массовая доля витамина Е, млн–1 |
Масса навески сухого продукта, г |
|
8,5–16 |
10,0 |
|
15–45 |
5,0 |
|
45–120 |
2,0 |
К анализируемой пробе добавить аскорбиновую кислоту (0,1– 0,15 г), прилить 40 мл этилового спирта, перемешать и внести 5–7 мл 9 н раствора гидроксида калия. Соединить колбу с обратным холодильником и выдержать на кипящей водяной бане в течение 30 минут. По окончании гидролиза анализируемую пробу охладить до комнатной температуры и отсоединить холодильник.
Содержимое колбы количественно перенести в делительную воронку. Колбу трижды ополоснуть дистиллированной водой (общий объем воды 50 мл), а полученные смывы собрать в делительную воронку. Признаком полноты гидролиза является отсутствие помутнения гидролизата при добавлении воды. В случае образования мути гидролиз повторить, увеличив объем щелочи.
К гидролизату добавить 25 мл диэтилового эфира, закрыть воронку пробкой и энергично встрянуть несколько раз. Дождаться разделения водного и органического слоев, отделить органический слой (верхний). Экстракцию неомыляемых веществ повторить дважды, добавляя каждый раз новую порцию диэтилового эфира по 25 мл.
Эфирные вытяжки объединить, перенести в делительную воронку и трижды промыть дистиллированной водой до нейтральной реакции промывной жидкости по фенолфталеину (общий объем воды 50 мл). В сухую, предварительно взвешенную круглодонную колбу отфильтровать эфирные вытяжки на воронке Шотта через слой безводного сульфата натрия (20–30 г). Осадок на фильтре промыть трижды диэтиловым эфиром (общий объем эфира не более 15 мл).
Колбу с объединенным эфирным фильтратом подсоединить к ротационному вакуумному испарителю и отогнать растворитель в атмосфере инертного газа на водяной бане при температуре не выше 30 оС. Неомыляемый остаток растворить в 15 мл абсолютного этилового спирта.
На анализ отобрать 1–5 мл спиртового раствора неомыляемого остатка (в зависимости от содержания токоферола), довести объем раствора до 5 мл абсолютным этиловым спиртом. К спиртовому раствору прилить 0,5 мл 0,5%-го спиртового раствора 2, 2'-дипиридила, 0,5 мл 0,025%-го спиртового раствора хлорида железа (III), перемешать. Не ранее чем через 20 с добавить 0,5 мл 0,03 М спиртового раствора ортофосфорной кислоты и вновь перемешать. Параллельно провести холостой опыт на реактивы.
Для приготовления холостого опыта к 5 мл абсолютного этилового спирта прилить 0,5 мл 0,5%-го спиртового раствора 2, 2'-дипиридила, 0,5 мл 0,025%-го спиртового раствора хлорида железа (III), не более чем через 20 с добавить 0,5 мл 0,03 М спиртового раствора ортофосфорной кислоты. Измерить оптическую плотность анализируемой и холостой проб на фотоэлектроколориметре при длине волны 490 нм в кюветах с длиной оптического пути 10 мм относительно абсолютного этилового спирта. Массовую долю a-токоферола (Сa-ТФ, млн–1) вычислить по формуле:
где mК – масса a-токоферола в анализируемой пробе, установленная по калибровочному графику (по разнице значений оптических плотностей между опытной и холостой пробами относительно абсолютного этилового спирта), мкг;
m – масса навески продукта, взятая на гидролиз, г;
V – общий объем раствора неомыляемого остатка в абсолютном этиловом спирте, 15 мл;
V1 – объем спиртового раствора, взятого на цветную реакцию, 1–5 мл.
Гидролиз стандартного раствора a-токоферола. В круглодонную колбу вместимостью 100 мл отмерить пипеткой 5 мл стандартного раствора a-токоферола (0,4 мг/мл), добавить 15 мл этилового спирта, 0,1 г аскорбиновой кислоты и 1 мл 9 н раствора гидроксида калия. Колбу соединить с обратным холодильником и выдержать в кипящей водяной бане 20 минут. По окончании гидролиза колбу охладить, отсоединить холодильник и количественно перенести полученный гидролизат в делительную воронку. Колбу трижды ополоснуть дистиллированной водой (общий объем воды 50 мл), а полученные смывы собрать в делительную воронку. Дальнейшую экстракцию неомыляемых веществ вести по методике, описанной выше для анализируемой пробы.
Колбу с эфирным экстрактом неомыляемых веществ подсоединить к ротационному вакуумному испарителю и отогнать растворитель в атмосфере инертного газа на водяной бане при температуре не выше 30 оС. Неомыляемый остаток растворить в 15 мл абсолютного этилового спирта, количественно перенести раствор в мерную колбу вместимостью 100 мл и довести объем раствора до метки тем же растворителем. Концентрация стандартного раствора a-токоферола после гидролиза должна составлять не менее 20 мкг/мл.
Проверка концентрации стандартного раствора a-токоферола. Измерить оптическую плотность стандартного спиртового раствора a-токоферола на спектрофотометре при длине волны 292 нм в кюветах с длиной оптического пути 10 мм относительно абсолютного спирта. Рассчитать массовую концентрацию (ССТ, мкг/мл) стандартного раствора a-токоферола по формуле:
где А – оптическая плотность стандартного раствора a-токоферола относительно абсолютного этилового спирта;
– удельный показатель поглощения при длине волны 292 нм для 1%-го раствора a-токоферола в абсолютном этиловом спирте, 75 мл/мкг×см;
104 – концентрация a-токоферола 1%-го раствора a-токоферола, мкг/мл;
l – длина оптического пути, 1 см.
Построение калибровочного графика. Из рабочего раствора a-токоферола (20 мкг/мл) в градуированных пробирках приготовить пять калибровочных растворов по схеме (табл. 2.1.20) и довести объем растворов до 5 мл абсолютным этиловым спиртом.
Таблица 2.1.20. Схема приготовления калибровочных растворов a-токоферола
|
Номер калибровочного раствора |
1 |
2 |
3 |
4 |
5 |
|
Объем рабочего раствора a-токоферола, мл |
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
|
Содержание a-токоферола, мкг/мл |
2 |
4 |
6 |
8 |
10 |
В шестой пробирке приготовить холостой опыт, для этого отмерить пипеткой 5 мл абсолютного этилового спирта. Во все шесть пробирок прилить по 0,5 мл 0,5%-го спиртового раствора 2, 2'-дипиридила, 0,5 мл 0,025%-го спиртового раствора хлорида железа (III) и перемешать. Не ранее чем через 20 с добавить 0,5 мл 0,03 М спиртового раствора ортофосфорной кислоты и вновь перемешать полученные растворы.
Измерить оптическую плотность калибровочных растворов и холостой пробы на фотоколориметре при длине волны 490 нм в кюветах с длиной оптического пути 10 мм относительно абсолютного этилового спирта. Построить калибровочный график в координатах: разность показаний оптической плотности калибровочных растворов и холостого опыта (А490) – содержание a-токоферола (Сa-ТФ , мкг/мл).
|
Необходимые реактивы, посуда, оборудование: §диэтиловый эфир, абсолютный этиловый спирт, 0,2- и 0,025%-ный спиртовой раствор хлорида железа (FeCl3 · 6H2O), сульфат натрия свежепрокаленный, аскорбиновая кислота, 0,5%-ный спиртовой раствор 2, 2’-дипиридила (С10Н8N2), 0,03 М спиртовой раствор ортофосфорной кислоты (Н3РО4), 9 н раствор гидроксида калия, 1%-ный спиртовой раствор фенолфталеина, 100%-ный препарат a-токоферол ацетата или 30%-ный масляный раствор; §колбы с пришлифованными пробками вместимостью 250 мл, обратные холодильники, делительные воронки, воронки Шотта, мерные колбы вместимостью 100 мл, пипетки, градуированные пробирки; §аналитические весы, фотоэлектроколориметр (l=490 нм, кюветы с длиной оптического пути 10 мм), спектрофотометр (l=292 нм), ротационный вакуумный испаритель, водяная баня. |
Стандартный раствор a-токоферола (0,4 мг/мл). Точную навеску 0,04 г препарата a-токоферолацетата или 30%-ный масляный раствор a-токоферолацетата растворить в 20 мл абсолютного этилового спирта, количественно перенести в мерную колбу вместимостью 100 мл и довести объем раствора до метки тем же растворителем.
Рабочий раствор a-токоферола (20 мкг/мл). В мерную колбу вместимостью 50 мл отмерить 2,5 мл стандартного раствора a-токоферола (0,4 мг/мл) и довести объем раствора до метки абсолютным этиловым спиртом.
0,2%-ный спиртовой раствор хлорида железа. Точную навеску 0,2 г треххлористого железа (FeCl3 · 6H2O) растворить в 25 мл абсолютного этилового спирта, количественно перенести в мерную колбу вместимостью 100 мл и довести объем раствора тем же растворителем до метки. Хранить раствор в темной склянке в холодильнике.
0,025%-ный спиртовой раствор хлорида железа. К 1,25 мл 0,2%-го спиртового раствора треххлористого железа добавить 8,75 мл абсолютного этилового спирта и перемешать.
0,03 М спиртовой раствор ортофосфорной кислоты. Точную навеску 0,327 г ортофосфорной кислоты растворить в 25 мл абсолютного этилового спирта, количественно перенести в мерную колбу вместимостью 100 мл и довести объем раствора тем же растворителем до метки.
0,5%-ный спиртовой раствор 2,2'-дипиридила. Точную навеску 0,5 г 2, 2'-дипиридила (С10Н8N2) растворить в 25 мл абсолютного этилового спирта, количественно перенести в мерную колбу вместимостью 100 мл и довести объем раствора тем же растворителем до метки.

