Витамин А дает окрашенные соединения сложной структуры с треххлористой сурьмой, треххлористым мышьяком, дихлоргидрином глицерина. На практике для количественного анализа продуктов, содержащих витамин А, используют метод Карра – Прайса.
Определение витамина А по реакции с хлоридом сурьмы
В основе метода Карра – Прайса лежит цветная реакция хлороформного экстракта витамина А с раствором треххлористой сурьмы в присутствии уксусного ангидрида. В результате водоотнимающего действия хлорида сурьмы витамин А превращается в соединение сложного состава синего цвета с максимумом поглощения при 620 нм. Качественная реакция хлорида сурьмы с веществами, обладающими А-витаминной активностью, не специфична – аналогичное окрашивание дают все соединения с сопряженными связями. Образующаяся синяя окраска не стабильна и переходит со временем в розово-фиолетовую, что осложняет анализ и требует строгого соблюдения времени выдерживания до фотометрирования. Кроме того, присутствие влаги в реакционной смеси даже в незначительном количестве вызывает гидролиз хлорида сурьмы до хлороксида сурьмы, который не реагирует с витамином А, а вызывает помутнение смеси. Поэтому для устранения следов влаги в реакционную смесь добавляют уксусный ангидрид.
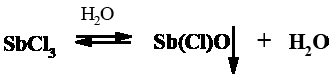 ,
,
Ход анализа. Точную навеску анализируемого продукта (3–6 г сухого или 15 г жидкого продукта) растворить в 20 мл дистиллированной воды в круглодонной колбе со шлифом вместимостью 250 мл. После полного растворения навески добавить 40 мл этилового спирта и 5–7 мл 50%-го раствора гидроксида калия. Колбу закрыть обратным холодильником и поместить в водяную баню при температуре 85 0С. Для стабилизации витамина А добавить 30–50 мг аскорбиновой кислоты.
Спустя 30 минут колбу с гидролизатом вынуть из бани, охладить и отсоединить холодильник. Содержимое колбы количественно перенести в делительную воронку. Колбу трижды ополоснуть небольшими порциями дистиллированной воды (общий объем 50 мл). Смывы объединить с основным гидролизатом и собрать в делительной воронке. Гидролизат, содержащий неомыляемую фракцию, трижды экстрагировать диэтиловым эфиром, используя на каждую экстракцию по 50 мл эфира. Эфирные вытяжки объединить и отмыть от щелочи дистиллированной водой до отрицательной реакции промывных вод по фенолфталеину. Объем дистиллированной воды не должен превышать 500 мл.
Органический слой (верхний) отделить и собрать в плоскодонную колбу. Эфирный экстракт оставить над осушителем (20 г безводного сульфата натрия) при периодическом перемешивании. Спустя 30 минут осушитель отфильтровать в круглодонную колбу со шлифом через воронку Шотта. Дважды промыть осушитель на фильтре небольшими порциями диэтилового эфира (по 10 мл). Растворитель отогнать на ротационном вакуумном испарителе в атмосфере инертного газа при температуре не выше 40 оС, полученный неомыляемый остаток растворить в 10 мл безводного хлороформа, количественно перенести в мерную колбу вместимостью 25 мл и довести объем до метки хлороформом. Концентрация витамина А должна составить примерно 3 мкг/мл.
В колориметрическую кювету внести 0,4 мл полученного раствора, добавить 1–3 капли уксусного ангидрида, 4 мл насыщенного раствора треххлористой сурьмы в хлороформе и перемешать. Не позднее чем через 10 с измерить оптическую плотность раствора на фотоэлектроколориметре при длине волны 620 нм в кювете с длиной оптического пути 10 мм относительно раствора хлороформа. Массовую долю витамина А (СА, млн–1) рассчитать по формуле:
где СК – концентрация витамина А, найденная по калибровочному графику, МЕ/мл;
V1 – объем раствора неомыляемой части в хлороформе, 25 мл;
m – навеска исследуемого продукта, г;
0,303 – коэффициент пересчета МЕ в млн–1.
Построение калибровочного графика. Точную навеску кристаллического ретинолацетата, содержащего не менее 105 МЕ/мл, растворить в хлороформе (в мерной посуде) с таким расчетом, чтобы содержание ретинолацетата составило около 100 МЕ/мл. Из стандартного раствора приготовить пять калибровочных растворов с массовой концентрацией ретинолацетата 2–10 МЕ/0,4 мл (табл. 2.1.7).
Таблица 2.1.7. Схема приготовления калибровочных растворов ретинолацетата
|
Номер калибровочного раствора |
1 |
2 |
3 |
4 |
5 |
|
Объем стандартного раствора |
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
|
Концентрация витамина калибровочного раствора (МЕ/0,4 мл) |
2 |
4 |
6 |
8 |
10 |
Для этого в градуированные пробирки отмерить необходимое количество стандартного раствора ретинолацетата и довести объем калибровочных растворов до 10 мл хлороформом. В кювету для колориметрирования отобрать пипеткой по 0,4 мл каждого калибровочного раствора, добавить 1–3 капли уксусного ангидрида, 4 мл насыщенного раствора треххлористой сурьмы в хлороформе и не позднее чем через 10 с измерить оптическую плотность при длине волны 620 нм в кюветах с длиной оптического пути 10 мм. Построить калибровочный график в координатах: оптическая плотность (А620) – содержание ретинол ацетата (СА, МЕ/мл).
Определение витамина А по реакции с 1,3-дихлор-2-пропанолом
Метод основан на реакции витамина А с соляной кислотой в среде 1,3-дихлор-2-пропанола (гидриновый реактив). Образующееся при этом соединение имеет фиолетовую или фиолетово-пурпурную окраску. Максимум поглощения лежит в области 550 нм. При взаимодействии витамина А с 1,3-дихлор-2-пропанолом образуется более стабильное соединение, чем с хлоридом сурьмы, сохраняющее окраску постоянной в течение 2–10 минут. Однако чувствительность данного метода ниже, а интенсивность окраски образующегося продукта реакции в пять раз слабее, чем при использовании метода Карра – Прайса (с треххлористой сурьмой).
Ход анализа. Подготовка пробы к анализу аналогична методу Карра – Прайса. Для омыления 5 г анализируемого продукта внести 10 мл 20%-го спиртового раствора гидроксида калия. Неомыляемые вещества экстрагировать диэтиловым эфиром, после удаления эфира полученный остаток растворить в необходимом количестве хлороформа.
В кювету для колориметрирования отмерить пипеткой 1 мл полученного раствора неомыляемого остатка, добавить 2 мл гидринового реактива и спустя 5 минут колориметрировать при длине волны 550 нм в кювете с длиной оптического пути 10 мм относительно рабочего раствора сравнения витамина А (рабочий раствор приготовить из стандартного раствора сравнения). Рассчитать массовую долю витамина А (СА, млн–1) по формуле:
где e – экстникция исследуемого раствора;
eС – экстникция рабочего раствора сравнения;
V1 – объем неомыляемого остатка в хлороформе, мл;
0,03 – содержание витамина А в стандартном растворе, 0,03 мг/мл;
V2 – общий объем раствора, взятый для колориметрирования, 1 мл;
m – масса навески исследуемого продукта, г;
1000 – коэффициент пересчета в млн–1.
Экстракция витамина А из пищевых продуктов
Провести омыление жира рыб или млекопитающих (навеска – 0,5–1 г) с добавлением 10 мл 0,5 н спиртового раствора гидроксида калия. Далее, как описано в методике выше.
Провести омыление сливочного или топленого масла (навеска – 10–20 г) с использованием 20–40 мл 20%-го спиртового раствора гидроксида калия в течение 1–2 часов при температуре 85–90 оС. К охлажденному раствору добавить 20–40 мл дистиллированной воды и экстрагировать диэтиловым эфиром. На первую экстракцию использовать 75 мл, экстрагента, две последующие по 25 мл. Далее, как описано в методике.
Молоко в количестве 100–200 мл смешать 10–20 мл 60%-го раствора гидроксида калия, добавить 20–40 мл этилового спирта и оставить на 48 часов в темном месте при 20–25 оС при небольшом перемешивании. Неомыляемую часть экстрагировать диэтиловым эфиром в четыре приема. На первую экстракцию использовать 75 мл экстрагента, две последующие по 25 мл. Далее – по методике.
Печень. Гомогенизированную навеску печени (около 1 г) залить 1 мл 60%-го раствора гидроксида калия и 10–20 мл этилового эфира. Гидролиз вести в течение 2–4 часов при температуре 85–90 0С. Далее – по методике.
Яичный желток. К 20 г яичного желтка добавить 6 мл 60%-го раствора гидроксида калия и 10–20 мл этилового спирта. Время гидролиза – 2 часа при температуре 85–90 оС. Далее – по методике.
Витаминизированные кондитерские изделия. Кондитерские изделия (конфеты, пряники) экстрагировать путем настаивания. Для этого 20–50 г исследуемого продукта трижды проэкстрагировать диэтиловым эфиром, затрачивая на каждую экстракцию по 20 мл. Объединенные эфирные вытяжки отфильтровать, растворитель отогнать на ротационном вакуумном испарителе в атмосфере инертного газа. Полученный остаток растворить в хлороформе. Далее – по методике.
Определение витамина А совместно с каротином. Эфирный экстракт осушить и отогнать растворитель в атмосфере инертного газа. Остаток неомыляемых липидов обработать разными способами. Для определения витамина А остаток после удаления диэтилового эфира растворить в хлороформе, для определения каротина – в петролейном эфире.
|
Необходимые реактивы, посуда, оборудование: §20, 50%-ный раствор гидроксида калия, этиловый спирт (ректификат), аскорбиновая кислота, диэтиловый эфир, абсолютный хлороформ, индикатор – раствор фенолфталеина, осушитель – безводный сульфат натрия, уксусный ангидрид, раствор хлорида сурьмы (III) в хлороформе), 1,3-дихлор-2-пропаноле (гидриновый реактив), стандартный раствор витамина А (ацетат или пальмитат), стандартный и рабочий растворы сравнения витамина А (метилового фиолетового и сафронина); §пипетки; колбы с пришлифованными пробками вместимостью 250 мл, плоскодонные колбы, обратные холодильники, водяная баня (80 оС), делительные воронки, воронки Шотта, мерная колба вместимостью 100 мл, пробирки, фотоколориметрические кюветы с длиной оптического пути 10 мм; §аналитические весы; водяная баня, ротационный вакуумный испаритель, фотоколориметр (λ 620, 550 нм). |
Раствор хлорида сурьмы (SbCl3). Хлорид сурьмы на фильтре промыть хлороформом до тех пор, пока стекающий раствор не станет бесцветным. Промытый реактив высушить в эксикаторе, используя в качестве осушителя концентрированную серную кислоту, в течение суток. Из осушенного реактива приготовить насыщенный раствор в хлороформе.
Раствор хлорида сурьмы (реактив Карра – Прайса). В конической колбе с пришлифованной пробкой вместимостью 500 мл растворить в хлороформе при нагревании на водяной бане (40 оС) 60 г хлорида сурьмы. После растворения осадка раствор охладить до комнатной температуры, внести 6–9 мл уксусного ангидрида. Колбу с раствором хлорида сурьмы закрыть пробкой и оставить в темном месте на 14–18 часов для отстаивания. Полученный прозрачный раствор аккуратно слить в склянку из темного стекла. Срок хранения раствора не более 40 дней при комнатной температуре.
Гидриновый реактив (соляная кислота в 1,3-дихлор-2-пропаноле). Смешать 2 мл концентрированной соляной кислоты с 98 мл 1,3-дихлор-2-пропанола и перелить в склянку из темного стекла. Хранить в холодильнике.
Стандартный раствор сравнения. В мерную колбу вместимостью 1 л внести 10 мг метилового фиолетового и 2,3 мг сафронина и довести объем до метки дистиллированной водой.
Рабочий раствор сравнения (эталонный раствор). К 12 мл стандартного раствора сравнения добавить 13 мл дистиллированной воды и перемешать. Величина экстинкции 1 мл рабочего раствора сравнения соответствует 0,03 мг витамина А.
Определение витамина А методом ТСХ
В колбу для омыления взвесить на аналитических весах навеску измельченного анализируемого продукта 0,05–0,10 г, добавить 20 мл этанола, 100 мг пирогаллола или гидрохинона, 5 мл 60%-го раствора гидроксида калия и подсоединить к колбе обратный холодильник. Омыление вести на глицериновой бане при температуре 90 оС в течение 30 минут.
Колбу с гидролизатом охладить до комнатной температуры, перелить щелочной гидролизат в делительную воронку и провести трехкратную экстракцию гексаном (каждая порция экстрагента по 30 мл). Объединенные экстракты промыть дистиллированной водой до нейтральной реакции (по универсальной индикаторной бумаге) и отфильтровать через безводный сульфат магния в круглодонную колбу со шлифом. Осушитель промыть на фильтре небольшими порциями гексана, промывные растворы объединить с основным фильтратом. Из полученного фильтрата удалить растворитель на ротационном вакуумном испарителе в инертной атмосфере, образовавшийся остаток растворить в хлороформе.
На стартовую линию пластины Silufol нанести 0,1 мл хлороформного раствора неомыляемого остатка. Рядом на линию старта пластины нанести каплю свидетеля – стандартного раствора ретинолацетата (0,5 мкг.). Поместить пластины в хроматографическую камеру. В качестве подвижной фазы использовать смесь хлороформ–гептан (94:6).
После достижения фронтом растворителя верхнего края пластину извлечь ее из камеры, подсушить и «проявить» путем опрыскивания 0,2%-ным раствором хлорного железа. Высушенную пластину поместить в камеру, насыщенную парами йода. Витамин А проявляется в виде темно-синей полосы на голубовато-коричневом фоне. Пластину снова подсушить теплым воздухом до ее полного обесцвечивания (исчезновения следов йода) и обработать 0,5%-ным спиртовым раствором 2, 2’-дипиридила. В итоге на белом фоне пластины должна проявиться розово-красная полоса, соответствующая витамину А. Определить величину Rf пробы относительно со свидетелем (стандартом).
Закрепить окраску образующегося комплекса на пластине, обработав парами аммиака. Окрашенную зону пластины вырезать ножницами и перенести в пробирку с притертой пробкой. В пробирку добавить элюент – смесь этанола, соляной кислоты, фосфорной кислоты и дистиллированной воды в объемных соотношениях 6:3:1:2.
Окрашенный элюата отфильтровать через бумажный фильтр. Оптическую плотность раствора измерить при длине волны 490 нм в кюветах с длиной оптического пути 10 мм относительно раствора сравнения (элюент). Содержание витамина определить по калибровочному графику.
|
Необходимые реактивы, посуда, оборудование: §96%-ный этиловый спирт, пирогаллол (или гидрохинон), 60%-ный раствор гидроксида кали, гексан, индикаторная бумага, безводный сульфат магния, пластины Silufol, хлороформ, стандартный раствор ацетата ретинола, гептан, 0,2%-ный раствор хлорного железа, кристаллический йод, элюент (смесь этанола, соляной кислоты, фосфорной кислоты и дистиллированной воды в объемных соотношениях 6:3:1:2), 25%-ный раствор аммиака, 0,5%-ный спиртовой раствор 2, 2’-дипиридила; §пипетки; колбы круглодонные с пришлифованными пробками, плоскодонные колбы, обратные холодильники, делительные воронки, воронки Шотта, мерные колбы, пробирки, фотоколориметрические кюветы с длиной оптического пути 10 мм; §аналитические весы; ротационный вакуумный испаритель, фотоэлектроколориметр, хроматографическая камера, глицериновая баня. |

