Метод активного кислорода является косвенным методом определения абсорбции кислорода и основан на определении перекисного числа при аэрации пробы при 80 или 110 оС до достижения перекисного числа, равного 0,5% йода (или 39 ммоль ½О2 /кг) для растительных масел и 0,1% йода (или 7,8 ммоль ½О2 /кг) для животных жиров.
Метод активного кислорода применим для определения стойкости к окислению жиров, не содержащих фосфолипидов (или содержащих в небольших количествах). Также он используется при определении сравнительной эффективности синтетических и натуральных ингибиторов окисления.
В процессе использования метода активного кислорода часто не ограничиваются лишь наблюдением за изменением только перекисных чисел. Параллельно определяют и другие показатели жиров (тиобарбитуровое число, анизидиновое число и др.). Анализ ведут при 80 оС или 110 оС. Температурный режим 110 оС применяют лишь для жиров, у которых индукционный период не менее 3 часов.
Таким образом, метод активного кислорода заключается в продувании воздуха с постоянной скоростью через фиксированный слой жира при повышенной постоянной температуре и определении перекисного числа в нем через равные промежутки времени. При окислении растительных масел отбор проб вначале проводят каждые один-два часа до возрастания перекисного числа приблизительно в два раза, затем каждые 20–30 минут. Пробы животных жиров, обладающих меньшей стабильностью, отбирают вначале каждые 30–60 минут, а затем каждые 20–30 минут. Определение выполняют в приборе, изображенном на рис. 15.
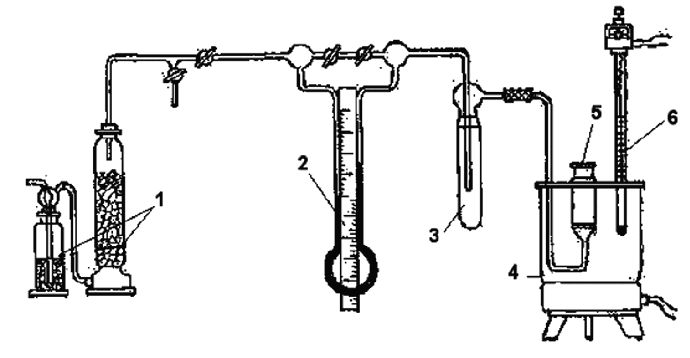
Рис. 15. Установка для определения устойчивости жиров к окислению:
1 – склянки с осушителями воздуха; 2 – капиллярный реометр; 3 – предохранительная склянка; 4 – глицериновая баня; 5 – ячейка для окисления масла; 6 – контактный термометр
Ход анализа. Собрать установку для определения устойчивости к окислению жиров. Откалибровать манометрическую трубку реометра. Отметить уровень столба жидкости в манометрической трубке при прохождении воздуха со скоростью 8 л/ч.
До начала аэрации нагреть глицериновую баню до 80 оС, поместить в нее ячейку. Соединить ячейку с воздушной системой, начать подачу воздуха со скоростью 8 л/ч.
В химический стаканчик взвесить 50 г исследуемого жира с заранее известным перекисным числом. Нагреть жир на водяной бане до температуры 80 оС и быстро перелить в ячейку для окисления.
В предварительно взвешенную колбу с пришлифованной пробкой отобрать пипеткой из ячейки приблизительно 1 мл жира. После охлаждения (в эксикаторе) колбу взвесить и по разности найти вес отобранной пробы. Определить перекисное число в отобранной пробе любым методом. Отбор проб вести через фиксируемые промежутки времени, периодичность отбора проб зависит от вида жира и величины исходного перекисного числа. Всего из ячейки отобрать 8–10 проб.
Результаты определений представить в виде кривой в координатах перекисное число – время окисления. Продолжительность индукционного периода (в часах) соответствует отрезку по оси абсцисс, ограниченному началом координат и перпендикуляром, опущенным из точки перегиба кривой (рис. 16).
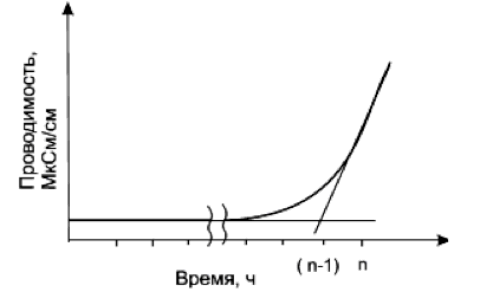
Рис. 16. Кривая зависимости перекисного числа от времени окисления
Автоматизированной версией метода активного кислорода является метод определения окислительной устойчивости на приборе Rancimat 743.

