Одним из первых колориметрических методов, нашедших широкое применение для определения стеринов, является метод Либермана–Бурхарда. Метод сводится к измерению интенсивности зеленовато-голубой окраски раствора стеринов, возникающей после обработки его смесью уксусного ангидрида и серной кислоты (соотношение от 20:1 до 5:1).
Часто используют всевозможные модифицированные реактивы Либермана–Бурхарда. Например, один объем концентрированной серной кислоты смешивают с 20 объемами уксусного ангидрида, охлажденного до температуры ниже 10 оС. Полученную смесь охлаждают в течение 9 минут и добавляют 10 объемов ледяной уксусной кислоты. Данный реактив пригоден для работы в течение одного часа.
Реактив, приготовленный на основе 2%-го раствора сульфата натрия и смеси уксусного ангидрида, уксусной и серной кислот в соотношении 6:3:1 (по объему) имеет срок хранения в холодильнике один месяц.
Схема реакции Либермана–Бурхарда следующая. На первой стадии под действием серной кислоты протекает реакция дегидратации с образованием 3,5 диенов, которые затем в процессе окислительной ди- и тримеризации образуют высокосопряженные производные, растворимые в серной кислоте.
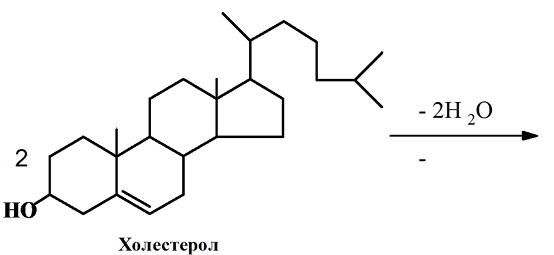
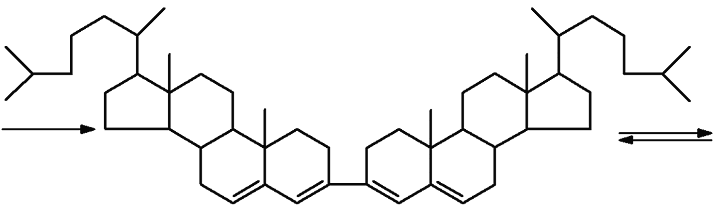
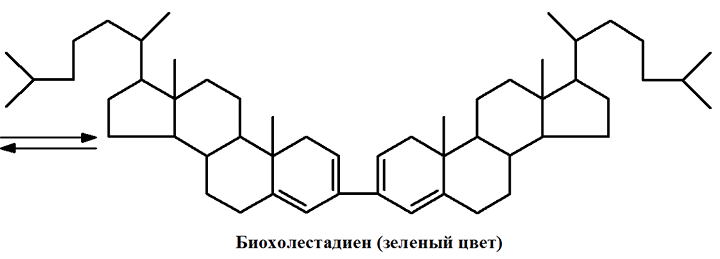
Серная кислота на первом этапе выступает в роли дегидратирующего агента, а в дальнейшем участвует в образовании сульфокислот холестерола, обуславливающих в конечном итоге зеленый цвет раствора. Вышеназванная реакция характерна не только для стеринов и их эфиров, но и для других соединений, например холевой кислоты. Максимум поглощения окрашенных соединений лежит при 610 и 410 нм. Из-за неустойчивости окраски полученных соединений необходимо строго выдерживать время фотометрирования. Кроме того, реакция чувствительна к изменению температуры, поэтому необходимо выдерживать температурный режим реактива после добавления серной кислоты.
Метод Либермана-Бурхарда дает завышенные результаты при определении эфиросвязанных стеринов. Интенсивность окраски эфиров холестерола выше, чем у свободного холестерола, что снижает надежность результатов анализа.
Определение холестерола
Метод Либермана-Бурхарда используется главным образом для количественного определения холестерола.
Ход анализа. В фотометрическую кювету внести пипеткой 4,2 мл реактива Либермана–Бурхарда и медленно по стенке добавить 0,1 мл раствора неомыляемых веществ в хлороформе (содержание свободного холестероола 1–3 мг/мл). Раствор перемешать, термостатировать при 37 оС в течение 30 минут при комнатной температуре. При этом развивается зеленое окрашивание. Полученный раствор зеленого цвета колориметрировать при длине волны 620 нм в кювете с длиной оптического пути 10 мм. В качестве раствора сравнения использовать смесь из 4,2 мл реактива Либермана-Бурхарда и 0,1 мл хлороформа. Концентрацию исследуемой пробы определить по калибровочному графику. Концентрацию холестерола (МС, мг%) рассчитать по формуле:
где СК – концентрация холестерола в исследуемой пробе, найденная по калибровочному графику, мг/мл;
V – объем пробы, взятой на анализ, 0,1 мл;
100 – коэффициент пересчета в проценты.
Построение калибровочного графика. Из стандартного раствора холестерола (1,8 мг/мл) в градуированных пробирках приготовить пять калибровочных растворов по схеме, приведенной в табл. 1.4.8.
Таблица 1.4.8. Схема приготовления калибровочных растворов холестерола
|
Номер калибровочного раствора |
1 |
2 |
3 |
4 |
5 |
|
Стандартный раствор холестерола, мл |
0,05 |
0,10 |
0,15 |
0,20 |
0,25 |
|
Реактив Либермана-Бурхарда, мл |
4,25 |
4,20 |
4,15 |
4,10 |
4,05 |
|
Масса холестерола, мг |
0,09 |
0,18 |
0,27 |
0,36 |
0,45 |
Объем растворов довести до 4,3 мл с помощью реактива Либермана-Бухарда. Содержимое пробирок аккуратно перемешать, термостатировать при температуре 37 оС и через 30 минут колориметрировать при длине волны 620 нм в кювете с длиной оптического пути 10 мм. В качестве раствора сравнения использовать смесь из 4,2 мл реактива Либермана-Бурхарда и 0,1 мл хлороформа.
Определение стеринов
Метод Либермана-Бурхарда применим для количественного определения стеринов, имеющих сопряженные кратные связи в 5 и 7 положениях (эргостерола и 7 – дегидрохолестерола). Интенсивность окраски D5, 7-оксистеринов почти в четыре раза выше интенсивности окраски холестерола, при этом окраска развивается почти мгновенно, тогда как в аналогичных экспериментальных условиях для развития окраски в присутствии холестерола требуется полчаса.
Это свойство используется для количественно определения 7-дегидрохолестерола в присутствии холестерола путем измерения поглощения в области 620 нм через 1,5 минуты и 30 минут с момента начала цветной реакции.
Ход анализа. В пробирку с пришлифованной пробкой внести пипеткой 1 мл экстракта неомыляемых веществ в хлороформе. К экстракту добавить 0,7 мл уксусного ангидрида и 0,1 мл концентрированной серной кислоты. Раствор перемешать, довести объем до 5 мл хлороформом и термостатировать при 37 оС в течение 1,5 минуты для развития окраски. Полученный раствор зеленого цвета колориметрировать при длине волны 620 нм в кювете с длиной оптического пути 10 мм.
В качестве раствора сравнения использовать смесь из 0,7 мл уксусного ангидрида, 0,1 мл концентрированной серной кислоты и 4,2 мл хлороформа. Концентрацию стеринов в исследуемой пробе определить по калибровочному графику.
Построение калибровочного графика. Из стандартного (0,1 мг/мл) эргостерола в хлороформе приготовить калибровочные растворы с заданной концентрацией по схеме, приведенной в табл. 1.4.9.
Таблица 1.4.9. Схема приготовления калибровочных растворов эргостерола
|
Номер калибровочного раствора |
1 |
2 |
3 |
4 |
5 |
|
Калибровочный раствор эргостерола, мл |
0,05 |
0,10 |
0,15 |
0,20 |
0,25 |
|
Хлороформ, мл |
4,15 |
4,10 |
4,05 |
4,00 |
3,95 |
|
Масса эргостерола, мкг |
5,0 |
10,0 |
15,0 |
20,0 |
25,0 |
Довести объемы калибровочных растворов до 5 мл, добавив к каждому по 0,7 мл уксусного ангидрида и 0,1 мл концентрированной серной кислоты. Окраска раствора при 37 оС развивается в течение 1,5 минут. Полученные зеленого цвета калибровочные растворы колориметрировать при длине волны 620 нм в кювете с длиной оптического пути 10 мм. В качестве раствора сравнения использовать смесь из 0,7 мл уксусного ангидрида, 0,1 мл концентрированной серной кислоты и 4,2 мл хлороформа.
|
Необходимые реактивы, посуда, оборудование: §реактив Либермана-Бурхарда, уксусная кислота, уксусный ангидрид, концентрированная серная кислота, хлороформ, холестерол, гексан, стандартный раствор холестерола, стандартный раствор эргостерола; §кюветы с длиной оптического пути 10 мм; пипетки, колбы вместимостью 100 мл, градуирированные пробирки, делительные воронки, круглодонные колбы со шлифом вместимостью 50 мл; §аналитические весы, термостат на 37 ˚С, фотоколориметр, ротационный вакуумный испаритель. |
Реактив Либермана-Бурхарда. В сухую колбу налить 10 мл ледяной уксусной кислоты и 50 мл уксусного ангидрида и охладить полученную смесь до температуры 10 оС. К охлажденной смеси при постоянном перемешивании добавить 10 мл концентрированной серной кислоты. Полученный реактив должен быть бесцветным или слегка желтоватым. Хранить в холодильнике в темной склянке с притертой пробкой.
Стандартный раствор холестерола (1,8 мг/мл, 4,7 ммоль/л). Навеску холестерола 0,18 г растворить в небольшом объеме хлороформа и количественно перенести в мерную колбу вместимостью 100 мл. Довести объем раствора до метки тем же растворителем.
Основной раствор эргостерола (10 мг/мл). Навеску эргостерола в 1 г растворить в небольшом объеме хлороформа и количественно перенести в мерную колбу вместимостью 100 мл. Довести объем раствора до метки тем же растворителем.
Стандартный раствор эргостерола (1 мг/мл). В мерную колбу вместимостью 100 мл отобрать пипеткой 10 мл основного раствора эргостерола и довести объем раствора до метки тем же растворителем.

