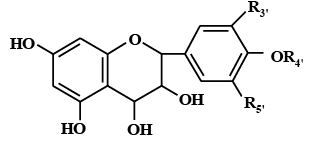
Витаминоподобные вещества – это группа органических соединений, которые обладают высокой биологической активностью и подобны витаминам, но в отличие от истинных витаминов, большинство из них может синтезироваться в необходимых количествах в организме человека в процессе нормального метаболизма. Хотя многие из них получили название витамины, их отнесение к витаминам оспаривается. К этой группе относят: рутин (витамин Р), инозитол (витамин В8), карнитин (витамин Вm, В11), ксантоптерин (витамин В14), липоевая кислота (витамин N), оротовая кислота (витамин В13), пангамовая кислота (витамин Q), метионинметилсульфоний хлорид (витамин U), холин (В4 или Вр).
§ 2.3.1 ФЛАВОНОИДЫ (ВИТАМИН Р)
Витамин Р (от permeability – «проницаемость») – это большая группа соединений полифенольной природы, объединенных общим названием «биофлавоноиды» и обладающих сосудоукрепляющим действием, сходным с действием витамина С. Из-за тесной связи с витамином С биофлавоноиды иногда называют витамином С2. Другие названия витамина Р: рутин, тиоктовая кислота.
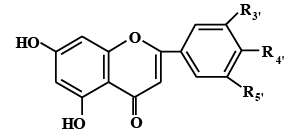
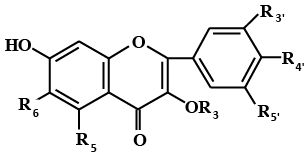
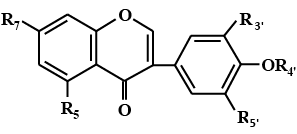
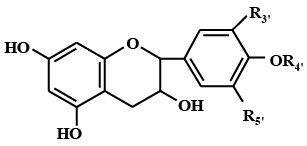
По химической природе биофлавоноиды являются производными хромона или флавона, содержат дифенилпропановый скелет (С6–С3–С6), состоящий из двух ароматических колец, соединенных трехуглеродным фрагментом, который формирует пирановый или пироновый циклы (при наличии кратной связи), и имеют общую формулу
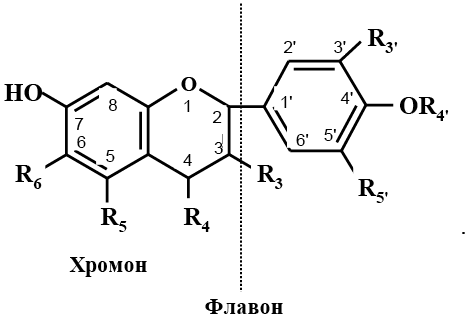
Отличаются они друг от друга по степени окисленности пиранового цикла, а также по числу и положению гидроксильных групп в ароматических кольцах. Наиболее часто в природе встречаются флавоноиды с четырьмя (положения – С5, С 7, С3’, С4’) или пятью (положения – С5, С7, С3’, С4’, С5’) гидроксильными группами в молекуле, максимально количество гидроксилов – семь. По строению флавоноиды напоминают токоферолы, у которых изопреноидная цепь заменена на фенольный радикал, содержащий гидроксильные группы. Антиоксидантные свойства флавоноидов связывают с наличием гидроксильных групп в положениях С3’–С5’, а кислотные свойства – у С7. В зависимости от природы заместителей в цикле различают семь основных групп флавоноидов (табл. 2.3.1).
Таблица 2.3.1. Основные группы флавоноидов, обладающих Р-витаминной активностью, и их агликоны
|
Структурная формула флавоноидов |
Наименование группы флавоноидов и соответствующих агликонов |
|
|
Флавоны: апигенин |
|
|
Флавонолы: |
|
|
Изофлавоны: |
|
|
Флаваноны: Флаванонолы: |
|
|
Флаванолы (катехины): |
|
|
Антоцианидины: |
|
|
Лейкоантоцианидины: |
Распространенность различных групп флавоноидов в природе не одинакова, приблизительно 40% из них приходится на флавонолы, менее распространены флавоны, еще реже встречаются флаваноны. В природе эти группы флавоноидов взаимопревращаемы, поэтому в растительном мире они сопутствуют друг другу (табл. 2.3.2). Многие из этих соединений, имеющих широкий спектр действия (антисептические и антиоксидантные свойства), обладают Р-витаминной активностью в различной степени.
Таблица 2.3.2. Содержание соединений, обладающих Р-витаминной активностью в плодах и овощах
|
Наименование |
Название |
Содержание витамина Р |
|
|
Сырой вес ткани,мг % |
Сухой вес ткани, % |
||
|
Яблоки |
Катехины |
100–150 |
|
|
Лейкоантоцианы |
450–600 |
||
|
Груши |
Лейкоантоцианы |
100–250 |
|
|
Айва |
Лейкоантоцианы |
200–825 |
|
|
Вишня |
Антоцианы |
1300–2500 |
|
|
Черешня темная |
Антоцианы |
225–900 |
|
|
Слива |
Лейкоантоцианы |
0,9 |
|
|
Апельсины |
Гесперидин |
3,07 |
|
|
Лимоны (сок) |
Эриодиктиол |
20 |
|
|
Кверцетин |
22 |
||
|
Гесперидин |
1,4 |
||
|
Гранаты |
Антоцианы |
200–700 |
|
|
Грейпфрут: |
|||
|
целый плод |
Нарингин |
120–360 |
|
|
Сок |
Нарингин |
36,0 |
|
|
Нарингенин |
12,4 |
||
|
Неогесперидин |
1,1 |
||
|
Гесперидин |
1,0 |
||
|
Рябина |
Рутин |
3,5 |
|
|
черноплодная |
Кверцетин |
1,8 |
|
|
Гесперидин |
0,9 |
||
|
Антоцианы |
4000 |
||
|
Облепиха |
Рутин |
2,3 |
|
|
(плоды) |
Гесперидин |
1,3 |
|
|
Шиповник |
Кверцетин |
2,8 |
|
|
(плоды) |
Гесперидин |
1,8 |
|
|
Черная смородина |
Антоцианы |
1000–1500 |
|
|
Лук: |
|||
|
Луковица |
Рутин |
0,95 |
|
|
Шелуха |
Рутин |
2,4 |
|
|
Кверцетин |
1,3 |
||
|
Красный перец |
Рутин |
2,1 |
|
|
(порошок) |
Кверцетин |
0,95 |
|
|
Гесперидин |
1,2 |
||
|
Щавель |
Рутин |
500 |
|
|
Укроп |
Кверцетин |
170 |
|
|
Петрушка (зелень) |
Апигенин |
157 |
|
Флавоноиды – растительные пигменты, которые определяют цвет различных органов растений, в частности цветов и фруктов. Значительно реже они встречаются в низших растениях, насекомых и микроорганизмах. Наиболее богаты флавоноидами молодые цветки и незрелые плоды, локализуются они в клеточном соке растений в растворенном виде. Распределение флавоноидов в мякоти и кожице фруктов и ягод разное, в одних имеет место относительно равномерное распределение, другие содержат их только в кожице, например, яблоки.
Большинство биофлавоноидов находятся в растениях в связанном состоянии с сахарами (флавоноиды гликозиды) и органическими кислотами, реже в свободном (флавоноиды агликоны). Так, например, флавоноиды гликозиды гисперидин и нарингин в качестве агликона содержат соответственно гисперитин и нарингенин, агликон рутина – кверцетин, а антоцианидины являются агликонами антоцианов. Флавоноиды агликоны в виду низкой растворимости расположены в липидных частях растений – жировые капли, восковые слои.
Основными пищевыми источниками флавоноидов являются фрукты, овощи и напитки (чай, соки, вино). Например, содержание флавоноидов в красном вине выше, чем виноградном соке, причиной тому являются микроорганизмы, участвующие в производстве вина. В продуктах питания флавоноиды могут присутствовать в мономерной, димерной и полимерной формах, последние называются танинами.
Биологическая роль флавоноидов заключается в стабилизации межклеточного матрикса соединительной ткани и уменьшении проницаемости капилляров. Непосредственно прочность стенок кровеносных капилляров контролируют гормоны коры надпочечников, роль Р-витаминных веществ заключается в том, что они предохраняют гормон мозгового слоя надпочечников адреналин от окисления, продлевая его действие.
Р-витаминная активность проявляется путем воздействия на некоторые ферментные системы организма, регулирующие сосудистую проницаемость. Например, биофлавоноиды наряду с витамином С инактивируют действие фермента гиалуронидазы, катализирующего распад гетерополисахарида – гиалуроновой кислоты – основного вещества соединительной ткани. Показано ингибирующее действие витамина Р и на аскорбиноксидазу. Витамин предохраняет аскорбиновую кислоту от окисления, способствует восстановлению дегидроаскорбиновой кислоты при участии глутатиона и усвоению витамина С в организме человека.
Антиокислительное действие флавоноидов связывают со способностью блокировать ими каталитическое действие тяжелых металлов, путем связывания их в стабильные комплексы. Считается, что флавоноиды действуют подобно другим липофильным антиоксидантам, имитируя в некоторой степени их действие.
Биофлавоноиды не синтезируются в организме человека и должны поступать с пищей. Дефицит витамина Р может привести к кровоизлияниям на слизистых оболочках, коже, кровоточивости десен из-за ломкости и повышенной проницаемости кровеносных сосудов. Недостаток витамина Р приводит к быстрой утомляемости. Точное значение суточной потребности в витамине Р человека неизвестно, за физиологическую норму принимают 25–50 мг/сут. До настоящего времени не известны случаи гипервитаминоза Р, флавоноиды нетоксичны их избыток легко выводится из организма.
Примером наиболее изученных и значимых для человека биофлавоноидов являются чайные катехины, рутин, квертецин и дигидрокверцетин, которые производят в промышленных масштабах, кроме того выпускают гесперидин и нарингин. Осуществлен химический синтез некоторых биофлавоноидов и их аналогов (рутин, эскулетин).
Рутин или 3-рутинозид кверцетина (3-рамногликозил-3, 5, 7, 3’, 4’-пентаоксифлавон) является флавиновым производным (флавонол). При гидролизе молекулы рутина и отщеплении сахарного остатка образуется агликон – кверцетин, обладающий Р-витаминной активностью.
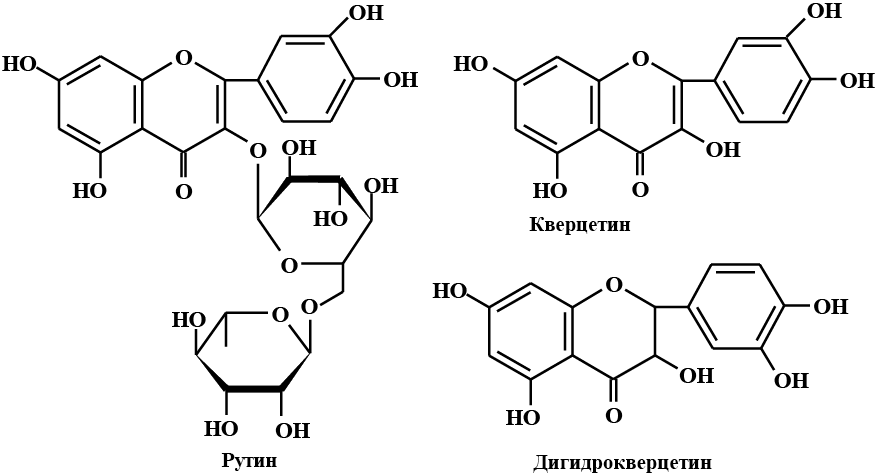
Вместе с витамином С рутин участвует в окислительно-восста-новительных реакциях, стимулирует тканевое дыхание, регулирует проницаемость капиллярных сосудов, повышая их прочность и предупреждая склеротическое повреждение, предохраняет аскорбиновую кислоту от окисления. Рутин и кверцетин являются мощными антиоксидантами, они способны, не только связывать свободные кислородсодержащие радикалы, но и ингибировать процесс их образования за счет связывания металлов переменной валентности. Например, комплекс рутина с ионами железа (II) почти в пять раз активнее самого рутина и выступает в качестве эффективной ловушки супероксидного радикала, с образования которого начинается процесс перекисного окисления липидов биомембран.
Обычно рутин содержится в тех же растительных продуктах, в которых встречается и витамин С. Более всего рутина содержится в, черной смородине, плодах шиповника, цитрусовых, зеленом чае, салате, цветах и листьях гречихи, винограде, капусте, яблоках, сливах. Получают рутин из зеленой массы гречихи и бутонов софоры японской.
Дигидрокверцетин. Другим перспективным природным антиоксидантом является дигидрокверцетин (ДКВ, таксифолина, 3, 3’, 4’, 5, 7–пентагидроксифлаванона), относящийся к группе биофлавоноидов, выделяемый в промышленном масштабе из древесины лиственницы. ДКВ по антиокислительному действию сравним с a-токоферолом, но превосходит его по стабильности. Спектр применения ДКВ достаточно широк, его используют в пищевой, косметической, фармакологической промышленностях. В пищевой промышленности ДКВ и кверцетин применяются в качестве безвредных антиоксидантных добавок для продления сроков хранения (в 2–2,5 раза) липидсодержащих пищевых продуктов (растительные масла, свиной и молочный жир, сухое молоко, пальмовое масло).
МЕТОДЫ ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ
|
Показатель |
Характеристика |
|
|
Рутин |
Кверцетин |
|
|
Формула |
С27Н30О16×3Н2О |
С15Н10О7·3Н2О |
|
Молекулярная масса |
610 |
302 |
|
Температура плавления, оС |
182–192 |
316–317 |
|
Растворимость |
Хорошо растворим в метаноле, изопропаноле, частично в ацетоне |
Растворим в ацетоне, этаноле, метаноле, изопропаноле |
|
Максимум поглощения, lmax, нм |
257, 362 |
256, 375 |
|
Удельный показатель поглощения, , мл/мкг×см |
32,5 |
|
В чистом виде флавоноиды представляют собой кристаллические соединения желтые (флавоны, флавонолы и др.), бесцветные (изофлавоны, катехины, флаваноны, флаванонолы), а также окрашенные в красный или синий цвет (антоцианы) в зависимости от рН среды. В кислой среде антоцианы имеют оттенки красного или розового цвета; в щелочной – синего.
Гликозиды флавоноидов, содержащие более трех остатков сахаров, растворимы в воде, но нерастворимы в диэтиловом эфире и хлороформе. Для флавоноидных гликозидов характерен кислотный или ферментативный гидролиз. Флавонол-3-гликозиды легко гидролизуются при нагревании в 0,1–1%-ных растворах минеральных кислот, а флавон-7-гликозиды гидролизуются лишь при нагревании в течение нескольких часов в 5–10%-ных растворах кислот. Флавоноидные С-гликозиды гидролизуются лишь под действием смеси концентрированной соляной и уксусной кислот. Агликоны флавоноидов растворяются в диэтиловом эфире, ацетоне, спиртах, практически нерастворимы в воде.
Экстракцию флавоноидов обычно проводят спиртами (этиловым, метиловым). Спиртовое извлечение упаривают, а осадок растворяют в горячей воде. Из водной фазы неполярные соединения отмывают хлороформом или четыреххлористым углеродом, а флавоноиды экстрагируют последовательно диэтиловым спиртом (агликоны), этилацетатом и бутанолом (гликозиды).
Для дальнейшего разделения фракций флавоноидов применяют хроматографический метод. Они хорошо поддаются хроматографическому разделению и характеризуются различиями в окраске в видимом и ультрафиолетовом свете. Для проявления флавоноидов после разделения наиболее часто применяют пары аммиака, растворы щелочи в метаноле, водные растворы хлористого алюминия, раствор пятихлористой сурьмы в четыреххлористом углероде, раствор боргидрида калия или натрия в изопропиловом спирте с последующим опрыскиванием спиртовым раствором хлористого алюминия и нагреванием при 120 °С. Идентификацию флавоноидов ведут с использованием УФ-, ИК-, ЯМР-спектроскопии.
К наиболее распространенным методами количественного анализа биофлавоноидов относятся хроматографический, спектрофотометрический методы и денситометрия с использованием хроматографии. Фотоколориметрические методы определения флавоноидов основаны на цветных реакциях с солями металлов (алюминия, циркония, титана, хрома, сурьмы) и лимонно–борным реактивом.
Холин (витамин В4 или Вр) – это гидроксид-2-гидроксиэтил- (триметил) аммония, его название происходит от греческого слова kholy – желчь.
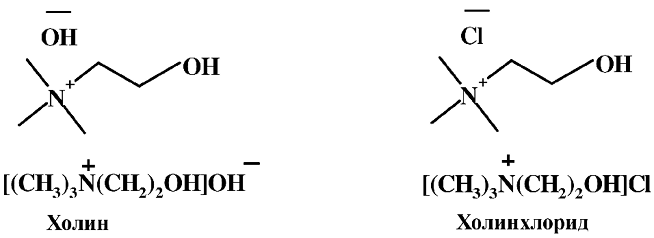
Он хорошо растворим в воде, является сильным основанием, образует соли с кислотами, наиболее распространенная соль – холинхлорид, которая широко применяется в фармакологии. Холин входит в состав важнейших фосфолипидов – лецитинов и сфингомиелинов, являющихся липидными компонентами клеточных мембран, а в нервных клетках составляют половину чувствительного миелинового слоя.
Не все млекопитающие обладают способностью синтезировать витамин В4, однако человек, некоторые животные и микроорганизмы способны к выработке холина. Синтез холина у млекопитающих протекает в печени ступенчато из фосфатидилсерина, в качестве донора метильных групп выступает метионин. Дополнительное количество холина синтезируется микрофлорой кишечника человека при участии аминокислот: метионина, серина, и витаминов В12 и В9, снижая долю эндогенного холина до одной пятой от суточной потребности в нем. Строго говоря, холин не является витамином, поскольку синтезируется в организме и используется как пластическое вещество при построении клеточных мембран. Однако в силу ограниченности синтеза метильных групп, холин относят к псевдовитаминам и его основная масса должна поступать с пищей.
Богатыми источниками холина являются животные, растительные ткани, продуцируют холин и некоторые микроорганизмы. В качестве важных пищевых источников выступают яйца, печень, соя, все виды капусты, арахис, мясо, рыба (табл.2.3.4).
Таблица 2.3.4. Содержание холина в продуктах питания
|
Наименование продукта |
Массовая доля, мг/г |
|
Желток яйца куриного |
1713 |
|
Печень свиная |
552 |
|
Яйцо куриное |
504 |
|
Пророщенная пшеница |
406 |
|
Почки бычьи |
333 |
|
Пророщенный рис |
300 |
|
Соя (бобы) |
300 |
|
Почки свиные |
256 |
|
Капуста |
251 |
|
Шпинат |
238 |
|
Чечевица |
223 |
|
Треска |
200 |
|
Лосось |
181 |
|
Овсянка |
156 |
|
Ячневая крупа |
139 |
|
Сельдь |
127 |
|
Помидоры |
106 |
|
Мясо |
75–100 |
|
Картофель |
66 |
|
Почки бычьи |
63 |
|
Хлеб белый |
62,5 |
|
Хлеб черный |
56,5 |
|
Капуста |
23 |
|
Шпинат |
22 |
|
Молоко |
14,7 |
|
Апельсиновый сок |
12 |
Растительные продукты содержат меньше холина, чем продукты животного происхождения, но хорошими источниками среди них являются зеленые листья и бобовые. Содержится холин в зародышевой части злаков, в плодах боярышника, капусте, шпинате, сое. Потери холина при варке растительных продуктов колеблются в диапазоне 10–40%, при варке мяса и печени они составляют 18%, при выпекании потери незначительны.
Основной метаболической формой холина является лецитин, он способствует липидному обмену в печени, то есть обладает гепатопротекторными свойствами. Холин препятствует ожирению печени, так как при недостатке витамина В4 замедляется процесс выделения из нее жирных кислот. Кроме, того, из холина в организме синтезируется ацетилхолин – важнейший нейромедиатор, принимающий участие в передаче нервных импульсов, отсюда роль холина в улучшении памяти. Холин является метилирующим агентом и принимает участие в биохимических реакциях метилирования, а именно в синтезе незаменимой аминокислоты – метионина.
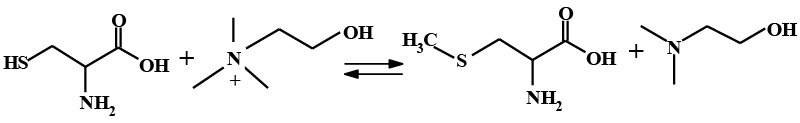
Реакция метилирования гомоцистеина под действием холина обратимая и при недостатке в организме холина он образуется из незаменимой аминокислоты – метионина. Тем не менее, биологический синтез не может полностью покрыть потребность холина в организме. Учитывая зависимость образования эндогенного холина от обеспеченности метионином и витаминами (В9, B12), очевидно, что холиновая недостаточность у человека возможна, как развитие вторичной недостаточности, связанной в первую очередь с недостаточностью белка. Дефицит холина в сочетании с дефицитом белка, может вызвать жировое перерождение печени и ее цирроз. Потребность в холине для человека составляет 1,5–4 г/сут., при сильных стрессах до 6 г/сут.
Холин, его соли и эфиры применяется в пищевой промышленности в качестве эмульгатора и зарегистрированы как пищевая добавка Е1001, в составе лецитина как антиокислитель – Е322.
1. Инозитол (В8, мио-инозит, мезо-инозит) – циклогексан-1, 2, 3, 4, 5, 6-гексола – цис-1, 2, 3, 5-транс-4, 6-циклогексанол, обладающий биологической активностью. Температура плавления инозитола 225 °С. Его кристаллы хорошо растворимы в воде (10–14 г/100 мл). Инозитол стоек к воздействию кислот и щелочей.
Инозитол по своей пространственной структуре может существовать в виде восьми цис-, транс-стереоизомеров, семь из которых являются оптически неактивными (мезо-форма), а один существует в виде двух оптических изомеров (D и L) и одного рацемата. Только один из этих изомеров обладает витаминной активностью и называется мио-инозит.
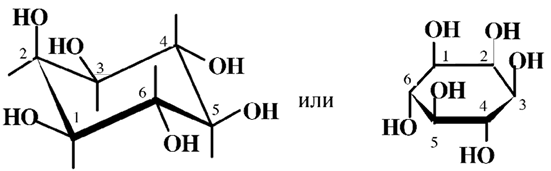
2. Циклогексановое кольцо мио-инозита имеет геометрическую форму кресла, в котором гидроксильные группы при С1–С3, С5, расположены по одну сторону кольца и обозначаются, как цис-гидроксилы, остальные – по другую сторону и обозначаются транс-гидроксилы. Метаболически активной формой мио-инозита является фосфодитилинозитол. Витаминную активность проявляют соли инозитфосфорной кислоты – фитины, которые обладают одинаковым биологическим эффектом с мио-инозитом. К природным инозитам относятся только мио-инозит и D-инозит, L-ионозит.
Инозитол – универсальный компонент большинства живых организмов находится, как в свободном, так и в связанном состоянии, в виде фосфорных эфиров, фосфолипидов и фосфопротеинов. Инозитол синтезируется млекопитающими из глюкозы в печени, путем циклизации глюкозо-6-фосфата до инозитол-1-фосфата с дальнейшим дефосфорилированием во многих тканях и органах (сердце, печени, почках).
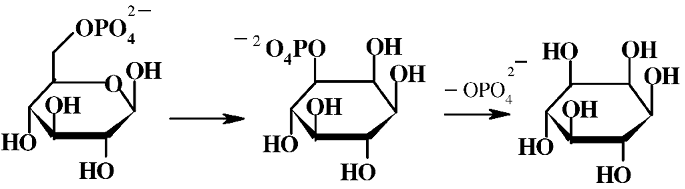
С кровотоком он попадает во все клетки, которые не могут сами его продуцировать. Дополнительным источником инозитола является его синтез в кишечнике. В высоких концентрациях инозитол обнаружен в клетках мозга, где он накапливается в биомембранах, он необходим для функционирования и роста нервных клеток. Много инозитола в хрусталике, задней стенки глаза и слезной жидкости, поэтому дефицит этого витамина может привести к различным глазным заболеваниям.
3. В продуктах питания инозитол присутствует в трех формах: инозитол, фитиновая кислота и инозитол содержащие фосфолипиды. Богатыми источниками инозитола являются семена растений, солод, а также цитрусовые, капуста, морковь, свекла, картофель, томаты, клубника, в которых он присутствует в основном в виде фитиновой кислоты, способной переводить кальций, магний, железо и цинк в неусваиваемые соли, что осложняет процесс всасывания (табл.2.3.5). Кроме того, для усвоения фитина из растительной пищи требуется большое количество фермента фитазы, содержащегося в желудочном соке и вырабатываемого в кишечнике, поэтому нарушение процессов пищеварения может привести к дефициту инозитола. В продуктах животного происхождения инозитол находится преимущественно в виде фосфолипидов.
4. Биологическую роль инозитола связывают с обменом фосфолипидов и образованием инозитол-1, 4, 5-трифосфата – активного вторичного посредника внутриклеточных сигналов. Инозитол обладает липотропным действием, понижает уровень холестерола в крови, препятствует отвердеванию артерий, восстанавливает структуру нервной ткани, нормализует сон, оказывает стимулирующее действие на моторную функцию пищеварительного аппарата. В медицинской практике инозитол применяется при болезнях печени, фитин как источник фосфора при нервных болезнях, стимуляции кроветворения.
Таблица 2.3.5. Содержание инозитола в продуктах питания, мг/г
|
Наименование продукта |
Массовая доля, мг% |
|
Спаржа |
0,29–0,68 |
|
Белые бобы |
2,83–4,40 |
|
Брокколи |
0,11–0,30 |
|
Капуста |
0,18–0,70 |
|
Морковь |
0,52 |
|
Цветная капуста |
0,15–0,18 |
|
Форель |
0,11 |
|
Горох |
1,16–2,35 |
|
Шпинат |
0,06–0,25 |
|
Томаты |
0,34–0,41 |
|
Молоко |
0,04 |
|
Яйцо |
0,09 |
|
Яичный желток |
0,34 |
|
Яблоки |
0,10–0,24 |
|
Виноград |
0,07–0,16 |
|
Грейпфрут |
1,17–1,99 |
|
Апельсины |
3,07 |
|
Груша |
0,46–0,73 |
|
Рис |
0,15–0,30 |
|
Пшеница |
1,42–11,5 |
|
Говядина |
0,09–0,37 |
|
Мясо куриное |
0,30–0,39 |
|
Свинина |
0,14–0,42 |
|
Печень говяжья |
0,64 |
|
Печень куриная |
1,31 |
|
Тунец |
0,11–0,15 |
Суточная потребность инозитола – 1–1,5 г/сут., примерно ¾ суточной потребности вырабатывается организмом из глюкозы, остальное количество поступает с пищей. Неправильное питание ведет в большинстве случаев к нарушению микрофлоры в кишечнике и тем самым к дефициту инозитола.
Убихиноны (кофермент Q, KoQn). Название происходит от латинского слова ubique – везде, повсюду и хинон. В 1978 году за разработку теории действия коэнзима Q10 – незаменимого клеточного компонента, принимающего участие в синтезе АТФ, американский ученый П. Митчел получил Нобелевскую премию. По строению это производные 2, 3-диметокси-5-метил-1, 4-бензохинон с изопреновой цепью в положении С6:
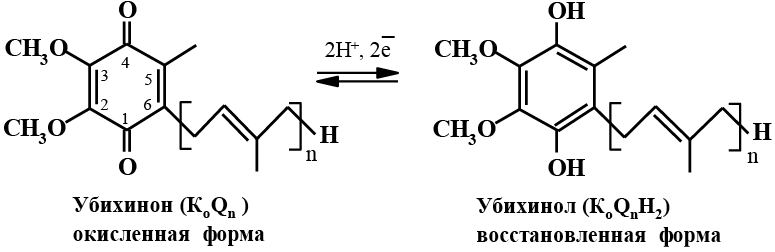
Они различаются между собой числом изопреновых звеньев от 6 до 15. Чаще всего природные убихиноны содержат от шести до десяти изопреновых фрагментов (Q6–Q10). При n=1–6 убихиноны представляют собой маслообразные вещества красного цвета, при n=7–15 это желтые или желто-оранжевые кристаллы, которые не растворимы в воде, но растворимы в органических растворителях. В природе убихиноны встречаются во всех организмах – млекопитающих, грибах, бактериях, простейших, насекомых. В небольших количествах присутствуют в митохондриях растений. Выделенные из бактерий убихиноны содержат от шести до девяти изопреновых звеньев, высшие растения – девять, млекопитающие – от девяти до десяти. В организме человека присутствует кофермент Q10.
Убихиноны способны к обратимым окислительно-восстанови-тельным превращениям и локализованы в цитоплазматических мембранах митохондрий. Основная их функция убихинонов – коферментная и связана с переносом электронов и протонов при дыхании и окислительном фосфорилировании. Поскольку кофермент Q10 принимает участие в обеспечении энергией клеток, то у человека самое большое количество кофермента Q10 сосредоточено в митохондриях клеток наиболее энергопотребляющих органов – сердце, печень, поджелудочная железа.
Другой важной функцией убихинонов является антиоксидантная. Они, наряду с a-токоферолом, b-каротином и селеном, являются мощными антиоксидантами, и расходуются в первую очередь. В отличие от вышеназванных антиоксидантов убихиноны синтезируются в самом организме человека и обладают способностью постоянно восстанавливать свою антиоксидантную активность, переходя из окисленной формы (убихинол) в восстановленную (убихинон). По некоторым данным они играет важную роль в защите от окисления липопротеинов низкой плотности. В клетках сердца Q10, снижая уровень свободных радикалов, замедляет развитие атеросклероза.
В клетках животных убихиноны синтезируются в достаточных количествах из соответствующих предшественников. Считается, что синтез убихинонов начинается в эндоплазматическом ретикулуме и заканчивается в комплексе Гольджи, откуда они распределяются по всем органеллам. Формирование изопреноидной цепи имеет общие этапы с синтезом холестерола, а бензольная часть образуется из тирозина. Поэтому синтез убихинонов может лимитировать наличие тирозина и его предшественника незаменимой аминокислоты – фенилаланина.
С возрастом содержание убихинонов в тканях человека снижается, 75%-ный дефицит убихинонов вызывает гибель клеток, а 25% снижения уровня заметно сказывается на работе не только внутренних органов (сердце, почек), но и нервной, и эндокринной систем. Дефицит кофермента Q10 приводит к таким заболеваниям как сердечная недостаточность, потеря иммунитета, мышечная дистрофия, хронические поражения печени.
Несмотря на то, что в желудке всасывается только 2–3% экзогенного Q10, он широко используется при лечении атеросклероза. Сведения о пищевых источниках убихинонов в литературе неоднозначны (табл. 2.3.6). Но так как убихиноны присутствуют во всех мембранах митохондрий, то можно предположить, что ими богаты многие пищевые продукты особенно сердце и мышечная ткань.
Таблица 2.3.6. Содержание кофермента Q10 в продуктах питания
|
Наименование продукта |
Массовая доля, мг% |
|
Свиное сердце |
20,30 |
|
Бычье сердце |
4,10 |
|
Сельдь |
2,70 |
|
Говяжья печень |
1,90 |
|
Куриные ножки |
1,70 |
|
Форель |
1,10 |
|
Баранья нога |
0,29 |
|
Шпинат |
0,23 |
|
Апельсины |
0,22 |
|
Цветная капуста |
0,06 |
Липоевая кислота (тиоктовая кислота, витамин N) по своему строению является тиопроизводным валериановой кислоты, легко подвергается окислительно-восстановительным превращениям:
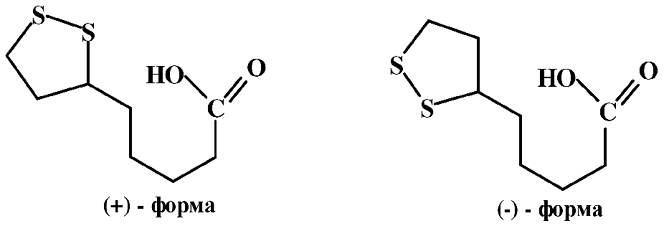
Липоевая кислота существует в виде двух стереоизомеров, из которых правовращающаяся обладает биологической активностью. Природная, правовращающаяся форма липоевой кислоты плавится при 47,5 °С, [a]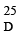 +104, а синтетически полученная представляет собой рацемат D, L– с температурой плавления 60–61°С.
+104, а синтетически полученная представляет собой рацемат D, L– с температурой плавления 60–61°С.
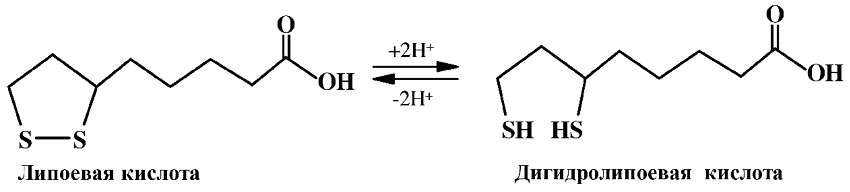
Биологическую активность липоевая кислота проявляет в качестве простетической группы дегидрогеназ, выполняя роль переносчика электронов и ацильных групп. Липоевая кислота и ее амид, связываются с ферментом через аминогруппу лизина, при этом дисульфидный мостик выполняет функцию окислительно-восстановительного центра.
Кроме того, липоевая кислота – мощный антиоксидант, и наряду с аскорбиновой кислотой она выступает в качестве основного водорастворимого антиоксиданта клетки, предохраняет от перекисного окисления ЛПНП. Совместное действие липоевой кислоты с витаминами Е и С предотвращает развитие атеросклероза.
Липоевая кислота является условно незаменимой для человека, в организме человека она может синтезироваться лишь в тех количествах, которые способны предотвратить ее дефицит. Суточная потребность в липоевой кислоте ориентировочно – 1–2 мг. Она широко распространена в природе (растения, микроорганизмы) в основном в связанной форме, но в невысоких концентрациях, наибольшее количество ее находят в митохондриях и хлоропластах, основные пищевые источники – дрожжи, мясные продукты, молоко.
Витамин N играет важную роль в профилактике рака, ингибирует деградацию инсулина, отсюда ее применение при лечении сахарного диабета. Основной терапевтической формой является липоамид, в качестве лекарственного средства выпускают и липоамид, и липоевую кислоту, применяя их в комплексной терапии коронарного атеросклероза, заболеваний печени и различных интоксикаций.
L-Карнитин (левокарнитин, витамин В11, ВТ) по своему строению – аминокислота g-амино-b-гидроксибутановая кислота. Название происходит от латинского слова сarnis – мясо. Карнитин существует в двух стереоизомерных формах: L-карнитин и D-карнитин, биологическую активность проявляет только L-карнитин.
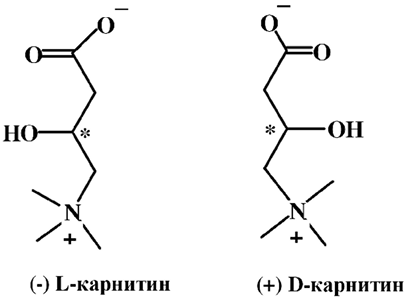
D-форма не оказывает влияния на организм, но выступает конкурентным антагонистом L-карнитина (левокарнитина). Левокарнитин представляет собой белый кристаллический порошок, легко растворимый в воде, горячем спирте и практически не растворимый в органических растворителях. Встречается карнитин в мышечной ткани животных, в растениях, микроорганизмах. Высшие животные, в том числе и человек, синтезируют левокарнитин из L-лизина при участии витаминов С, В3, В6, В9, В12, железа, метионина.
Карнитин один из основных источников получения энергии для мышечных тканей. Его функция в организме связана с транспортом длинноцепочечных жирных кислот, в процессе окисления которых выделяется метаболическая энергия. При этом L-карнитин выступает в качестве кофермента, участвующего в транспорте жирных кислот через мембраны из цитоплазмы в митохондрии. Он взаимодействует с коферментой формой жирной кислотой, формируя цвиттер-ион – производное, имеющее высокое сродство к липидному слою клеточных мембран. Это обеспечивает легкий транспорт жирной кислоты через митохондриальную мембрану, а затем освобождение кислоты в результате гидролиза:
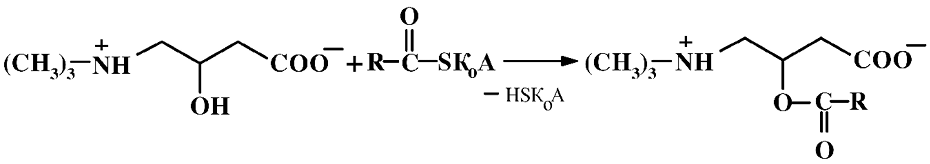
Таким образом, карнитин интенсифицирует поступление в клетку жирных кислот и образование АТФ, предотвращая отложение жира в организме, прежде всего в сердце, печени, скелетной мускулатуре. Карнитин регулирует соотношение кофермента А и ацил-кофермента А, обеспечивая работу цикла трикарбоновых кислот и оптимизацию энергетического метаболизма.
L-карнитин синтезируется в печени и почках, из которых транспортируется в другие ткани и органы. Уровень L-карнитина является постоянным, он не накапливается в организме, излишки эффективно выводятся. Карнитин синтезируется в организме человека в больших количествах (около 25% от суточной потребности), поступает с пищей (75%), поэтому убедительных доказательств в необходимости его дополнительного введения с пищей нет, хотя общеизвестно применение мясных бульонов, богатых экстрактивными веществами, для стимулирования процессов обмена у ослабленных больных. Бульон практически не содержит белков, жиров и углеводов, зато богат экстрактивными веществами, в том числе и карнитином, который повышает секрецию и ферментативную активность пищеварительных соков желудочного и кишечного, улучшает усвоение пищи.
Рекомендуемая норма суточного потребления карнитина составляет, мг: для взрослых – 300, для детей до года – 10–15 , с года до трех лет – 30–50 , с четырех до шести лет – 60–90, с семи до восемнадцати лет – 100–300. Эти нормы потребления в несколько раз возрастают при наличии умственных, физических или эмоциональных перегрузок.
Больше всего карнитина содержится в мясе, птице, морепродуктах, молочных продуктах. В зернах, фруктах и овощах карнитин присутствует в небольших количества (табл. 2.3.7).
Таблица 2.3.7. Содержание карнитина в продуктах питания
|
Наименование продукта |
Массовая доля, мкг% |
|
Говядина |
59,8–67,4 |
|
Куриное мясо |
4,6–9,1 |
|
Сердце |
19,3 |
|
Коровье молоко |
0,53–3,91 |
|
Говяжья печень |
2,6 |
|
Говяжьи почки |
1,8 |
|
Казеин |
1,5 |
|
Авокадо |
1,25 |
|
Пшеница |
0,35–1,22 |
|
Арахис |
0,76 |
|
Хлеб |
0,24 |
|
Цветная капуста |
0,13 |
Левокарнитин называют «витамином роста», так как он нормализует липидный и белковый обмен, снижает содержание жира в мышцах и усиливает обмен, ускоряя процесс наращивания мышечной массы. Способность карнитина оказывать влияние на энергетические процессы, снижать утомляемость, повышать физическую выносливость, уменьшать боль в мышцах после тренировок, снижая уровень молочной кислоты в мышцах, используют в спортивной медицине. L-карнитин применяют в педиатрии для повышения устойчивости к психоэмоциональным нагрузкам, при нервном и физическом истощении, особенно пожилых людей, и в послеоперационной период восстановления. Многие производители детского питания используют его в приготовлении адаптированных смесей на молочной и соевой основе.
В настоящее время существует несколько технологий промышленного синтеза L-карнитина: химический синтез, экстракция из натурального сырья (из побочных продуктов мясного животноводства) и микробиологический синтез (производство микроорганизмами натурального 100%-го L-карнитина).
§ 2.3.7 МЕТИОНИНМЕТИЛСУЛЬФОНИЙ ХЛОРИД
Метионинметилсульфоний хлорид (S-метилметионин, витамин U). Название витамин U происходит от латинского слова ulcus – язва. Основу его структуры составляет аминокислота метионин, сульфидная группа которой переведена в сульфониевую:
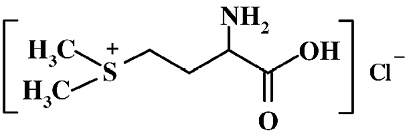
В природе метионинметилсульфоний хлорид синтезируется многими растениями, наиболее богаты им спаржа, капуста, сельдерей, томаты, картофель, листья чая (табл. 2.3.8), основным пищевым источником является сок сырых овощей, присутствует в парном молоке и печени.
Таблица 2.3.8. Содержание витамина U в продуктах питания (в пересчете на сухой вес)
|
Наименование продукта |
Массовая доля, мг% |
|
Спаржа, побеги |
100–160 |
|
Капуста белокочанная, листья |
84,6 |
|
Томаты незрелые, зеленые |
46,7–48,2 |
|
Капуста белокочанная, кочерыжка |
35,9 |
|
Томаты зрелые, красные |
18,7–47,5 |
|
Сельдерей, стебель |
17,4 |
|
Свекла столовая |
14,6 |
|
Петрушка зелень |
6,4 |
|
Зеленый чай |
4,6 |
|
Черный чай |
– |
Метионинметилсульфоний хлорид хорошо растворим в воде, разрушается при нагревании до 100 оС в нейтральной и особенно в щелочной среде, устойчив в кислой. Потери витамина при технологической обработке продуктов зависят от продолжительности и интенсивности теплового воздействия. Потери при бланшировании составляют 3–4%, при продолжительном тушении происходит полное разрушение витамина.
Метионинметилсульфоний хлорид является активной формой незаменимой аминокислоты метионина, выступает донором метильных групп в различных биохимических реакциях, главным образом в реакциях метилирования с образование фрагментов: CH3OR, CH3NHR, CH3C при биосинтезе холина, креатина, адреналина.
Помимо метилметионинсульфония-хлорида были выделены бромид-, йодид- и сульфат-формы, они находят применение в качестве противоязвенных средств. Предположительно витамин U улучшает обмен тиамина и холина, в частности в слизистой оболочке желудка, и повышает ее резистентность к возникновению язв. Витамин U повышает кислотность желудочного сока, улучшает моторную функцию тонкого и толстого кишечника, а также желчного пузыря. Он обладает липолитическим, антиаллергическим и антисклеротическим действием.
Организм человека не способен синтезировать витамин U и получает его в основном с растительной пищей. Незаменимость S-метилметиона не доказана, в реакциях с участием витамина при его нехватке в человеческом организме он замещается другими веществами. Суточная потребность составляет приблизительно 500 мг.
Пангамовая кислота (витамин В15, 6-О-N, N-диметилглицил-D-глюконовая кислота). Название происходит от греческих слов pan – «всюду», gamy – «семя». По своей структуре она является пентагидроксизамещенной гексановой кислотой, в которой гидроксильная группа при С-6 этерифицирована N, N-диметиламиноуксусной кислотой.
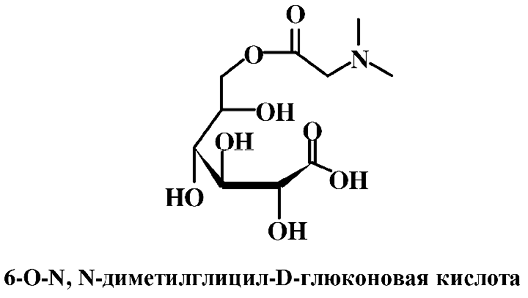
Пангамовая кислота впервые выделена Г. Кребсом из ядер косточек абрикосов. Она широко представлена в семенах растений – кунжута, тыквы, коричневого риса, и семенах других злаковых растений, ядрах косточковых плодов, присутствует в пивных дрожжах и печени.
Физиологическое действие пангамовой кислоты заключается в активировании кислородного обмена в клетках различных тканей организма, кроме того она выступает донором метильных групп в реакциях метилирования. Пангамовая кислота обладает липотропными свойствами и необходима для нормализации липидного обмена, снижает риск заболеваний печени. Она принимает участие в синтезе креатинфосфата, который играет важную роль в нормализации функциональной способности мышц и улучшении энергетических процессов в целом. По этой причине дефицит пангамовой кислоты вызывает заболевания сердечно-сосудистой системы, повышение утомляемости, преждевременное старение, нервные расстройства. Кроме того, пангамовая кислота выводит токсины из организма, понижает уровень сывороточного холестерола, снижает стремление к алкоголю.
В медицинской практике пангамовую кислоту применяют в виде кальциевой соли для комплексной терапии и профилактики атеросклероза, гепатита, цирроза печени и алкогольной интоксикации. Получают пангамовую кислоту химическим методом окисления D-глюкозы до D-глюконовой кислоты, затем этерифицируют в ней первичную гидроксильную группу N, N-диметилглицином и образующийся эфир переводят в кальциевую соль:
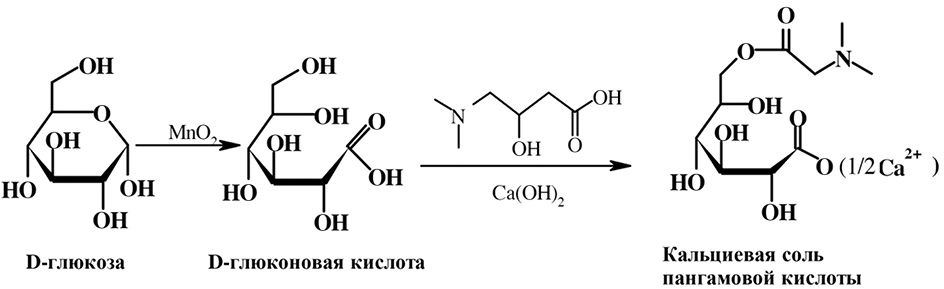
Суточная доза пангамовой кислоты для взрослых составляет 50–150 мг/сут., для детей от 3 до 14 лет – 100–300 мг/сут.