Неомыляемыми веществами называются вещества, присутствующие в жирах в растворенном состоянии, извлекаемые петролейным или диэтиловым эфирами после омыления жиров спиртовыми растворами щелочей и не улетучивающиеся при сушке. К ним относятся стеролы, фосфолипиды, свободные жирные кислоты, некоторые пигменты, обусловливающие окраску жиров, вещества, определяющие вкус и запах жиров, углеводороды, свободные высшие алифатические спирты, липовитамины, воски, гликолипиды и др. Ориентировочные данные по содержанию неомыляемых веществ в некоторых жирах приведены в табл. 1.4.1.
Таблица 1.4.1. Массовая доля неомыляемых веществ в растительных жирах
|
Наименование жира |
Массовая доля неомыляемых веществ, % |
Наименование жира |
Массовая доля неомыляемых веществ, % |
|
Арахисовое |
0,2–0,9 |
Пальмоядровое |
0,2–1,0 |
|
Горчичное |
0,7–1,4 |
Подсолнечное |
0,3–1,5 |
|
Какао |
0,2–1,1 |
Рапсовое |
0,6–1,4 |
|
Касторовое |
0,3–1,0 |
Сафлоровое |
0,3–1,4 |
|
Кокосовое |
0,2–0,6 |
Соевое |
0,4–1,6 |
|
Конопляное |
0,8–1,0 |
Хлопковое |
0,4–1,5 |
|
Кукурузное |
0,8–2,5 |
Бараний |
до 1,0 |
|
Кунжутное |
0,9–2,5 |
Говяжий |
до 1,0 |
|
Льняное |
0,5–1,9 |
Свиной |
до 0,8 |
|
Оливковое |
0,5–1,8 |
Тресковый |
3,3–4,7 |
|
Пальмовое |
0,2–1,0 |
Китовый |
1,4–1,9 |
Неомыляемые вещества оказывают существенное влияние на пищевую ценность жиров. Одни из них являются источником эссенциальных нутриентов, другие, являясь токсичными веществами, делают жиры, не пригодными для пищевых целей.
Липиды на основе сфингозина, или сфинголипиды, – липиды мембранного происхождения, которые построены на основе длинноцепочечного аминоспирта сфингозина и его аналогов, например сфингонина и фитосфингонина.
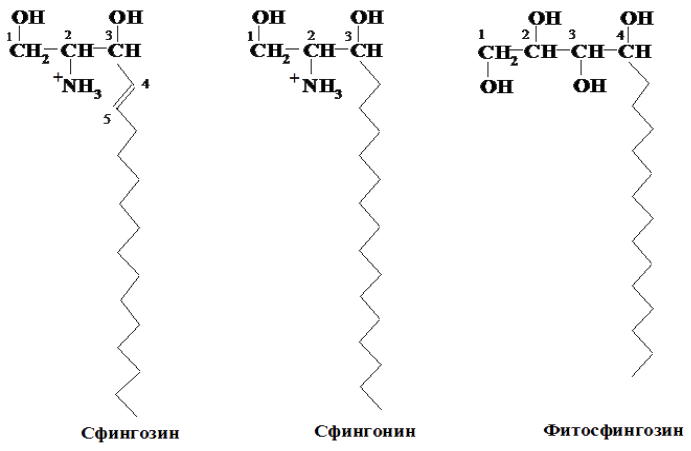
Сфингозин и сфингонин являются диолами с гидроксильными группами при С-1 и С-3 и аминогруппой при С-2. Животный сфингозин имеет кратную связь трансконфигурации между С-4 и С-5. Фитосфингозин имеет четыре гидроксильные группы.
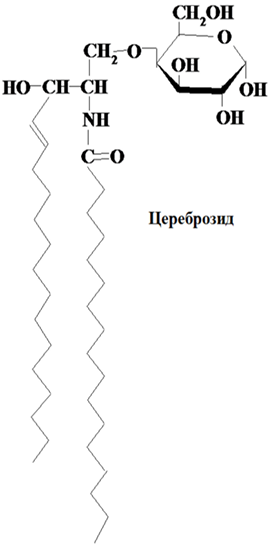
В сфинголипидах имеется амидная связь с жирными кислотами, то есть жирная кислота взаимодействует со сфингозинами по аминогруппе, остальные спиртовые группы обычно свободны. Наиболее богаты сфинголипидами нервные ткани и особенно мозг. Из сфинголипидов наиболее распространенные цереброзиды – гликосфинголипиды, которые состоят из сфингозина, жирной кислоты и моносахарида галактозы.
Цереброзиды входят в состав нервной ткани, мозга и многих важных органов – почек, селезенки, надпочечной железы. Не исключено, что они входят в состав всех животных клеток.
Цереброзиды набухают в воде, давая гели, а в разбавленных растворах образуют коллоидные растворы (золи). Цереброзиды нерастворимы в воде, этиловом спирте и других органических растворителях, при повышенных температурах их растворимость увеличивается.
Все сфинголипиды имеют амфифильную структуру – полярную гидрофильную головку и длинную углеводородную цепь – гидрофобную часть молекулы.
Фосфофолипиды – главные компоненты биологических мембран. По строению они представляют собой эфиры фосфорных кислот и двух многоатомных спиртов – глицерина либо сфингозина. Фосфолипиды входят в состав каждой клетки животных и растений, но больше их в мозговых и нервных тканях, яичном желтке, печени, почках. В растениях присутствуют в семенах, обычно в связанном состоянии с белками. Среди масличных культур наиболее богаты фосфолипидами семена хлопка, сои, подсолнечника. В пищевом рапсовом масле содержание фосфолипидов составляет 0,04–0,09% (на Р2О5), но значительную долю фосфатидов составляют трудногидратируемые и негидратируемые фосфатидилсерины, полифосфоглицериды и фосфатидные кислоты (табл. 1.4.2).
Таблица 1.4.2. Фракционный состав фосфолипидов семян безэруковых сортов рапса
|
Группы фосфолипидов |
Массовая доля фосфора в семенах рапса, % |
||
|
«Зефир» |
«Сюрприз» |
«Кубанский» |
|
|
Фосфатидилинозитолы |
10,0 |
2,0 |
3,0 |
|
Фосфатидилхолины |
30,0 |
20,0 |
23,0 |
|
Фосфатидилсерины |
19,0 |
21,0 |
20,0 |
|
Фосфатидилэтаноламины |
10,0 |
13,0 |
10,0 |
|
Полифосфатидные кислоты |
2,0 |
5,0 |
7,0 |
|
Дифосфатидилдиглицерины |
5,0 |
10,0 |
11,0 |
|
Фосфатидные кислоты |
0 |
15,0 |
15,0 |
Содержание фосфолипидов в растительных маслах изменяется в широких пределах в зависимости от их содержания в семенах, способов и технологических режимов получения масла из семян и степени его очистки. При хранении масел фосфолипиды выпадают в осадок, ускоряя тем самым порчу готового продукта, по этой причине фосфолипиды удаляют из растительных масел в процессе рафинации (табл. 1.4.3).
Таблица 1.4.3. Содержание фосфолипидов в растительных маслах в пересчете на лецитин, %
|
Вид масла |
Наименование растительного масла |
|||
|
Соевое |
Подсолнечное |
Льняное |
Хлопковое |
|
|
Нерафинированное |
3,00–3,50 |
0,90–1,15 |
1,00–1,80 |
1,21 |
|
Очищенное |
0,02–0,25 |
следы – 0,24 |
0,07–0,60 |
0,20–0,30 |
|
Щелочная |
следы – 0,02 |
следы |
до 0,02 |
0,01–0,20 |
Данные о содержании фосфолипидов в некоторых продуктах животного происхождения приведены в табл. 1.4.4.
Таблица 1.4.4. Содержание фосфолипидов в продуктах животного происхождения
|
Наименование продукта |
Массовая доля фосфолипидов, % |
|
Печень (говяжья, свиная) |
3,3–3,6 |
|
Мышечная ткань |
0,7–0,98 |
|
Жировая ткань |
1,2–1,4 |
|
Мясо кролика |
1,5–2,5 |
|
Говяжий топленый жир |
1,25 |
|
Свиной топленый жир |
0,33 |
|
Селезенка говяжья |
2,2–-2,3 |
|
Мозг быка |
6,0–6,1 |
|
Масло сливочное |
0,3–0,4 |
|
Пахта пастеризованная |
0,2 |
|
Яйцо куриное |
3,4 |
|
Яйцо перепелиное |
5,4 |
§ 1.4.3. Классификация фосфолипидов
Фосфолипиды делят на содержащие в своей структуре азот (моно-, диаминофосфолипиды) и не содержащие (фосфатидокислоты).
Фосфатидокислоты
Фосфолипиды, не содержащие атома азота, называют фосфатидокислотами, у них одна из первичных гидроксильных групп глицерина замещена на остаток фосфорной кислоты. Глицерофосфолипиды могут иметь ацильную форму (R – остаток высшей жирной кислоты); либо алкильную форму (R – остатки высших жирных спиртов). Встречаются в различных органах и тканях животных, а также в моллюсках, осьминогах.
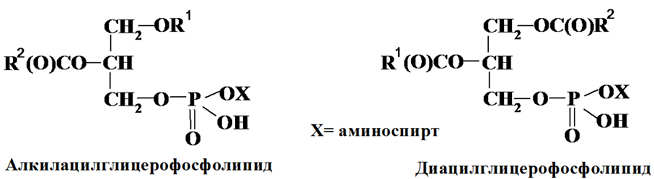
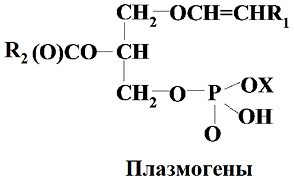
Глицерофосфолипиды с одной кратной связью называют плазмогенами, они обнаружены в тканях и органах всех животных. В организме человека они составляют 22% от общего числа фосфолипидов (в головном мозге – белое вещество, мозговая оболочка).
Фосфолипиды обнаружены в микроорганизмах, в растениях. Простейшие глицерофосфолипиды – фосфатидовые кислоты – найдены во многих природных источниках, хотя их содержание невелико (1–5% от общего количества фосфолипидов), они являются предшественниками для биосинтеза других фосфолипидов.
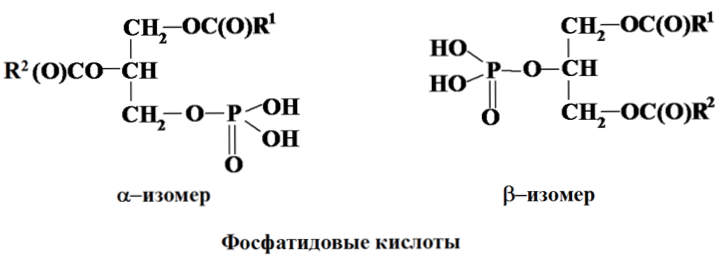
Эти соединения имеют кислый характер и способны к дальнейшей этерификации, например фосфатидоглицерол – продукт этерификации глицерином. Природные фосфатидовые кислоты являются в основном a-изомерами.
Моноаминофосфолипиды (Р:N=1:1)
Лецитины – глицерофосфолипиды, содержащие холин (одна гидроксильная группа остатка фосфорной кислоты этерифицирована холином) и его изомеры. В состав лецитинов входят глицерин, высшие жирные кислоты, фосфорная кислота и холин. Остаток фосфорной кислоты находится либо при α-, либо у β-углеродном атоме. Наличие в молекуле кислотной НО-группы при атоме фосфора и основной холиновой приводит к образованию цвиттериона в широком диапазоне рН.
Кефалины – глицерофосфолипиды, содержащие аминоспирт этаноламин – NH2(CH2)2OH.
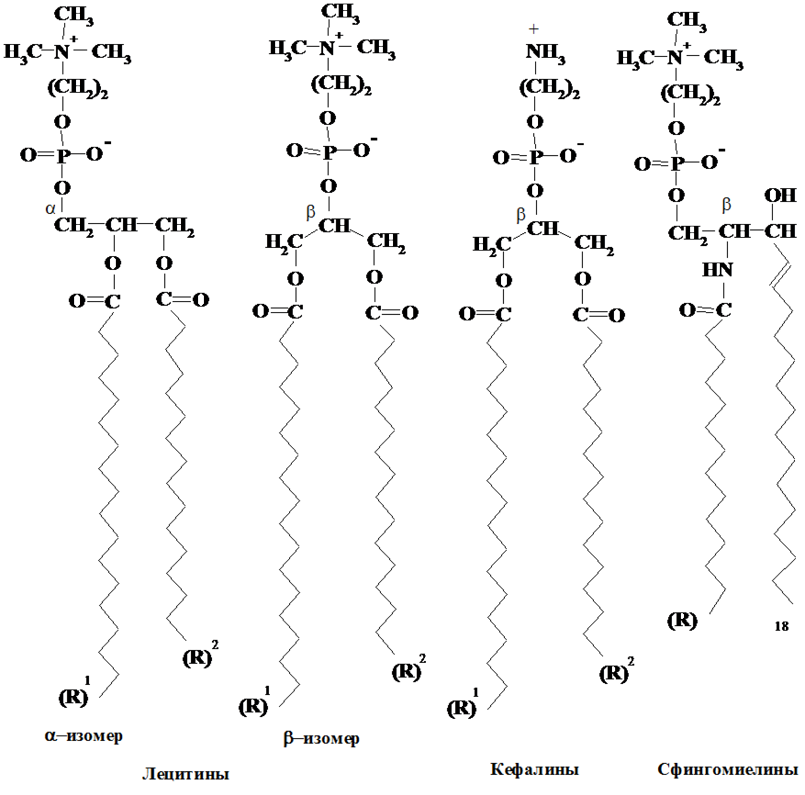
Остаток фосфорной кислоты находится либо у a-, либо у b-углеродного атома глицерина. К этой же группе относятся фосфолипиды, в которых остаток фосфорной кислоты этерифицирован серином – фосфатидилсерин.
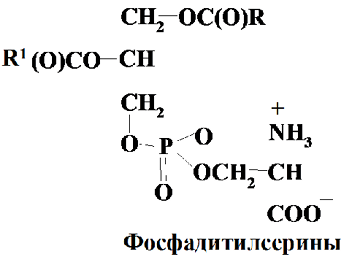
В составе лецитинов, кефалинов, фосфатидилсеринов довольно много жирных кислот разного состава. Обычно лецитины и кефалины встречаются в маслах. Фосфатидилсерины имеют в своем составе остаток аминокислоты серина. Присутствие свободной карбоксильной группы придает им кислотный характер. В природных источниках встречается главным образом в виде калиевых солей. В фосфолипидах животного происхождения фосфатидилсерина больше (до 15%), чем в растительных фосфолипидах (до 5%).
Диаминофосфолипиды – сфингомиелины (P:N = 1:2)
Сфингомиелины содержат остаток спирта (сфингозина), фосфорной кислоты, холина, высших жирных кислот. Обладают и кислотными, и основными свойствами, встречаются в основном в животных тканях (мозговых и нервных).
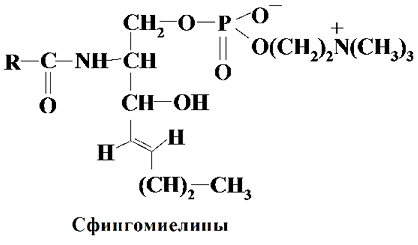
Все фосфолипиды содержат и гидрофобную и есть обладают бифильностью по отношению к растворителям. Длинноцепочечные алкильные радикалы обладают липофильностью, а фосфатное звено вместе с остатком спиртовой компоненты проявляет гидрофильность за счет ионных пар и гидроксильных групп, способных к образованию водородных связей.
Отсюда свойства фосфолипидов выступать в качестве эмульгаторов. Они способны образовывать на поверхности раздела фаз (вода – неполярная жидкая фаза) прочные пленки.
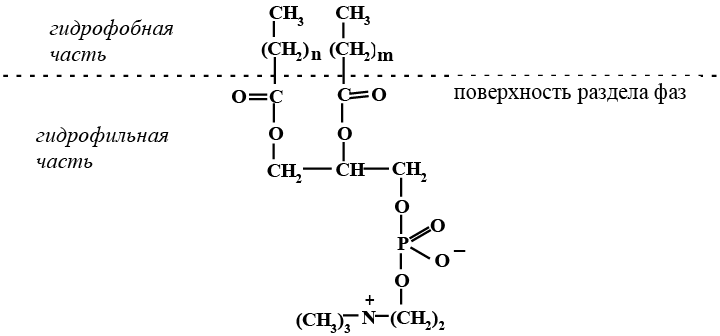
Фосфолипиды находят применение в качестве эмульгаторов в производстве маргарина, шоколада, кондитерских изделий. Выделяют фосфолипиды, главным образом, из яичных желтков, сейчас из семян сои.
Стерины широко распространены в природе, входят во все растительные и животные жиры, в свободном состоянии или в виде сложных эфиров жирных кислот – стеридов – входят в состав каждой клетки. Они растворимы в жирах и вместе с ними извлекаются из клеток. Различают животные стерины – зоостерины, растительные – фитостерины и стерины микробиологического происхождения – микостерины.
Стерины относятся к обширному классу биологически важных соединений – стероидов – и состоят их четырех циклов: А, Б, В – шестичленные, Г – пятичленные циклы. Если спиртовая группа расположена в положении – 3, то их называют стеролами.
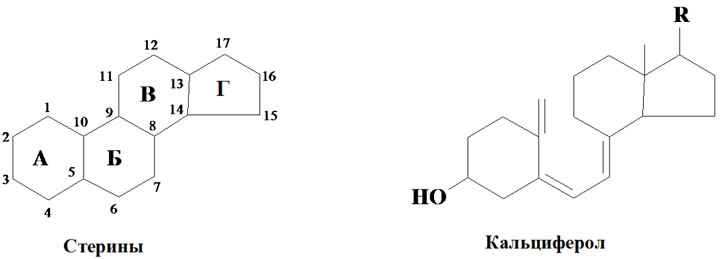
Под действием УФ стеролы превращаются в разновидность витамина D (кальциферол) в результате разрыва цикла Б между 9 и 10 атомами углерода. Метильная группа превращается в метиленовую, возникает система из трех сопряженных двойных связей, что характерно для витамина D. В положении 10 и 13 находятся метильные группы, в положении 17 – боковая цепь, длина и строение которой различны.
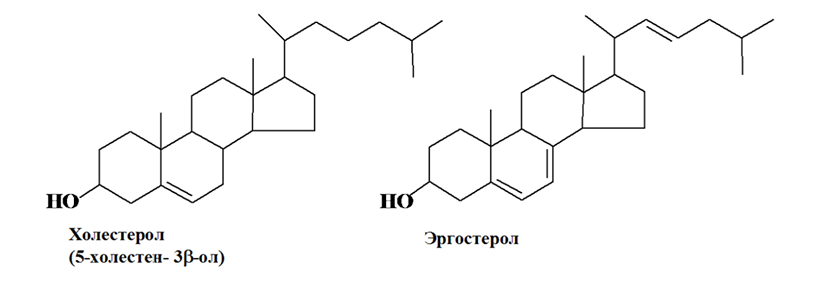
Из зоостеринов самый известный – холестерин (ол)1 – вторичный спирт с одной кратной связью, эмпирическая формула – С27H46O. Он широко распространен в организме высших животных, в том числе и человека, много его в головном и спинном мозге, желчи, в клетках кожи. Из растительных стеринов известны ситостерол и стигмастерол и ряд других стеролов.
Содержание стеролов в некоторых жирах приведено в табл. 1.4.5.
Таблица 1.4.5. Содержание стеролов в растительных маслах и животных жирах
|
Наименование жира |
Массовая доля, стеролов, % |
|
Арахисовое |
0,19–0,25 |
|
Какао |
0,17–0,20 |
|
Касторовое |
0,50 |
|
Кокосовое |
0,06–0,08 |
|
Кукурузное |
0,58–1,00 |
|
Кунжутное |
0,43–0,55 |
|
Льняное |
0,37–0,48 |
|
Оливковое |
0,23–0,31 |
|
Соевое |
0,15–0,48 |
|
Рапсовое |
0,35–0,50 |
|
Хлопковое |
0,26–0,57 |
|
Пальмовое |
0,03 |
|
Пальмоядровое |
0,06–0,12 |
|
Подсолнечное (рафинированное) |
0,08–0,11 |
|
Подсолнечное (нерафинированное) |
0,09–0,12 |
|
Зародышей пшеницы |
1,30–5,60 |
|
Рисовых отрубей |
0,75 |
|
Коровье |
0,24–0,50 |
|
Бараний |
0,03–0,10 |
|
Говяжий |
0,08–0,14 |
|
Свиной (лярд) |
0,11–0,12 |
Ситостерол является основным компонентом стеринов высших растений. Он доминирует на ранних стадиях созревания плодов оливы, томата, семян подсолнечника и сорго. Стигмастерол становится доминирующим в зрелых плодах.
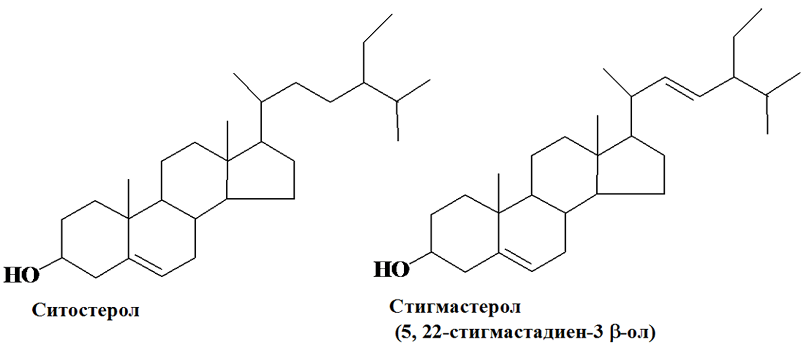
Эргостерол получают из грибов, дрожжей, спорыньи, он имеет три кратные связи, одна из них – в боковой цепи. Это биологический предшественник витамина D.
Холестерол
Холестерол является не только объектом пристального внимания исследователей различных областей, но и камнем преткновения, страсти по которому кипят почти весь ХХ век. Холестерол был открыт французскими химиками. В 1769 году Пулетье де ла Саль выделил из желчных камней «жировоск», а в 1789 году А. Фуркруа выделил его в чистом виде. В 1815 году М. Шеврель также выделил это соединение и назвал холестерином. Позднее было установлено наличие в нем спиртовой группы, и он был переименован в холестерол. Однако строение его было окончательно установлено лишь в 1934 году и подтверждено химическим синтезом холестерола в 1951 году.
Холестерол в основном присутствует в животных клетках. Прежде всего это клеточные оболочки животных, которым холестерол придает необходимую прочность за счет того, что он встраивается в углеводородные цепочки жирных кислот клеточных мембран и таким образом «цементирует» липопротеиновую пленку. В оболочках клеток печени содержание холестерола составляет 17%, в мембранах внутриклеточных структур – около 3%. Миелиновое многослойное покрытие нервных волокон, которое выполняет изолирующую функцию, содержит 22% холестерола. Белое вещество мозга содержит 14% холестерола, а серое вещество мозга – 6%. Прочная оболочка эритроцитов крови человека на 23% состоит из холестерола. Общее содержание холестерола в организме взрослого человека, по некоторым оценкам, лежит в интервале от 100 до 140 г, причем около 25% его находится в головном мозге.
Таблица 1.4.6. Содержание холестерола в пищевых продуктах
|
Наименованиепродукта |
Массовая доля холестерола, мг% |
|
Мозги говяжьи и свиные |
2000 |
|
Яичный желток (сухих веществ 50%) |
1510 |
|
Печень трески |
746 |
|
Почки |
300 |
|
Икра осетровая (зернистая) |
300 |
|
Печень говяжья |
270 |
|
Масло сливочное «Вологодское» |
190 |
|
Креветки (дальневосточные) |
160 |
|
Жир говяжий (топленый) |
110 |
|
Телятина |
80–110 |
|
Свинина |
60–100 |
|
Говядина |
60–70 |
|
Куры |
40–80 |
|
Кальмары дальневосточные |
85 |
|
Баранина |
70 |
|
Сметана, 20% жирности |
66 |
|
Творог жирный, 18% жирности |
60 |
|
Щука |
50 |
|
Сметана, 10% жирности |
30 |
|
Треска |
30 |
|
Молоко козье |
30 |
|
Молоко, 3,5% жирности |
10 |
|
Молоко, 1,5% жирности |
5 |
|
Творог нежирный |
2 |
Холестерол был выделен из многих продуктов животного происхождения, больше всего его содержится в яичных желтках, почках, печени и мозгах говяжьих, печени трески, икре осетровых (табл. 1.4.6). В растительных продуктах холестерол обнаружен в незначительных количествах, более заметно его присутствие в томатах.
Суточная потребность в холестероле составляет 2,5 г, причем 80% этой потребности синтезируется организмом, главным образом, в печени (эндогенный холестерол), а 20% должно поступить с пищей (экзогенный холестерол). Содержание холестерола в организме взрослого человека, по некоторым оценкам, составляет от 100 до 140 г, причем около 25% его находится в головном мозге. Холестерол в организме присутствует как в свободном состоянии (спиртовая форма), так и в виде эфиров: холестеролсульфат, холестеролфосфат, пальмитохолестерол, стеоратохолестерол, миристинхолестерол. В крови 2/3 холестерола находится в свободном состоянии и 1/3 в виде эфиров.
Биологическими предшественниками холестерола являются тритерпены: сквален (С30) и ланостерол (С30).
Схема биосинтеза холестерола и продукты его метаболизма представлены на рисунке 10.
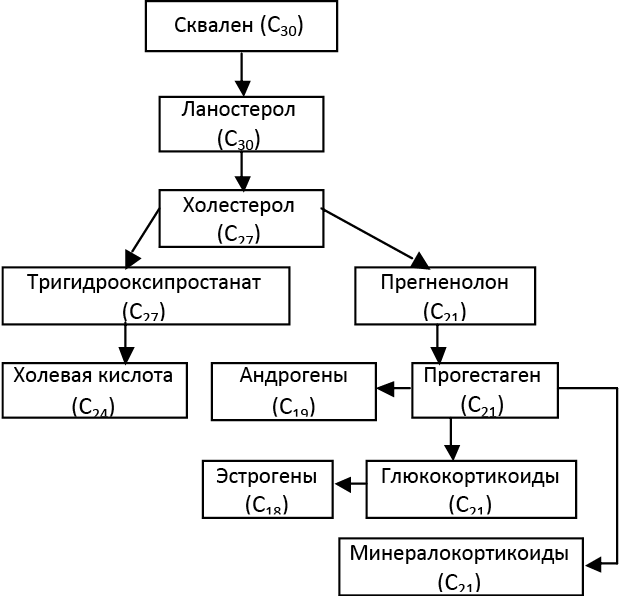
Рис. 10. Схема биосинтеза и метаболизма холестерола
Холестерол метаболизирует с образованием трех важнейших для организма групп биорегуляторов: желчные кислоты, кортикостероиды и половые гормоны. Желчные кислоты, прежде всего холевая кислота, содержатся в желчи многих животных, стимулируют расщепление и усвоение жиров.
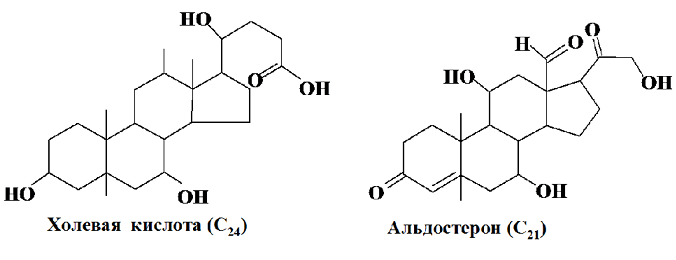
Кортикостероиды регулируют водный, солевой и углеводный обмены, из них альдостерон – главный минералокортикоид, стимулирующий транспорт натрия через почечные канальцы. Кортизол – глюкокортикостероид, стимулирующий глюконеогенез и образование гликогена, способствует расщеплению жиров и белков.
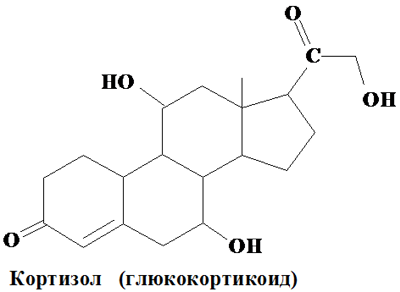
И наконец, продуктами метаболизма холестерола являются половые гормоны – андрогены (С19) – мужские половые гормоны, которые стимулируют развитие и функционирование мужской половой системы, и эстрогены (С18), регулирующие формирование и функционирование женских половых органов и молочных желез. Трудно переоценить значение этих важнейших групп низкомолекулярных биорегуляторов, биологическим предшественником которых является холестерол. К тому же нужно учесть, что холестерол входит в состав клеточных мембран, в том числе мембран головного и спинного моз га. Мембраны нейрона ответственны за возникновение и проведение нервного импульса, и таким образом холестерол важен для нормальной работы нейронов и механизмов памяти. Нарушение метаболизма холестерола приводит к серьезным заболеваниям, то есть холестерол является жизненно важным и необходимым компонентом нормального функционирования организма.
Тем не менее, вторая половина ХХ века характеризуется отчаянной борьбой за снижение холестерола в пище. Это обусловлено тем, что высокое содержание холестерола в крови было связано с развитием сердечно-сосудистых заболеваний, в частности, холестерол рассматривался как важный фактор риска развития атеросклероза. Антихолиностериновая теория получила очень широкое распространение во всех слоях общества, и только в начале ХХI века появились сообщения, которые сначала осторожно, а потом все настойчивее выразили сомнение по поводу правильности этой теории. Прежде всего количество холестерола, поступающего с пищей, гораздо меньше, чем его количество, вырабатываемое в организме печенью, то есть уровень холестерола в крови определяется не столько внешними факторами (питанием), сколько внутренними факторами – состоянием самого организма. Кроме того, известно, что дефицит холестерола в крови может способствовать развитию других заболеваний, в частности бесплодия, депрессивного состояния, нарушения работы головного мозга.
Холестерол, являясь жироподобным веществом, не растворяется в воде. В крови он присутствует в составе комплекса липопротеинов. Это надмолекулярные комплексы переменного состава, в которые входят белок, фосфолипиды, образующие вокруг липидных «капелек» гидрофильную оболочку и делающие их растворимыми в воде. Белки, входящие в состав липопротеиновых частиц, носят название аполипопротеины или просто апопротеины. Они выполняют три основные функции: способствуют растворению частиц за счет связывания с фосфолипидами, регулируют реакции липидов с ферментами и связывают липопротеины с рецепторами на поверхности клеток. Каждая липопротеиновая частица имеет в своем составе несколько апопротеинов, которые во многом определяют ее функциональные свойства.
В настоящее время выделено несколько фракций липопротеинов, входящих в состав крови. В зависимости от плотности, размеров и состава входящих в них липидов и апопротеинов различают: хиломикроны (ХМ), липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП) и липопротеин (а) (ЛП(а)). Состав липопротеинов представлен в табл. 1.4.7.
Таблица 1.4.7. Содержание основных компонентов в липопротеинах разной плотности
|
Показатель |
Липопротеины |
||||
|
Хило-микроны |
ЛПОНП |
ЛПНП |
ЛПВП2 |
ЛПВП3 |
|
|
Плотность, г/мл |
<0,95 |
<1,006 |
1,019–1,063 |
1,063–1,1250 |
1,125–1,210 |
|
Диаметр, нм |
80–90 |
30–80 |
18–25 |
5–12 |
|
|
Массовая доля, % |
|||||
|
Белок |
2 |
10 |
25 |
55 |
|
|
Триацилглицериды |
85 |
50 |
10 |
4 |
|
|
Холестерол |
1 |
7 |
8 |
2 |
|
|
Эфиры холестерола |
3 |
13 |
37 |
15 |
|
|
Фосфолипиды |
9 |
20 |
20 |
24 |
|
Хиломикроны – наиболее крупные, но и самые легкие частицы. Они образуются при всасывании жира клетками, выстилающими тонкий кишечник. ХМ осуществляют транспорт экзогенных липидов, преимущественно триацилглицеридов и в меньшей степени холестерола, к тканям. ХМ являются источниками всех липопротеинов и содержат в своем составе ТАГ (80% от массы) и холестерол (10% от массы), окруженные белковой и фосфолипидной оболочкой.
Липопротеины очень низкой плотности по составу сходны с ХМ, но синтезируются в печени. Состоят в основном из эндогенных ТАГ и эфиров холестерола. Их плотность составляет 0,950–1,006 г/мл. ЛПОНП подвергаются липолизу в плазме крови и превращаются в ЛППП.
Липопотеины промежуточной плотности содержат в своем составе больше эфиров холестерола, имеют плотность 1,006–1,019 г/мл. Часть ЛППП захватываются рецепторами печени, часть превращается в ЛПНП.
Липопротеины низкой плотности – высокомолекулярные вещества, внешняя оболочка которых состоит из фосфолипидов, а внутренняя – из белков. Холестерол и его эфиры находятся внутри комплекса (рис. 11).
Рис. 11. Структура холестерола
(Кац Дэвид Л., Гордон Дебра Л. Холестерин: и друг, и враг. С. 23. 2006)
По массе это самая большая фракция липопротеинов крови, они переносят 75–80% холестерола. Считается, что именно ЛПНП способствуют образованию атеросклеротических бляшек, так как образуют жироподобный налет на стенках артерий, причем чем мельче и плотнее частицы ЛПНП, тем они опаснее. Это так называемый плохой холестерол.
Другая фракция липопротеинов крови – липопротеины высокой плотности (ЛПВП). Это частицы гораздо меньшего размера. Переносят в крови 20–25% холестерола. ЛПВП – это «чистильщики артерий», они «вскрывают» ЛПНП, отбирают у них часть холестерола и направляют его в печень, убирая из кровотока. Его называют «хорошим холестеролом». Таким образом, состояние кровеносных сосудов зависит не столько от общего содержания холестерола в крови, сколько от соотношения ЛПНП и ЛПВП. Чем меньше содержание ЛПНП и больше содержание ЛПВП, тем лучше. Нормой считается пропорция ЛПНП : ЛПВП = 5:1, а идеальной – 3,5:1.
Липопротеины (а) представляют собой частицы с плотностью 1,051–1,082 г/мл, сходные с ЛПНП и отличаются уникальностью входящего в него апобелка. Лп (а) участвует в процессе атеротромбоза, и его концентрация в крови напрямую зависит от тяжести атеросклероза.
Таким образом, связь содержания холестерола в крови и развитие атеросклероза и ишемической болезни сердца в действительности оказалась гораздо сложнее, и полувековая борьба с холестеролом сейчас представляется не столь эффективной, как это казалось ранее. Поскольку нужно анализировать не только общий уровень холестерола, а прежде всего соотношение ЛПНП и ЛПВП, в которых холестерол и его эфиры находятся внутри оболочки из фосфолипидов и белка. Кроме того, появились и другие маркеры развития атеросклероза, например, содержание липопротеина (а) и гомоцистеина. Атеросклероз и ишемическая болезнь сердца – это многофакторные заболевания и могут развиться и при низком уровне холестерола в крови, а обилие в меню богатой холестеролом пищи не всегда приводит к ним. Здесь играют роль многие факторы, в том числе это генетические, гормональные нарушения, стрессовые состояния. Как и в любом деле, в питании должен быть разумный компромисс – отказ от пищи, содержащей холестерол, бессмысленен, а ее обилие чревато негативными последствиями.
Воски являются жироподобными веществами, как правило, сложного состава, но основу их составляют сложные эфиры неразветвленных длинноцепочечных жирных кислот и жирных спиртов.
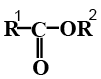
Воски входят в состав кожного жира животных, содержатся в черенках листьев, в некоторых бактериях, например микобактериях и коренбактериях. Известны два основных типа восков – простые и сложные.
К простым воскам относятся эфиры нормальных кислот и высших нормальных первичных спиртов с числом атомов углерода 8–18 и более. Наиболее часто встречаемыми компонентами простых восков являются лаурилпальмитат, цетилпальмитат, миристилстеарат, стеарилстеарат и др. Известны также ненасыщенные воски, например цетилолеат, олеилпальмитат и др. Воски сальных желез птиц содержат эфиры нормальных спиртов с разветвленными жирными кислотами.
К сложным воскам относят эфиры разветвленных одно- или двухатомных спиртов и разветвленных жирных кислот или оксикислот. Примерами сложных восков являются цериды – воски Mycobacterium tuberculosis, которые представляют собой диэфиры фтиоцеролов (разветвленных С33-С35-диолов) и микоцерозиновых кислот (разветвленных С29-С32-кислот). Кожный жир животных содержит диэфирные воски двух типов: производные оксикислот, в которых гидроксильная группа оксикислот этерифицирована жирной кислотой, а карбоксил – жирным спиртом; производные a-, b-алкандиолов, в которых гидроксильные группы диола этерифицированы жирными кислотами.
В состав восков чаще всего входят следующие кислоты:
СН3(СН2)14СООН – пальмитиновая (гексадекановая),
СН3(СН2)22СООН – лингоцериновая (тетракозановая),
СН3(СН2)24СООН – церотиновая (гексакозановая);
и высшие жирные спирты, неразветвленные, первичные:
СН3(СН2)14СН2ОН – цетиловый (гексадеканол),
СН3(СН2)24СН2ОН – цериловый (гексакозанол),
СН3(СН2)28СН2ОН – мирициловый (триаконтанол).
Иногда в образовании восков принимают участие и такие спирты, как эйкозанол-2 СН3(СН2)17СНОН-СН3 и октадеканол-2 СН3(СН2)15СНОН-СН3 и другие высшие спирты. В состав животных восков входят эфиры холестерола. Общее число атомов углерода обычно составляет 30–60. Примером сложных эфиров вышеуказанных кислот и спиртов может быть цетин – главный компонент спермацета – С15Н31СООС16Н33. Эфир церотиновой кислоты и цетилового спирта – С25Н51СООС16Н33 – основной компонент китайского воска, а эфир церотиновой кислоты и мирицилового спирта – С25Н51СООС30Н61 – основной компонент пальмового воска.
Воски широко распространены в природе и входят в состав защитных покрытий листьев, стеблей и плодов растений, предохраняя их от излишней потери влаги – это растительные воски. Аналогичную защитную функцию воски выполняют у насекомых, животных и микроорганизмов.
По химическим и физико-химическим свойствам воски близки к жирам, но отличаются от них большей устойчивостью к гидролизу, только в щелочной среде они могут быть гидролизованы с трудом. Они труднее окисляются, поэтому прогоркание для них не характерно. Воски более гидрофобны по сравнению с глицеридами и фосфолипидами, они не образуют поверхностно-активных пленок и макроструктур, подобных липидным бислоям.
Классифицируются воски по агрегатному состоянию и по происхождению. Таким образом, различают воски твердые и жидкие, а также воски животных, насекомых, растительные воски, ископаемые.
В пищевой промышленности воски используются для покрытий пищевых изделий с целью снижения влагопотерь и повышения сохранности.
МЕТОДЫ ОПРЕДЕЛЕНИЯ СТЕРИНОВ
Стерины входят в состав неомыляемой фракции жиров и при непродолжительном омылении они не разрушаются. В дальнейшем их разделение ведут либо путем экстракции, либо хроматографическим способом. Существует большое количество методов определения стеринов. Наиболее исследованы методы определения холестерола как соединения, входящего в ткани живого организма и выполняющего важные физиологические функции. На практике для определения стеринов используют следующие методы: колориметрические, нефелометрические, титриметрические, газохроматографические, гравиметрические и др.
Хроматографический метод анализа стеринов широко используется в исследовательских целях. Он нашел применение при оценке подлинности молочного жира на наличие примеси растительных жиров (ГОСТ Р 51471–99. «Жир молочный. Метод обнаружения растительных жиров газожидкостной хроматографией стеринов»). Метод основан на осаждении стеринов дигитонином. Образующиеся при этом дигитониды растворяют в смеси формамида с диметилфорамидом, а затем экстрагируют стерины пентаном. Окончательное разделение стеринов ведут методом ВЖХ.
В основе многих аналитических методов, имеющих практическую значимость, лежат различные химические реакции. Это в первую очередь реакция стехиометрического окисления оксигруппы стеринов и последующее определение продуктов их окисления. Практическое значение имеет метод, основанный на ферментативном окислении и колориметрическом определении образующегося пероксида водорода.
Выбор метода осложняется тем, что стерины встречаются как в свободном (неэтерифицированные), так и связанном (этерифицированные) виде, в этой связи количественный анализ стеринов ведут в несколько этапов. Одноступенчатые методы не требуют подготовки анализируемого образца: экстракции либо выделения стеринов. Однако они не свободны от влияния неспецифичных хромогенов.
Двухступенчатые методы включают обычно стадии хроматографического разделения или экстракции стеринов с помощью органических растворителей (этилового спирта, метанола, диэтилового эфира и хлороформа), удаляя тем самым вещества, мешающие проведению анализа.
Трехступенчатые методы включают дополнительную стадию гидролиза эфиров. Первоначально определяют содержание свободных стеринов, а потом после гидролиза – общее содержание стеринов. В многоступенчатах методах для дополнительной очистки стеринов используют способность дигитонина осаждать их.
Из химических методов наибольшее распространение получили колориметрические, которых насчитывается около 150. Они основаны на изменении окраски исследуемых растворов в результате протекания химической реакции и обычно применяются для анализа липидных экстрактов или хроматографически однородных фракций.
Среди колориметрических методов практическое значение имеют методы Либермана-Бурхарда, Златкинса-Зака, ферментативные, которые находят применение как для исследовательских целей при анализе суммарных липидных экстрактов или хроматографически однородных фракций, так и в медицине.
Так, например, в некоторых химических реакциях интенсивность окраски эфиров холестерола выше, чем у свободного холестерола, что снижает надежность результатов анализа.
МЕТОДЫ ОПРЕДЕЛЕНИЯ ФОСФОЛИПИДОВ
Источником фосфора в жирах являются фосфолипиды, которые различаются и по составу, и содержанию в них фосфора. Так, в растительных маслах присутствует несколько групп различных фосфолипидов (фосфатидилэтаноламины, фосфатидилхолины, фосфатидилсерины, инозитфосфатиды) и продукты их взаимодействия с сахарами (меланофосфатиды) и с госсиполом (госсифосфатиды).
Для определения фосфорсодержащих веществ в жирах и маслах применяют различные химические и физические методы. Результаты выражают в процентах фосфора, оксида фосфора (Р2О5) (табл. 1.4.12).
Таблица 1.4.12. Содержание фосфолипидов в растительных маслах
|
Содержание фосфолипидов |
Растительное масло |
|
|
Нерафинированное |
Рафинированное |
|
|
На фосфор, не более % |
0,2–0,6 |
0,2 |
|
На окись фосфора (Р2О5), не более % |
0,096 |
0,005 |
|
На стеароолеолецитин, не более % |
1,0 |
0,05 |
В качестве физического метода определения фосфорсодержащих веществ применяют метод атомно-абсорбционной спектроскопии (ГОСТ Р 52676–2006. «Масла растительные. Методы определения фосфорсодержащих веществ»). Названный метод позволяет оценить содержание фосфора в жиросодержащем материале в диапазоне концентраций 0,20–230 мг (в пересчете на оксид фосфора – 5×10–4–5,3×10–1%).
Метод основан на испарении анализируемой пробы жира, смешанной с модификатором, в графитовой кювете и последующем измерении поглощения свободными атомами фосфора при длине волны 213,5 нм. Матричный модификатор представляет собой раствор лантан-органометаллического стандарта в циклогексане (с массовой долей лантана 5000 мг/кг в 10 мл циклогексана).
Содержание фосфора находят по величине интегрального аналитического сигнала и рассчитывают по калибровочному графику. Калибровочные растворы готовят из 2%-го раствора соевого лецитина в контрольном образце масла с добавлением 4 г циклогексана. В качестве контрольного образца масла применяют жидкое рафинированное масло с содержанием фосфора менее 2 мг/кг, его же используют для приготовления калибровочных растворов. Содержание фосфора в контрольном образце масла находят колориметрическим методом.
В основе химических методов лежит окисление образца различными окислителями (минерализация), которое проводят двумя способами – путем сухого или мокрого сжигания. В случае мокрого сжигания окислителем выступает смесь концентрированных кислот (азотной и серной); в методе сухого сжигания – сухой порошок окиси магния. В обоих случаях органическая часть сгорает, а фосфор, входящий в состав фосфорсодержащих веществ жира, образует фосфорные кислоты или их соли. Полученные в результате сжигания фосфорные кислоты или их соли осаждают в присутствии азотнокислого аммония и азотной кислоты избытком молибденовокислого аммония в виде желтого осадка фосфорномолибденовокислого аммония следующего состава:
(NH4)2Mo4 + H3PO4 + NH4NO3 + HNO3 → (NH4)3РО4 ×12МоО3 × 2HNO3 × Н2О.
МЕТОДЫ ОПРЕДЕЛЕНИЯ ВОСКОПОДОБНЫХ ВЕЩЕСТВ
Воскоподобные вещества – это сложная смесь восков, свободных длинноцепочечных жирных кислот различной степени окисленности, гидроксикислот, свободных первичных, вторичных высокомолекулярных спиртов и диолов, сложных эфиров двухатомных спиртов, длинноцепочечных алифатических углеводородов и кетонов. В масле, извлекаемом из семян, при охлаждении образуется так называемая «сетка» из взвешенных кристаллов твердого воска. Из-за близких значений относительной плотности воска и масла кристаллы восков практически не оседают, что затрудняет их извлечение, ухудшает товарный вид масла. Присутствие в составе восков продуктов окисления жирных кислот инициирует протекание в масле окислительных процессов.
Существует множество методов определения восков в растительных маслах. Они отличаются между собой по продолжительности, некоторые требуют специальное сложное оборудование. Не всегда методы, используемые для анализа сырых масел, пригодны для масел после вымораживания (винтеризации).
1 В отечественной литературе обычно называют холестерином, за рубежом – холестеролом, что с химической точки зрения более правильно, так как он имеет у третьего атома углерода спиртовую гидроксильную группу.

