К этому классу относятся как простые, так и сложные окислы, не содержащие в своем составе гидроксильных ионов. Сложные окислы нет смысла выделять особо, тем более что по кристаллическому строению они либо аналогичны простым окислам, либо немногим отличаются от них.
Относящиеся сюда минералы в большинстве обладают сравнительно простыми кристаллическими структурами. Более сложны лишь кристаллические структуры минералов особо стоящей группы кварца SiO2.
Отношения между катионами и анионами кислорода в этих минералах колеблются в пределах от 2 : 1 (А2Х) до 1 : 2 (АХ2). В сложных окислах, кроме того, устанавливаются различные соотношения между катионами — обычно 1 : 1 и 1 : 2. Лишь для некоторых редких соединений мы наблюдаем более сложную картину соотношений.
Как известно, вода в природе находится в трех состояниях: твердом (лед, снег), жидком (дождь, минеральные источники, реки, озера, моря и океаны) и газообразном (водяной пар в атмосфере и вулканических эксгаляциях). По своим свойствам вода стоит особняком среди окислов металлов и металлоидов. Вода играет огромную роль в химических процессах, совершающихся в земной коре: химические реакции происходят главным образом в водных растворах. Без воды, так же как и без кислорода, немыслимо существование и органической жизни на Земле.
Это соединение мы рассмотрим лишь в твердом состоянии.
ЛЕД — Н2О. Химический состав. Н — 11,2 %, О — 88,8 %. Иногда содержит газообразные и твердые механические примеси.
Сингония гексагональная; дигексагонально-пирамидальный в. с. L66P. Пр. гр. P63mc(С 46v). а0 = 7,82; с0 = 7,36. Кристаллическая структура. Лед обладает молекулярной кристаллической структурой, в локальном отношении близкой к структуре алмаза (каждая молекула Н2О имеет координационное число 4).
Строение самой молекулы Н2О характеризуется симметрией, близкой к симметрии тетраэдра, что обеспечивается механизмом химической связи в молекуле. Все шесть внешних электронов кислорода гибридизированы (приведены в одинаковое возбужденное состояние), образуя четыре σ-облака, в двух из которых находится лишь по одному электрону. Одноэлектронные σ-облака принимают в себя s-электроны двух атомов водорода, образуя с ними полярную ковалентную связь (рис. 143а).
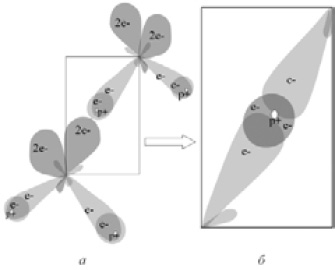
Рис. 143. Возникновение тетраэдрической координации в структуре льда:
а — конфигурация валентных электронов в свободной молекуле воды
(густота заливки приближенно пропорциональна
электронной плотности, o — протон).
Показана также вторая молекула, притягивающаяся к первой;
б — принятие протоном второго электрона от L-пары и образование
донорно-акцепторной связи c равномерным распределением двух
центрированных протоном s-электронов между
облаками бывших связывающей пары и L-пары атомов кислорода
Каждое из двух других σ-облаков атома кислорода образовано парой неподеленных электронов (L-парой), занимающей значительный объем. Все электронные σ-облака испытывают взаимное отталкивание и пытаются принять положение с максимальной угловой удаленностью друг от друга. Если бы все они были совершенно одинаковыми, мы получили бы симметричную тетраэдрическую конфигурацию, однако на конце двух из четырех σ-облаков расположены протоны H+, которые, частично компенсируя отрицательный заряд электронов, уменьшают взаимное отталкивание этих облаков, в результате чего угол между двумя связями O—H в свободной молекуле отклоняется от идеального для тетраэдра значения 109,5° и принимает значение 104,5°.
На концах двух таких σ-облаков сосредоточен избыточный положительный заряд протонов, в то время как на двух неподеленных L-парах — отрицательный. Молекулы с таким распределением заряда способны связываться друг с другом по донорно-акцепторному механизму (протон — акцептор электрона, L-пара — донор), приобретая взаимное расположение, обеспечивающее сближение протонов одних молекул с L-парами других (рис. 143б). В силу этого в структуре льда слабосвязываемые между собой водородной донорно-акцепторной связью молекулы Н2О ориентированы таким образом, что положительно заряженные участки одних молекул направлены к отрицательно заряженным участкам других молекул. В структуре льда распределение электронов между протонами и двумя сортами σ-облаков делается неразличимым и молекулы приобретают тетраэдрическую симметрию.
По общему расположению молекул структура льда аналогична структуре вюртцита (см. рис. 96) с той лишь разницей, что места Zn и S заняты молекулами Н2О. При таком строении (с низким координационным числом, равным 4) получается далеко не плотная упаковка структурных единиц (остаются большие просветы). Этим и объясняется то, что удельный вес льда ниже, чем воды.
Облик кристаллов. Для кристаллов льда в подавляющем большинстве случаев характерно скелетное развитие. Кристаллические образования снежинок, обладающих гексагональной симметрией, чрезвычайно разнообразны по формам шестилучевых фигур роста. Широко известны также дендриты и узорчатые образования льда. В ледяных пещерах кристаллы льда встречаются в виде правильных шестиугольных пластинок, таблитчатых индивидов и сложных по форме сростков. Известны уникальные по величине и хорошему огранению кристаллы льда (до 40 см в длину и до 15 см в поперечнике), встреченные на северо-востоке Азии в горных выработках в условиях вечной мерзлоты. В одном случае они были обнаружены в полостях мощной зоны дробления на глубине 55–60 м от поверхности, где температура мерзлых боковых пород равна 3–4 °С. Как показали измерения прикладным гониометром, наиболее часто встречающимися гранями кристаллов оказались гексагональная дипирамида и пинакоид (на самом деле — две гексагональные пирамиды и два моноэдра).
В другом случае очень крупные кристаллы льда столбчатого облика были встречены в заброшенных горных выработках, пройденных в зоне окисления сульфидного месторождения. При вскрытии этих выработок было установлено, что они заполнены сплошной массой льда, среди которого встречались полости с минерализованной водой и газами, находившимися под большим давлением. Наибольшие кристаллы льда достигали длины до 60 см при 15 см в диаметре и имели вид гексагональных призм, притупленных гранями гексагональной пирамиды.
Агрегаты. В сплошных массах нередко наблюдаются кристаллически-зернистые агрегаты (плотный снег, фирн в ледниковых районах). Глетчерный лед состоит из очень крупных, неправильных по форме кристаллических зерен. Всем хорошо известны также натечные формы сосулек, образующихся из переохлажденной воды на теневой стороне крыш при таянии снега, а также в ледяных пещерах (сталактиты и сталагмиты). В граде, выпадающем из туч в грозовые периоды, нередко можно наблюдать концентрически-слоистое строение. В морозное осеннее утро часто образуются выцветы на земле (иней).
Цвет. Лед бесцветен или слабо окрашен в голубоватый цвет (в больших массах). Блеск стеклянный. Оптически положительный. Показатель преломления очень низкий: Ng = 1,310, Nm = 1,309.
Твердость 1,5. Хрупок. Спайностью не обладает. Уд. вес 0,917 (меньше, чем у воды). Уменьшение удельного веса при кристаллизации свойственно также металлическому висмуту.
Происхождение. Лед образуется на поверхности водных бассейнов при охлаждении воды. Возникающая вначале ледяная каша смерзается в плавающую корочку, на которой снизу нарастают кристаллические индивиды, вытягивающиеся в вертикальном направлении вдоль шестерных осей симметрии. Снег образуется в холодных областях атмосферы за счет водяного пара. При тех же условиях появляются иней и ледяные узоры на охлажденных предметах. В ледяных пещерах с низкой температурой в лед превращаются просачивающиеся по трещинам поверхностные воды.
В районах вечной мерзлоты с суровым климатом, малоснежной продолжительной зимой в зимнее время образуются так называемые наледи, т. е. ледяные покровы, иногда на огромных по размерам площадях. Речные наледи возникают при полном промерзании реки в мелких местах, в результате чего текучие воды ищут выход на поверхность, пропитывая снежные покровы. Другие наледи образуются за счет глубинных вод, выходящих из-под толщ вечной мерзлоты в виде не замерзающих зимой ключей. На происхождении ледников и глетчерных льдов останавливаться не будем.
Месторождения льда общеизвестны. Из ледяных пещер, встречающихся в районах с холодной длинной зимой и коротким летом, отметим известную у нас Кунгурскую пещеру (Пермская область), привлекающую многочисленных туристов красотой множества сверкающих на сводах кристаллов. Из ледовых пещер зарубежных стран наиболее замечательна пещера Добшины (Словакия), в которой свыше 7000 м2 покрыто льдом. Общий объем льда составляет 120 000 м3. Ледяные стены достигают 15 м высоты.
Практическое значение. Лед применяется в холодильном деле и для различных целей в быту и технике, в травматологии. В суровых холодных районах, где зимой нет возможности достать воду для питья, последняя получается из мощного речного и озерного льда.
Из окислов металлов типа А2О в природных условиях известен лишь один куприт — закись меди (Сu2О). Искусственно в структуре куприта кристаллизуется также Ag2O, не установленная в природе.
КУПРИТ — Сu2О. Название происходит от лат. cuprum — медь. Синоним: красная медная руда. Так называемые кирпичная медная руда (с примесью гидроокислов железа) и смоляная медная руда (с примесью кремнезема и гидроокислов железа) являются по существу минеральными смесями.
Химический состав. Си — 88,8 %. Очень часто устанавливается в качестве механической примеси самородная медь, а в скрытокристаллических разностях — Fe2O3, SO2 и Н2О.
Сингония кубическая; гексаоктаэдрический в. с. 3L44L366L29PC. Пр. гр. Рn3–т(O4h). a0 = 4,26. Кристаллическая структура может быть формально представлена как объемноцентрированная кубическая решетка с атомами кислорода в узлах, в которую вдвинута со смещением на одну четверть вдоль телесной диагонали гранецентрированная решетка того же размера, но с медью в узлах. Координация меди равна двум, а кислорода — четырем. Облик кристаллов октаэдрический (рис. 144), реже кубический или додекаэдрический; в исключительных случаях (месторождение Корнуолл, Англия) присутствуют грани пентагонтриоктаэдра (проявление гипоморфизма). Кристаллы обычно мелки. Изредка наблюдаются игольчатые или волосистые индивиды, а также объемные скелетные кристаллы с тремя системами взаимно перпендикулярных игл (халькотрихит). Чаще встречается в сплошных зернистых, иногда в землистых (в смеси с посторонними примесями) агрегатах.
Рис. 144. Кристалл куприта
Цвет куприта красный до свинцово-серого (в тонкозернистых или скрытокристаллических агрегатах). Черта коричнево-красная или буровато-красная (при растирании вторым бисквитом желтеет). Блеск кристаллов в изломе алмазный или полуметаллический. В тонких осколках куприт полупрозрачен. N = 2,85.
Твердость 3,5–4. Хрупкий. Спайность по {111} ясная. Уд. вес 5,85–6,15.
Диагностические признаки. Характерными свойствами являются: алмазный блеск, красная черта и особенно парагенезис с самородной медью, иногда другими вторичными минералами меди — малахитом, азуритом и др. От киновари, прустита и пираргирита отличается по черте (у киновари — ярко-красная, у прустита и пираргирита — красная, зеленеющая при растирании, а у куприта — коричнево-красная), но главным образом по поведению п. п. тр.
П. п. тр. на угле чернеет, затем спокойно плавится и в восстановительном пламени дает королек меди. При нагревании в щипчиках окрашивает пламя в слабый зеленый цвет, а после смачивания HCl — в красивый голубой. В HNO3 легко растворяется, раствор зеленеет, а от прибавления избытка аммиака становится синим.
Происхождение и месторождения. Куприт образуется почти исключительно при экзогенных процессах окисления халькозиновых, реже борнитовых руд, распространенных в медных месторождениях в зоне вторичного сульфидного обогащения (ниже уровня грунтовых вод). Массовое развитие его может иметь место главным образом в том случае, когда в силу тех или иных причин (в частности, при понижении базиса эрозии) происходит понижение уровня грунтовых вод и возникшая до этого зона, богатая халькозином, попадает в сферу окисления. Процесс окисления халькозина при растворении в воде образующейся серной кислоты протекает, очевидно, по следующей реакции:
Cu2S + 2О2 + Н2О → Cu2O + H2SO4.
Легко видеть, что в случае недостатка кислорода по этой реакции вместо Сu2О или наряду с ним будет возникать металлическая медь, которая действительно очень часто наблюдается в образцах куприта (узнается по занозистости в изломе купритовых масс).
Вместе с самородной медью изредка встречается в некоторых осадочных породах, содержащих растительные остатки. В этих случаях он, по всей вероятности, является продуктом восстановления органическими веществами сульфата закиси меди при некотором доступе кислорода по схеме:
Cu2SO4 + С + О → Сu2О + СО2 + SO2.
В тех случаях, когда концентрация углекислоты в растворах становится значительной, куприт оказывается неустойчивым. В природе широко распространены псевдоморфозы карбоната меди — малахита — по куприту. В более редких случаях он замещается другим карбонатом меди — азуритом.
В больших количествах и в хорошо образованных кристаллах встречался в Гумешевском, Меднорудянском и Турьинских рудниках на Урале, а также в ряде месторождений Алтая и в других местах в ассоциации с малахитом, азуритом, гидроокислами железа и пр. Из зарубежных пользовалось известностью месторождение Шесси близ Лиона (Франция), где встречались кристаллы 2–3 см в поперечнике, и многие другие.
Практическое значение. Является одной из самых лучших медных руд. В далекие времена купритовые руды вместе с самородной медью, очевидно, представляли собой важнейшие объекты эксплуатации. В настоящее время в значительных массах встречается сравнительно редко.
К этому семейству принадлежат сравнительно редкие в природе простые окислы типа АХ, т. е. двухвалентных металлов (Mg, Ni, Fe, Mn, Cd, Ca, Be, Zn). К этому семейству условно отнесем и оксиды двухвалентных Cu и Pb. Мы здесь кратко рассмотрим лишь цинкит, а также тенорит.
ЦИНКИТ — ZnO. Химический состав. Zn — 80,3 %, О — 19,7 %. Сингония гексагональная; дигексагонально-пирамидальный в. с. Пр. гр. P63mc(С 46v). Кристаллическая структура типа вюртцита. Наблюдался в виде вкрапленных зерен и сплошных масс.
Цвет оранжево-желтый до темно-красного из-за примеси марганца (чистый синтетический ZnO бесцветен). Черта оранжево-желтая. Блеск алмазный. Оптически положительный. Ng = 2,029 и Nm = 2,013.
Твердость 4. Спайность по {100} средняя. Уд. вес 5,66.
П. п. тр. не плавится. В кислотах растворяется. Прочие свойства. Обладает детекторными свойствами.
Месторождения. В России отмечен в Дукатском месторождении (Магаданская область). В значительных скоплениях встречается в известном контактово-метасоматическом месторождении Франклин в Нью-Джерси (США) в ассоциации с виллемитом — Zn2SiO4 и франклинитом — (Zn,Mn)Fe2O4 в кальцитовых массах. Кристаллы очень редки и наблюдаются только в более поздних кальцитовых жилах. Указывался также в свинцово-цинковом месторождении Олькуш (Польша), близ Саравеццы в Тоскане (Италия) и в других местах.
ТЕНОРИТ — СuО. Химический состав. Сu — 79,9 %, О — 20,1 %. Синоним: мелаконит (массивная разность).
Сингония моноклинная. Призматический в. с. L2PC. Пр. гр. С2/с. Редкий. Наблюдается обычно в виде тонкочешуйчатых или землистых агрегатов.
Цвет черный или серовато-черный. Черта серовато-черная. Блеск полуметаллический. В полированных шлифах сильно анизотропен.
Твердость 3,5. Хрупкий. Уд. вес 5,8–6,4.
П. п. тр. не плавится. В кислотах легко растворяется.
Месторождения. Встречается в зонах окисления медносульфидных месторождений в ассоциации с купритом, лимонитом, хризоколлой, малахитом, гидроокислами марганца и другими гипергенными минералами. На Урале был описан в районе Турьинских медных рудников (Северный Урал), в Меднорудянском месторождении (у Нижнего Тагила). Обнаружен среди продуктов осаждения из эксгаляций вулкана Большой Толбачик (Камчатка) в виде щеток пластинчатых кристаллов.
В больших количествах наблюдался в медных месторождениях в районе Верхнего озера в штате Мичиган (США), в месторождениях пустыни Атакама (Чили) и др. В тонких чешуйках на лаве встречается на Везувии и Этне в ассоциации с хлоридами щелочей и меди.
4. Семейство корунда — ильменита
Кроме составляющих группу корунда полуторных простых окислов типа А2Х3 (Al2O3, Fe2O3, Cr2O3, V2O3) сюда, по данным рентгенометрии, следует отнести также принадлежащие к группе ильменита сложные (двойные) окислы типа ABX3 (где A = Mg, Fe2+, Mn2+, Zn и B = Ti), кристаллизующиеся в структуре, производной от типа корунда. Характерно, что Fe2O3 с FeTiO3 при высоких температурах образуют непрерывный ряд твердых растворов, распадающихся при охлаждении.
Все минералы группы корунда кристаллизуются в тригональной сингонии и имеют однотипные кристаллические структуры — тип Аl2О3 (рис. 145). Лишь Fe2O3 в природных условиях встречается в двух модификациях: α-Fe2O3 — тригональной сингонии и γ-Fe2О3 — кубической. Симметрия двойных окислов типа FeTiO3 более низкая по сравнению с простыми окислами типа Fe2O3, так как катионы их неэквивалентны. Образуются они в условиях относительно высоких температур.
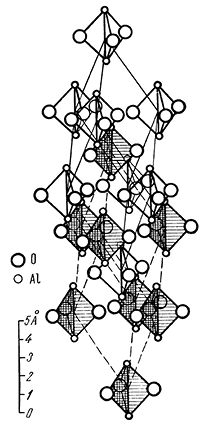
Рис. 145. Кристаллическая структура корунда,
изображенная в виде групп Аl2О3
КОРУНД — Аl2О3. Название минералу дано еще в Индии. Для Аl2О3 известны следующие полиморфные модификации: 1) α-Аl2О3 (корунд) — тригональная, наиболее устойчивая в природных условиях; образуется в широком температурном интервале (500–1500 °С); 2) β-Аl2О3 — гексагональная, устойчивая при очень высоких температурах; превращение α-Аl2О3 в β-Аl2О3 происходит при температурах 1500–1800 °С; эта модификация образуется при очень медленном охлаждении расплава Аl2О3; 3) γ-Al2O3 — кубическая, с кристаллической структурой типа шпинели (так же как и в случае маггемита); получается искусственно при прокаливании гидрата окиси алюминия (бемита) до температур ниже 950 °С; при более высоких температурах неустойчива — переходит в α-Аl2О3.
Химический состав. Аl — 53,2 %. Кристаллические разности исключительно чисты по составу. Ничтожные примеси Сr обусловливают красную, Fe3+ — коричневую (в смеси с Mn) и розовую, Ti4+ — синюю, смесь Fe2+ и Fe3+ — черную окраску.
Сингония тригональная; дитригонально-скаленоэдрический в. с. L363L23РС. Пр. гр. R3–c(D63d). a0 = 4,76; с0 = 13,01; а0 : с0/2 = 1 : 1,363. Кристаллическая структура Аl2О3 изображена на рисунке 145 в виде групп Аl2О3 по углам двух ромбоэдров, слагающих элементарную ячейку. Несмотря на кажущуюся сложность, она имеет довольно простую структурную схему. Ионы кислорода находятся в плотнейшей гексагональной упаковке и располагаются слоями перпендикулярно тройной оси (рис. 146), наложенными один на другой. Катионы Аl располагаются между двумя такими слоями в виде гексагональной сетки, заполняя две трети октаэдрических пустот (т. е. пустот между шестью анионами кислорода, три из которых принадлежат одному, а три других, повернутых относительно первых на 180°, — другому слою ионов кислорода). При этом группы каждых трех ионов кислорода образуют общую грань для двух смежных октаэдров в соседних слоях. Характерно, что катионные слои наложены друг на друга таким образом, что в каждой вертикальной колонке из октаэдров, так же как и в слое, чередуются два заселенных с одним незаселенным, причем пары заселенных октаэдров по вертикали образуют винтовые тройные оси.
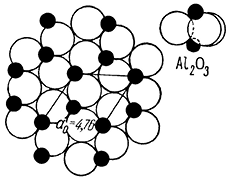
Рис. 146. Один слой плотнейшей упаковки анионов кислорода
с катионами алюминия (в октаэдрических пустотах)
в проекции на плоскость (0001). В гексагональной ячейке
располагаются один над другим шесть слоев Аl—О.
Вверху показана группа Аl2О3 (в профиле)
Облик кристаллов. Обычно наблюдаются довольно хорошо образованные бочонковидные, столбчатые, пирамидальные и пластинчатые кристаллы, достигающие иногда больших размеров (до дециметра в поперечнике). Наиболее часто встречаются грани гексагональной призмы {110}, гексагональных дипирамид {22
1}, {22
3}, ромбоэдра {10
1} и пинакоида {0001} (рис. 147). Часто грани призм и дипирамид, а также грани пинакоида бывают покрыты косой штриховкой. В других случаях наблюдается штриховка в горизонтальном направлении вследствие двойникования по пинакоиду. Корунд обычно бывает вкраплен в породу, но известны месторождения, где он слагает сплошные зернистые массы (наждак).
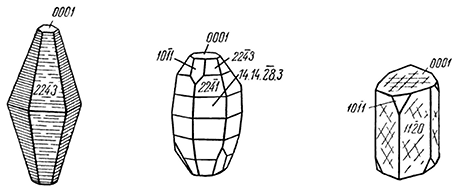
Рис. 147. Кристаллы корунда
Цвет корунда обычно синевато-, розовато- или желтовато-серый (для мутных полупрозрачных разностей). Встречаются прозрачные кристаллы различной окраски. Разновидности прозрачных драгоценных корундов: лейкосапфир — бесцветный, сапфир — синий, рубин — красный, «восточный топаз» — желтый, «восточный аметист» — фиолетовый, «восточный изумруд» — зеленый, «звездчатый корунд», обладающий астеризмом при рассматривании на свет (в плоскости базопинакоида наблюдается перебегающая при поворотах опалесценция в форме шестилучевой звезды, обусловленная ориентированными микроскопическими включениями). Блеск стеклянный. Nm = 1,767 и Np = 1,759.
Твердость 9. Спайность практически отсутствует, однако часто наблюдается отдельность по пинакоиду, а также по основному ромбоэдру (вследствие полисинтетического двойникования), в последнем случае выколки по отдельности очень близки к прямоугольным параллелепипедам. Уд. вес 3,95–4,1. Температура плавления искусственного корунда 2040 °С.
Диагностические признаки. Легко узнается по форме кристаллов, штриховке на гранях, часто характерной синевато-серой окраске и высокой твердости. От похожего на него кианита (Al2SiO5) отличается по отсутствию совершенной спайности и по высокой твердости. Рубин от красной шпинели отличим по форме кристаллов, а в неправильных зернах — только под микроскопом. П. п. тр. не плавится. В кислотах не растворяется.
Происхождение и месторождения. Иногда встречается в богатых глиноземом и бедных кремнеземом глубинных магматических породах — корундовых сиенитах и анортозитах в ассоциации с полевыми штатами, изредка в других породах (андезитах, базальтах и др.). Известны также корундсодержащие сиенитовые пегматиты, имеющие промышленное значение.
Контактово-метасоматические месторождения корунда образуются в превращенных в кальцифиры известняках по соседству с изверженными породами. Здесь он часто бывает представлен драгоценными разновидностями (рубином, сапфиром и др.). В ряде случаев (вторичные кварциты) месторождения его возникают в связи с резким воздействием кислых флюидов на глиноземистые осадочные и изверженные породы. Корунд в этих случаях ассоциирует с такими минералами, как андалузит, силлиманит, а также рутил, диаспор и др.
Корундовые породы могут образоваться также в результате регионального метаморфизма за счет богатых глиноземом осадков (бокситов) вне прямой связи с изверженными породами. Породы при этом превращаются обычно в кристаллические сланцы.
Являясь химически очень устойчивым минералом, он часто устанавливается в россыпях.
При гидротермальных процессах ранее образовавшийся корунд иногда подвергается гидратации, т. е. превращению в диаспор (НАlО2). В поверхностных условиях это явление не наблюдается за редкими сомнительными исключениями.
В России ряд месторождений корунда известен на восточном склоне Урала — в Кыштымском районе, в верховьях р. Борзовки, в виде корундсодержащих плагиоклазовых жил среди ультраосновных пород, вдоль восточного берега оз. Иртяш, где среди метаморфических пород, в частности мраморов, располагаются линзообразной и неправильной формы тела наждака, содержащего хлоритоид и сульфиды. В Ильменских горах (Южный Урал) крупные кристаллы синевато-серого корунда находятся в сиенитовых пегматитах в полевых шпатах с мусковитом и самарскитом. В пределах хромитового месторождения Рай-Из (Полярный Урал) богатый хромом густо-красный корунд в виде столбчатых кристаллов до дециметра в длину известен в флогопит-плагиоклазовых метасоматитах, образовавшихся при воздействии на ультраосновные породы кислых флюидов. В метасоматически измененных глиноземистых гнейсах и ассоциированных с ними амфиболитах совместно с кислым плагиоклазом, биотитом, альмандином и амфиболом метакристаллы розового корунда встречаются в Северной Карелии (Хитостров, Варацкое озеро и др.). Синий корунд с герцинитом, содалитом и биотитом обнаружен в фенитизированных ксенолитах вмещающих пород среди нефелиновых сиенитов в ряде пунктов Хибинского щелочного массива (Кольский полуостров). Образовавшиеся при метаморфизме бокситов агрегаты красного корунда с кианитом находятся в Чайнытском месторождении (Южная Якутия). Из проявлений россыпного корунда отметим зерна сапфира в аллювии р. Кедровка в Приморском крае.
Интересное месторождение высококачественного корундового сырья (наждака) Семиз-Бугу находится в Баян-Аульском районе Казахстана (в 320 км к юго-западу от Павлодара). Гнездообразные рудные тела сложены здесь почти сплошным зернистым корундом темно-синего или серого цвета. От вмещающих их кварцитов они отделены зонами андалузитовой породы. С корундом парагенетически связаны мусковит, местами гематит, рутил, диаспор и другие минералы. Из иностранных большей известностью пользуются месторождения драгоценных прозрачных корундов (рубина и сапфира) в Верхней Бирме (в зоне контакта мраморов с гранитами), в Австралии (в щелочных базальтах) в Таиланде (в россыпях, главным образом сапфир) и др.
Практическое значение. Корунд, обладающий высокой твердостью, главное применение находит в качестве абразивного материала. С этой целью из него изготовляются точильные корундовые круги, диски, наждачные бумаги и порошки («минутники»), используемые при шлифовании и полировании различных изделий (главным образом в металлообрабатывающей промышленности). Прозрачные окрашенные разности употребляются в качестве драгоценных камней в ювелирном деле.
В ряде стран, производящих дешевую электроэнергию, изготовляют искусственный корунд (алунд) путем электроплавки богатых глиноземом пород, в частности бокситов. Искусственный корунд перед естественным обладает преимуществами — чистотой и крупнозернистостью. В специальных печах путем сплавления порошка Аl2О3 с 2,5 % Cr2O получаются рубины, тождественные природным, а с Ti и также с Co — сапфиры.
ГЕМАТИТ — α-Fe2O3. Название происходит от греч. гематикос — кровавый. В природе известны две полиморфные модификации окиси железа: α-Fe2O3 — тригональная, устойчивая и γ-Fe2О3 — кубическая, менее распространенная, которую мы рассмотрим отдельно. Синонимы: железный блеск, железная слюдка, красный железняк (плотная скрытокристаллическая разность), железная сметана (красная порошковатая разность). Мартитом называют псевдоморфозы гематита по магнетиту.
Химический состав. Fe — 70 %. Иногда в виде изоморфных примесей присутствуют Ti (титангематит) и Mg. В незначительных количествах обнаруживается также вода (гидрогематит, встречающийся обычно в колломорфном виде). В скрытокристаллических плотных массах часто устанавливается присутствие кремнезема и глинозема в виде механических примесей.
Сингония тригональная; дитригонально-скаленоэдрический в. с. L363L23PC. Пр. гр. R3–c(D63d). a0 = 5,029, c0 = 13,73. Кристаллическая структура аналогична структуре корунда (см. рис. 145). Облик кристаллов. Сравнительно часто встречается в пластинчатых, ромбоэдрических и таблитчатых кристаллах (рис. 148), образующихся в пустотах. Обычны формы: ромбоэдров (101), (10
4), пинакоида {0001}, гексагональной дипирамиды (22
3) и др. Вследствие образований полисинтетических двойников по ромбоэдру {10
1}, плоскости пинакоида, так же как и у корунда, бывают покрыты треугольной штриховкой (см. рис. 148), а плоскости ромбоэдра {10
1} — параллельной диагональной штриховкой. Простые двойники наблюдаются редко, преимущественно по ромбоэдру и призме. Известны оригинальные скопления слегка искривленных пластинчатых кристаллов, сросшихся по плоскостям, близким к положению пинакоида (так называемые «железные розы»). Агрегаты. Часто встречается в сплошных плотных скрытокристаллических массах, листоватых или чешуйчатых агрегатах. Крупные почкообразные формы с радиальноволокнистым строением носят название «красной стеклянной головы» (см. рис. 46). В очень многих случаях тонкораспыленная безводная окись железа в отдельных минералах и горных породах окрашивает их в интенсивный красный цвет. Таковы, например, сургучно-красные яшмы (кремнистые породы), красные мраморы, красные глинистые сланцы.
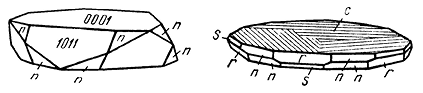
Рис. 148. Кристаллы гематита: n {223}, r {10
1}, s {02
1}, с {0001}
Цвет кристаллических разностей гематита железно-черный до стально-серого. В тончайших пластинках он просвечивает густо-красным цветом. Землистые, распыленные разности обладают ярко-красным цветом. Черта вишнево-красная. Блеск металлический до полуметаллического. Иногда наблюдается синеватая побежалость. Полупрозрачен только в очень тонких пластинках. Nm = 3,01 и Np = 2,78 (для Li-света).
Твердость 5,5–6. Хрупок, благодаря чему часто проявляет ложную пониженную твердость агрегатов, сложенных из пластинок. Спайность отсутствует. Характерна грубая отдельность по ромбоэдру {101}. Уд. вес 5–5,2.
Диагностические признаки. Довольно легко отличается от похожих на него минералов (ильменита, магнетита, гётита и др.) по вишнево-красной черте, высокой твердости, пластинчатым или чешуйчатым агрегатам и по отсутствию магнитности.
П. п. тр. не плавится. Характерно, что в восстановительном пламени при высокой температуре он становится магнитным (превращается в магнетит). Очень медленно растворим в HCl.
Происхождение и месторождения. Гематит образуется в окислительных условиях в самых различных генетических типах месторождений и горных пород. Температуры образования могут колебаться в широких пределах, но при высоких температурах он неустойчив.
1. Как составная часть в очень незначительных количествах он иногда присутствует в изверженных породах, преимущественно кислых (в гранитах, сиенитах, андезитах и др.). Сравнительно редко встречается также в пегматитах как минерал, образовавшийся в гидротермальный этап процесса.
2. В некоторых гидротермальных месторождениях он встречается в значительных массах в ассоциации с кварцем, баритом, иногда магнетитом, сидеритом, хлоритом и другими минералами. Явления позднейшего восстановления его до магнетита наблюдаются довольно часто. Однако в других местах устанавливается обратный процесс: превращение магнетита в гематит (процесс мартитизации). Очевидно, эти явления связаны с изменением окислительно-восстановительного потенциала уже после отложения этих минералов из гидротермальных растворов.
3. Как продукт вулканических эксгаляций обычно в небольших количествах встречается в виде кристаллов и налетов на стенках кратеров вулканов и в трещинах лав. В 1817 г. на Везувии в одной из трещин в течение 10 дней таким путем отложилась масса гематита мощностью около 1 м. По всей вероятности, он является результатом разложения возгонов хлористых соединений железа.
4. В коре выветривания в условиях сухого жаркого климата гематит и гидрогематит возникают в результате дегидратации первоначально образующихся гидроокислов железа. Этот необратимый переход легко доказывается искусственным путем при постепенном обезвоживании гётита. Нередко эти минералы ассоциируют с гидроокислами алюминия — диаспором и бёмитом (в железистых ярко-красных бокситах).
Известны гематито-гидрогематитовые образования сферолитовой формы с гладкой блестящей поверхностью почек («красная стеклянная голова»), обладающие концентрически-скорлуповатым строением и занозистым изломом. Отдельные концентрические зоны состоят из радиально-волокнистых масс то гематита, то гидрогематита, иногда гётита. Условия образования их недостаточно изучены.
Наконец, следует указать, что в странах с жарким климатом в верхних зонах магнетитовых месторождений нередко широко проявляется мартитизация, т. е. окисление магнетитовых масс с превращением их в гематитовые массы по реакции:
4Fe3O4 + O2 = 6Fe2O3.
5. При процессах регионального метаморфизма в условиях повышенной температуры и повышенного давления гематит нередко в весьма больших массах возникает в осадочных месторождениях бурых железняков путем их дегидратации. Таковы, в частности, оолитовые красные железняки, сланцы с железной слюдкой и железистые кварциты, состоящие из прослойков кварцита, перемежающихся с прослойками тонкочешуйчатого плотного гематита. Подобные кварциты содержат иногда огромные по размерам тела гематито-магнетитовых сплошных руд.
Гематит как высший окисел железа является химически стойким минералом в зоне окисления. Иногда наблюдаются лишь явления физического выветривания (дезагрегации) гематитовых масс с образованием «железной сметаны». Превращение кристаллических разностей его в гидроокислы устанавливается исключительно редко, и притом в совершенно особых условиях и в очень незначительном масштабе.
В России крупнейшие месторождения высококачественных гематито-магнетитовых руд, например Михайловское и Яковлевское, находятся в пределах Курской магнитной аномалии (КМА) в докембрийских железистых кварцитах, являющихся результатом регионального метаморфизма первоначально осадочных железистых толщ, многократно собранных в крутые складки. Руды этой формации имеются и в Кривом Роге (Украина).
Примером гидротермальных месторождений является Кутимское (Северный Урал), руды которого залегают в палеозойских доломитах и представлены кристаллическими массами крупнопластинчатого гематита, местами превращенного в магнетит. Оолитовые красные железняки в виде пластовых залежей распространены на западном склоне Среднего Урала — в Кусье-Александровском и Пашийском районах. Мартитовые руды в существенных количествах встречаются в верхних зонах ряда крупных магнетитовых месторождений Урала: на горах Магнитной, Высокой (у Нижнего Тагила) и др. Сростки типа «железных роз» отмечены в некоторых хрусталеносных жилах Приполярного Урала.
Из зарубежных месторождений отметим крупнейшие месторождения в докембрийских метаморфизованных толщах в районе Верхнего озера (США) и в Итабири (штат Минас-Жерайс, Бразилия). Большой интерес в минералогическом отношении представляет конктактово-пневматолитовое месторождение на о. Эльба, откуда происходят замечательные кристаллы железного блеска, экспонирующиеся во многих минералогических музеях. «Железные розы» встречаются в ряде мест в Альпах (Сен-Готтард и др.).
Практическое значение. Гематитовые руды принадлежат к числу важнейших железных руд, из которых выплавляются чугун и сталь. Значение их в народном хозяйстве и промышленности общеизвестно. Содержание железа в сплошных гематитовых рудах обычно колеблется от 50 до 65 %. Чистые разности порошковатого гематита употребляются в качестве красок и для изготовления красных карандашей.
ИЛЬМЕНИТ — FeTiO3, или FeO . TiO2. Название происходит от Ильменских гор (Южный Урал), где этот минерал впервые был установлен. Синоним: титанистый железняк.
Химический состав. Fe — 36,8 %, Ti — 31,6 %, О — 31,6 %. В качестве изоморфных примесей может содержать Mg, нередко в значительных количествах (пикроильменит), иногда Мn (до нескольких процентов), также Cr, Al и V. Существуют непрерывный изоморфный ряд FeTiO3—MgTiO3 (гейкилит) и, вероятно, ряд FeTiO3—MnTiO3 (пирофанит), а при высоких температурах устанавливается ряд и с Fe2O3 (гемоильмениты).
Сингония тригональная; ромбоэдрический в. с. L36C. Пр. гp. R3– (C 23i). а0= 5,083; с0 = 14,04. Кристаллическая структура аналогична структуре корунда с той лишь разницей, что места Аl через слой поочередно занимаются Fе2+и Тi4+. Такая замена разнородными ионами ведет к снижению симметрии структуры. Облик кристаллов толстотаблитчатый (рис. 149), ромбоэдрический, иногда пластинчатый. Наиболее часто наблюдаются следующие формы: пинакоид {0001}, ромбоэдры {101}, {02
1}, {22
3} и др. Двойники по ромбоэдру {10
1}. Обычно встречается в виде вкрапленных зерен неправильной формы, редко в сплошных зернистых массах. Под микроскопом ильменит в виде пластинчатых выделений устанавливается в некоторых разностях гематита в качестве продукта распада твердых растворов, но гораздо чаще он наблюдается в так называемых титаномагнетитах и изредка в некоторых титанистых разностях авгитов и других минералов тоже как продукт распада твердых растворов.
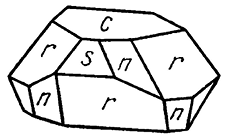
Рис. 149. Кристалл ильменита. с {001}, n {22
3}, r {10
1}, s {022
}
Цвет ильменита железно-черный или темный стально-серый. Черта большей частью черная до темно-серой, иногда бурая или буровато-красная (для разностей, содержащих в виде включений гематит). Блеск полуметаллический. Непрозрачен.
Твердость 5–6. Спайность несовершенная по ромбоэдру {101}, излом неровный и полураковистый. Уд. вес 4,72. Не ферромагнитен, гемоильмениты слабо магнитны.
Диагностические признаки. Похож на гематит. В кристаллах отличим по их формам (присутствуют только ромбоэдры, нет граней гексагональных дипирамид и скаленоэдров). В сплошных массах от гематита отличается по черте и более слабому блеску.
П. п. тр. не плавится. В восстановительном пламени становится явно магнитным. В порошке с трудом растворяется в концентрированной HCl с выделением окиси титана. После плавления с КНSО4 при кипячении с оловом дает синевато-фиолетовый раствор, при разбавлении водой розовый (реакция на титан).
Происхождение и месторождения. В качестве вкрапленников в кимберлитах содержится пикроильменит, являющийся одним из минералов-индикаторов, позволяющих обнаруживать коренные месторождения алмаза по ореолам механического рассеяния. В виде вкрапленности ильменит встречается в основных изверженных породах (габбро, диабазах, пироксенитах и др.), часто в ассоциации с магнетитом, а также в щелочных породах. В значительных количествах он иногда наблюдается в пегматитах некоторых типов (сиенитовых) в парагенезисе с полевыми шпатами, биотитом, ильменорутилом и др.
В гидротермально измененных изверженных породах ильменит, как правило, наблюдается в разложенном состоянии, будучи превращен в так называемый лейкоксен. Известны также случаи разложения ильменита с образованием механической смеси гематита и рутила с сохранением внешней формы кристаллов ильменита.
В России кристаллы ильменита, иногда значительных размеров, встречаются в пегматитах Ильменских и Вишневых гор около г. Миасса (Южный Урал) среди сиенито-гнейсов. В виде включений в титаномагнетитах он широко распространен во многих месторождениях.
В поверхностных условиях ильменит относительно устойчив и может, претерпевая дальнюю транспортировку, накапливаться в аллювиальных и особенно в прибрежно-морских россыпях с рутилом, цирконом и др. (см. рис. 58).
Из иностранных месторождений отметим норвежские: Экерзунд-Зоггендаль в виде жил в норитах (основная изверженная порода), Крагерё, где встречаются крупные кристаллы 6–7 кг весом, и др.
Практическое значение. Является главной рудой на титан (большая часть добывается из россыпей), используемый в виде TiO2 в качестве белой краски (титановых белил с высокой кроющей способностью), а также для сплавов с железом — ферротитана, содержащего 10–15 % Ti, для изготовления особых сортов стали и для других целей.
Способность металлического титана выдерживать высокие температуры, устойчивость к коррозии, способность свариваться и низкий удельный вес делают его особенно ценным сырьем для авиационной промышленности.
Сюда относятся окислы Mn, частью с Fe, существенно отличающиеся по кристаллическому строению от минералов группы корунда.
БРАУНИТ — Mn2+ Mn3+6 SiO12. Иногда пишут сокращенную формулу с другой стехиометрией: Мn2О3.
Химический состав. MnO — 44,8 %, MnO2 — 55,2 %. В брауните нередко устанавливается железо, иногда 10 % и выше. Спектроскопически обнаруживается также присутствие B и Ba. Последний элемент, возможно, связан с баритом, являющимся обычным спутником браунита.
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр. I4/acd(D204h). а0 = 13,44; с0 = 18,93. Структура координационная субслоистая. Может быть представлена в виде дефектной, сильно искаженной кубической плотнейшей упаковки кислорода с послойным заполнением октаэдров одного слоя катионами только Mn3+, а в другом слое наряду с октаэдрами Mn3+ имеются скрученные кубы Mn2+ и тетраэдры Si4+. Кристаллы имеют октаэдрический облик (рис. 150); тетрагональная дипирамида, приближающаяся по углам к октаэдру, находится иногда в комбинации с гранями призмы и пинакоида. Чаще наблюдается в зернистых агрегатах.
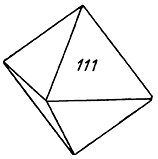
Рис. 150. Кристалл браунита
Цвет браунита черный до серого, с коричневым оттенком. Черта бурая до коричневой. Блеск полуметаллический. Непрозрачен.
Твердость 6. Спайность заметная по {111}. Уд. вес 4,7–5. Немагнитен.
Диагностические признаки. Похож на многие марганцевые черные минералы. Для него характерны высокая твердость, буровато-черная черта. С достоверностью может быть установлен в полированных шлифах под микроскопом и рентгенометрическим путем.
П. п. тр. не плавится. С бурой дает реакцию на Mn. В HCl с трудом растворяется с выделением из раствора хлора и студенистого кремнезема. В HNO3 разлагается на MnO и MnO2 (в осадке).
Происхождение и месторождения. Возникает в восстановительных условиях, но устойчив в пределах определенных значений восстановительно-окислительного потенциала. В более восстановительной обстановке замещается гаусманитом MnMn2O4. Встречается в некоторых контактово-метасоматических месторождениях, а также в гидротермальных жилах в ассоциации с различными минералами марганца и железа баритом, кварцем и др. В значительных массах распространен в регионально-метаморфизованных осадочных месторождениях марганца (формация гондитов).
В зоне окисления браунит неустойчив: постепенно окисляясь до высшей валентности Mn, превращается в псиломелан, а затем в более устойчивый в присутствии кислорода пиролюзит (MnO2).
На Урале известно гидротермальное месторождение Сапальское (у Нижнего Тагила) в известняках, где браунит ассоциирует с гаусманитом, гематитом, магнетитом, якобситом, сульфидами Fe, Pb и др. Известен также на Поперечном месторождении (Хабаровский край). В больших массах находится в ряде метаморфизованных осадочных месторождений в Центральном Казахстане: Джезды в Карсакпайском районе, где он в виде сплошных зернистых агрегатов наблюдается также в небольших жилах гидротермального происхождения; Караджал в Атасуйском районе и др.
Из иностранных месторождений следует указать крупные метаморфизованные месторождения Индии, Бразилии, Южной Африки (Постмасбург) и др.
Практическое значение. Браунитовые руды принадлежат к числу важнейших марганцевых руд, используемых в черной металлургии для выплавки ферромарганца, который идет в присадку при выплавке сталей в мартеновских печах. Бедные марганцем руды употребляются для подшихтовки при выплавке обыкновенных чугунов в домнах.
Минералы семейства шпинелидов с типовым составом RO . R2O3, согласно данным рентгенометрии, должны рассматриваться как двойные окислы, а не как соли кислородных кислот, т. е. не как алюминаты, ферриты и др. В этой группе широко представлены изоморфные смеси. В качестве трехвалентных металлов, замещающих друг друга, принимают участие Fe3+, Аl3+, Сr3+, V3+, Аl3+ и Mn3+, а в качестве двухвалентных — главным образом Mg2+, Fe2+, иногда Zn2+, Мn2+ и изредка, обычно в небольших количествах, Cu2+, Ni2+ и Со2+; кроме того, в составе шпинелидов может присутствовать Ti4+. Характерно, что двухвалентные ионы с большими ионными радиусами — Pb, Sr, Ca, Ba, а также одновалентные — Na и K — совершенно не участвуют в составе минералов этой группы. В зависимости от сочетаний перечисленных элементов различают большое количество минеральных видов, имеющих много общих свойств в форме кристаллов, физических признаках и условиях образования (возникают преимущественно при высоких температурах и давлениях).
Подавляющая их масса кристаллизуется в кубической сингонии, образуя кристаллы преимущественно октаэдрического облика. Лишь некоторые принадлежат к тетрагональной сингонии, причем облик их кристаллов также октаэдрический. Особняком стоит соединение аналогичной химической формулы — хризоберилл. Ионный радиус Be2+ настолько мал, что это соединение имеет существенно отличную структуру, кристаллизуясь в ромбической сингонии.
Кристаллическая структура минералов группы шпинели довольно сложная. Кислородные ионы плотно упакованы в четырех плоскостях, параллельных граням октаэдра (кубическая плотнейшая упаковка). В структурном типе нормальной шпинели (n-шпинель) двухвалентные катионы (Mg2+, Fe2+ и др.) окружены четырьмя ионами кислорода в тетраэдрическом расположении, в то время как трехвалентные катионы (Аl3+, Fe3+, Cr3+ и др.) находятся в окружении шести ионов кислорода по вершинам октаэдра. При этом каждый ион кислорода связан с одним двухвалентным и тремя трехвалентными катионами. На рисунке 151 изображен основной мотив структуры шпинели MgАl2О4 из AlO6-октаэдров в установке с вертикальной четверной осью. Все пустующие колонки этого мотива выполнены полосами из тетраэдров MgO4. Если обозначить двухвалентные катионы буквой А, а трехвалентные — В, то общая формула нормальной шпинели, с обозначением координационных чисел катионов верхними индексами, может быть записана в следующем виде: АIVВVI2О4. В структуре инвертированной (обратной) i-шпинели размещение катионов по позициям отвечает следующей формуле: ВIV(АВ)VIО4.
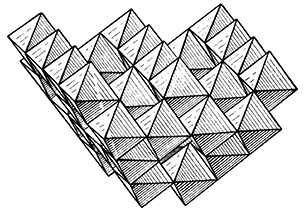
Рис. 151. Кристаллическая структура шпинели.
Основной мотив структуры из октаэдров в установке
с вертикальной четверной осью (по Н. В. Белову)
Таким образом, структура характеризуется сочетанием изометрических «структурных единиц» — тетраэдров и октаэдров, причем каждая вершина является общей для одного тетраэдра и трех октаэдров.
Эти особенности структуры хорошо объясняют такие свойства этих минералов, как оптическая изотропия, отсутствие спайности, химическая и термическая стойкость соединений, довольно высокая твердость и пр. Структурный тип шпинели допускает вариации параметров упаковки анионов кислорода и размеров катионных позиций без нарушения симметрии, что дает возможность принимать в этих позициях катионы с различными размерными характеристиками, обеспечивая высокую изоморфную емкость минералов этого семейства.
ШПИНЕЛЬ — MgAl2O4. Название происходит, вероятно, от лат. spinella — шип из-за формы кристаллов. Прозрачные разности, красиво окрашенные в различные цвета (красный, розовый, зеленый, синий, фиолетовый и др.), носят название благородной шпинели.
Химический состав. MgO — 28,2 %, Аl2О3 — 71,8 %. Наблюдаются примеси: Fe2O3, обусловливающая бутылочно-зеленую окраску (хлорошпинель); FeO, которая вместе с Fe2O3 вызывает коричневую или черную окраску; иногда ZnO, MnO, Сr2О3. Намечаются устойчивые даже при низких температурах изоморфные ряды с такими минеральными видами семейства, как ганит (ZnAl2O4), магнезиоферрит (Fe3+(MgFe3+)O4), галаксит (MnAl2O4) и герцинит Fe2+Al2O4.
Сингония кубическая; гексаоктаэдрический в. с. 3L44L366L29PC. Пр. гр. Fd3m(O7h). a0 = 8,86. Кристаллическая структура является типической и описана выше (шпинель имеет нормальную структуру). Облик кристаллов. Шпинель встречается преимущественно в виде идиоморфных октаэдрических кристаллов (рис. 152), иногда с дополнительными гранями тетрагонтриоктаэдра {211} и ромбододекаэдра {110}, обычно небольших размеров, но иногда попадаются очень крупные экземпляры (до 25 см). Двойники характерны по (111)-плоскостям плотнейшей упаковки ионов кислорода. Отсюда название: двойники «по шпинелевому закону» (рис. 153).
Рис. 152. Кристалл шпинели.
Обычная форма вообще для всех шпинелидов
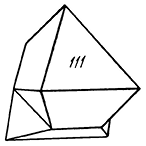
Рис. 153. Двойник по «шпинелевому закону»
Цвет. Бесцветные разности наблюдаются редко, большей частью шпинель окрашена в различные цвета, преимущественно розово-красных и сине-зеленых тонов. Черная разновидность (с высоким содержанием железа) называется плеонастом. Блеск стеклянный. Оптически изотропна. N = 1,718–1,75.
Твердость 8. Примеси Fe2O3 и Сr2О3 понижают ее до 7,5–7. Спайность по {111} несовершенная. Уд. вес 3,5–3,7 (наименьший у минералов из группы шпинели). Температура плавления 2150 °С.
Диагностические признаки. Характернейшими признаками шпинели являются октаэдрический облик кристаллов и высокая твердость. Исследование порошка минерала в поляризованном свете под микроскопом без труда дает возможность отличить изотропную шпинель от двупреломляющих, аналогичных по окраске и похожих по форме разновидностей корунда. От других минералов группы шпинели она отличается наименьшим удельным весом.
П. п. тр. не плавится. Кислоты не действуют.
Происхождение и месторождения. Шпинели наиболее часто встречаются в контактово-метасоматических образованиях среди доломитов и магнезиальных известняков в результате воздействия на них магматических флюидов при высоких температурах. В парагенезисе с ними в образующихся богатых карбонатами Ca и Mg магнезиальных скарнах — кальцифирах наблюдаются различные минералы того же происхождения: форстерит, пироксены (обычно диопсид или энстатит), амфиболы (тремолит), флогопит, фторсодержащие силикаты (группы гумита) и др.
Изредка встречается в пегматитах и магматических горных породах. Известны находки ее также в глубинных сильно метаморфизованных породах: гнейсах и кристаллических сланцах.
В поверхностных условиях шпинель совершенно устойчива и потому часто встречается в россыпях.
Сколько-нибудь значительные месторождения благородной шпинели в России пока не установлены. Отдельные экземпляры ее изумрудно-зеленой окраски были обнаружены в россыпях по р. Каменке в Кочкарском районе (Южный Урал); очевидно, она вместе с другими самоцветами образуется при разрушении распространенных в районе пегматитов. Затем были найдены шпинели розовой, синей и фиолетовой окраски в Прибайкалье в окрестностях Слюдянки. Изобильная вкрапленность крупных кристаллов черной шпинели (плеонаст) наблюдается с форстеритом и флогопитом в кальцифирах месторождений Гоновское, Канку и Каталах (Алдан, Якутия). Герцинит обнаружен в виде черных каемок вокруг синего корунда с содалитом, плагиоклазом и биотитом в районе Лопарского перевала в Хибинах (Кольский полуостров).
Крупное месторождение благородной розовой шпинели Кухи-Лал находится на Юго-Западном Памире (Таджикистан, близ границы с Афганистаном). Крупнейшие месторождения благородной красной шпинели известны на островах Цейлон и Борнео (в золотоносных россыпях), а также в Бирме, Таиланде, Афганистане и в других местах.
Практическое значение. В качестве драгоценных камней употребляются лишь совершенно прозрачные, лишенные трещиноватости кристаллы. Добыча производится обычно попутно с добычей золота или самоцветов (рубина). В рубиновых копях Могок (Северная Бирма) благородная шпинель ежегодно добывалась в количествах до 10 000 карат попутно с рубином (до 50 000 карат). Крупных скоплений в коренных породах неизвестно.
МАГНЕТИТ — Fe3+(Fe2+Fe3+)O4, применяются и сокращенные формулы: Fe2+Fe3+2O4 или даже — Fe3O4. Происхождение названия минерала неясно. Предполагают, что оно связано с местностью Магнезия (в Македонии) или с именем пастуха Магнеса, впервые нашедшего природный магнитный камень, который притягивал к себе железный наконечник его палки и гвозди его сапог. Синоним: магнитный железняк.
Химический состав. FeO — 31 %, Fe2O3 — 69 %. Содержание Fe — 72,4 %. Обычно бывает сравнительно чистым по составу. Разновидности: титаномагнетит (правильнее было бы писать Ti-магнетит, т. е. титанистый магнетит) с содержанием TiO2 (до нескольких процентов), существующий при высоких температурах в виде твердого раствора ульвёшпинели Fe2+(Fe2+Ti4+)O4 в магнетите, ульвёшпинель и выпадает в магнетитовой матрице при распаде твердого раствора, окисляясь обычно в дальнейшем до ильменита. Для многих титаномагнетитов характерно присутствие существенной примеси кулсонита Fe2+V3+2O4, что делает такие разности промышленно важным источником ванадия. Известен Cr-магнетит с содержанием Сr2О3 (до нескольких процентов). Изредка встречаются разности, богатые MgO (в Mg-магнетите до 10 %), Аl2О3 (15 %) и др. Здесь же следует упомянуть о сравнительно редко встречающейся в природе ферромагнитной окиси железа γ-Fe2О3 кубической сингонии, получившей название маггемита (начальные буквы слов магнетит и гематит).
Сингония кубическая; гексаоктаэдрический в. с. а0 = 8,374. Кристаллическая структура является структурой инвертированной шпинели, что и отражено в формуле, приведенной выше.
Облик кристаллов. Нередко наблюдающиеся кристаллы имеют октаэдрический, реже ромбододекаэдрический габитус (рис. 154). Грани {110} часто бывают покрыты штрихами, параллельными длинной диагонали ромбов. В базальтовом стекле под микроскопом устанавливается в виде мельчайших дендритов. Двойники по (111). Агрегаты. Большей частью встречается в сплошных зернистых массах или в виде вкраплений в изверженных, преимущественно основных породах. В пустотах можно встретить друзы кристаллов.
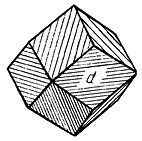
Рис. 154. Кристалл магнетита, q {110}.
Ахматовская копь около Златоуста (Южный Урал)
Цвет магнетита железно-черный, иногда с синеватой побежалостью на кристаллах. Черта черная. Блеск полуметаллический. Непрозрачен.
Твердость 5,5–6. Хрупок. Спайность отсутствует, однако у магнезиальных магнетитов часто наблюдается отчетливая отдельность по {111}. Уд. вес 4,9–5,2. Прочие свойства. Сильно магнитен, иногда полярно. При красном калении (около 580 °С, так называемая точка Кюри) магнетизм внезапно исчезает, но по охлаждении снова обнаруживается.
Диагностические признаки. По магнитности и черной черте обычно легко узнается и отличается от сходных с ним по внешнему виду минералов (гематита, гётита, гаусманита, хромита и др.), но не всегда легко отличим от реже встречающихся богатых закисью и окисью железа других минеральных видов группы шпинели: хромита (Fe2+Cr3+2O4), якобсита (Fe3+(Mn2+Fe3+)O4) и др.
П. п. тр. не плавится. В окислительном пламени вначале превращается в маггемит (γ-Fe2О3), затем в гематит, теряя магнитность. С бурой и фосфорной солью реагирует на железо (бутылочно-зеленое стекло). В HCl в порошкообразном состоянии растворяется.
Происхождение и месторождения. Магнетит, в отличие от гематита, образуется в более восстановительных условиях и встречается в самых различных генетических типах месторождений и горных пород.
1. В магматических горных породах он обычно наблюдается в виде вкрапленности. С основными породами (габбро) нередко генетически связаны магматические месторождения титаномагнетита в виде неправильной формы скоплений и жил.
2. В незначительных количествах он присутствует во многих пегматитах в парагенезисе с биотитом, сфеном, апатитом и другими минералами.
3. В контактово-метасоматических образованиях он часто играет весьма существенную роль, сопровождаясь гранатами, пироксенами, хлоритами, сульфидами, кальцитом и другими минералами. Известны крупные месторождения, образовавшиеся на контакте известняков с гранитами и сиенитами.
4. Как спутник магнетит встречается в гидротермальных месторождениях, главным образом в ассоциации с сульфидами (пирротином, пиритом, халькопиритом и др.). Сравнительно редко он образует самостоятельные месторождения в ассоциации с сульфидами, апатитом и другими минералами. Наиболее крупные месторождения этого типа в России известны в Ангаро-Илимском районе Сибири.
5. В экзогенных условиях образование магнетита может происходить лишь в исключительных случаях. Присутствие магнетитовых зернышек в современном морском иле, как полагают, является результатом сноса их с суши в виде не только обломочного материала, но также новообразований на месте за счет гидроокислов железа под восстанавливающим влиянием разлагающихся органических веществ.
6. При региональном метаморфизме магнетит, так же как и гематит, возникает при дегидратации гидроокислов железа, образовавшихся в осадочных породах при экзогенных процессах, но в восстановительных условиях (при недостатке кислорода). К такого рода образованиям относят многие крупные по размерам пластовые залежи гематито-магнетитовых руд, встречающиеся среди метаморфизованных осадочных толщ.
В зоне окисления он является сравнительно устойчивым минералом. При механическом разрушении горных пород он, освобождаясь от своих спутников, повсеместно переходит в россыпи. В черных шлихах, получающихся при промывке золотоносных песков, магнетит является главной частью.
При выветривании он с большим трудом поддается гидратации, т. е. превращению в гидроокислы железа. Этот процесс наблюдается редко и сравнительно в очень небольших размерах.
Явление мартитизации (образование псевдоморфоз гематита по магнетиту) наблюдается в зонах жаркого климата. Локально проявляющаяся мартитизация магнетита устанавливается также в гидротермальных и метаморфизованных месторождениях вне всякой связи с экзогенными процессами.
Из многочисленных месторождений России приведем лишь отдельные примеры.
1. К числу магматических месторождений относится Кусинское месторождение титаномагнетита, содержащего также повышенное количество ванадия (на Урале в 18 км к северу от Златоуста). Это месторождение представлено жилами сплошных руд, залегающими среди материнских измененных изверженных пород габбровой формации. Магнетит тесно ассоциирует здесь с ильменитом и хлоритом. На Южном Урале разрабатывается Копанское месторождение Ti-магнетита.
2. Примером контактово-метасоматических месторождений является известная гора Магнитная (Южный Урал). Мощные магнетитовые залежи располагаются среди гранатовых, пироксено-гранатовых и гранат-эпидотовых скарнов, образовавшихся при воздействии гранитной магмы на известняки. На некоторых участках рудных залежей магнетит ассоциирует с первичным гематитом. Руды, залегающие ниже зоны окисления, содержат вкрапленные сульфиды (пирит, изредка халькопирит, галенит и др.).
К числу таких же месторождений относятся на Урале: гора Высокая (у Нижнего Тагила), гора Благодать (в Кушвинском районе), Коршуновское (в Забайкалье), группа месторождений в Кустанайской области Казахстана (Соколовское, Сарбайское, Куржункуль), а также Дашкесан (Азербайджан) и др.
3. Крупнейшее месторождение Кривой Рог (Украина) относится к числу регионально-метаморфизованных осадочных месторождений. В толще слоистых железистых кварцитов, кроме типичных пластовых залежей, сплошные железные руды представлены также столбообразными залежами с линзовидной формой в поперечном сечении, уходящими на значительную глубину. К числу аналогичных по генезису месторождений относятся: Курская магнитная аномалия (к юго-востоку от Курска). Глубоко метаморфизованные железистые кварциты известны также в месторождениях на Кольском полуострове (Оленегорское) и в Западной Карелии (Костомукша).
Из иностранных отметим крупнейшие месторождения Кирунаваара и Люоссаваара в Швеции, залегающие в виде мощных жилообразных залежей в метаморфизованных толщах вулканитов; магнетит ассоциирует здесь с апатитом. Огромные месторождения магнетито-гематитовых руд США располагаются в районе Верхнего озера среди древнейших метаморфизованных сланцев, в Лабрадоре (Ньюфаундленд) и др.
Практическое значение. Магнетитовые руды, содержащие нередко около 60 % Fe, представляют собой важнейшее сырье для выплавки чугуна и стали. Вредными примесями в руде считаются фосфор, содержание которого при бессемеровском способе плавки не должно превышать 0,05 %, а для качественного металла — 0,03 %, и сера, предельное максимальное содержание которой должно быть не выше 1,5 %. При плавке руд по томасовскому способу, при котором фосфор переводится в шлак, содержание его должно быть не ниже 0,61 и не выше 1,5 %. Получающийся при этом фосфористый шлак носит название томасшлака и используется в качестве удобрения.
При плавке титаномагнетитовых руд из шлаков извлекается ванадий, имеющий большое значение при изготовлении качественных сталей. Пятиокись ванадия используется также в химической промышленности, а как краситель — в керамике и для других целей.
ХРОМШПИНЕЛИДЫ с общей формулой — (Fe,Mg)(Cr,Al,Fe)2O4 характеризуются доминированием хрома в октаэдрических позициях шпинелевой структуры n-типа. Все относящиеся сюда минеральные виды в природе встречаются в одинаковых условиях и по внешним признакам настолько похожи друг на друга, что практически без химического анализа невозможно отличить разные по составу виды. В практике разведочного и горного дела все они называются просто хромитами. По составу различают следующие главные минеральные виды: собственно хромит FeCr2O4 (в чистом виде встречается в метеоритах, в земной коре очень редок), магнохромит MgCr2O4, разновидностями которых являются соответственно алюмохромит Fe(Cr,Al)2O4 и хромпикотит (Mg,Fe)(Cr,Аl)2О4. Впервые хромит был известен акад. Т. Ловицу еще в 1797 г.
Химический состав. Содержание Cr2О3 в наиболее часто встречающихся хромшпинелидах колеблется в весьма широких пределах: от 18 до 62 %, FeO — 0–18 %, MgO — 6–16 %, Al2O3 — 0–33 %, Fe2O3 — 2–30 %. Кроме того, в виде изоморфных примесей иногда присутствуют: TiO2 — до 2 %, V2O3 — до 0,2 %, MnO — до 1 %, ZnO — до нескольких единиц, NiO — до десятых долей, CoO — до сотых долей процента.
Сингония кубическая; гексаоктаэдрический в. с. 3L44L366L29PC. a0 = 8,305. Кристаллическая структура аналогична шпинели. Облик кристаллов. Встречаются в виде октаэдрических мелких кристаллов. Обычно же наблюдаются в округленных или не совсем правильной формы зернах и в сплошных зернистых агрегатах.
Цвет хромшпинелидов черный. В тонких шлифах полупрозрачны или просвечивают густо-красным или коричнево-красным цветом. Лишь богатые FeO и Fe2O3 разности совершенно непрозрачны. Черта бурая, часто — бледная, серо-коричневая, иногда с оливковым оттенком. Блеск полуметаллический до алмазного. N = 2,07–2,16.
Твердость 6–7,5. Спайность отсутствует. Уд. вес 4–4,8. Прочие свойства. Хромшпинелиды, содержащие FeO и Fe2O3, обнаруживают слабые магнитные свойства. Разности, богатые этими компонентами и бедные Cr2О3, сильно магнитны.
Диагностические признаки. Общими отличительными признаками хромшпинелидов являются черный цвет, бурая черта, высокая твердость и реакция на хром. Эти минералы настолько постоянно встречаются в ультраосновных породах (дунитах, перидотитах и серпентинитах), что в полевых условиях по указанным признакам почти безошибочно можно их узнавать.
П. п. тр. не плавятся. Перл буры или фосфорной соли в холодном состоянии изумрудно-зеленый (реакция на хром). В кислотах не растворяются.
Происхождение и месторождения. Хромшпинелиды встречаются почти исключительно в магматических ультраосновных породах (дунитах) как в виде вкрапленности, так и в виде сплошных скоплений большей частью неправильной гнездообразной, линзообразной и столбообразной формы. В ассоциации с ними постоянно наблюдаются зеленоватого цвета серпентин (гидросиликат Mg и Fe), оливин (форстерит) — (Mg,Fe)2SiO4, хромсодержащие хлориты, брусит (придающий некоторым рудам «седой» облик), иногда хромовые гранаты изумрудно-зеленого цвета и др. В некоторых массивах ультраосновных пород с ними парагенетически связаны минералы группы платины и осмистого иридия.
В зоне выветривания хромшпинелиды химически устойчивы. Лишь в условиях жаркого климата они подвергаются окислению и разрушению.
Подавляющее большинство месторождений этих руд в России принадлежит Уралу. На Полярном Урале находится месторождение хромитов Рай-Из. Другое известное месторождение, Сарановское, находится на Северном Урале (в 6 км от ст. Бисер) и представлено крупнопадающими жилообразными телами сплошных хромитовых руд относительно низкого качества (с высоким содержанием железа). Крупное по запасам Аганозерское месторождение магнохромитов расположено в Карелии.
Крупнейшие на территории бывшего СССР месторождения высококачественных хромитовых руд сосредоточены на восточном склоне самой южной части Урала: Донские или Кемпирсайские (в Актюбинской области, Казахстан). Небольших размеров месторождения известны в Закавказье: Шорджинское, Гейдаринское и др. (на восточном берегу оз. Севан и юго-восточнее его в Армении).
Из зарубежных месторождений следует отметить хромитовые месторождения Родезии (Юго-Восточная Африка), Новой Каледонии, Турции, о. Кубы и др.
Практическое значение. Хромитовые руды являются единственным сырьем для выплавки феррохрома, используемого в качестве присадки при выплавке высококачественных специальных сортов хромовых и хромоникелевых сталей. Кроме того, в металлической промышленности имеет большое значение хромирование, т. е. покрытие металлическим хромом различных металлических изделий в целях борьбы с коррозией металла. Некоторая часть хромитовых руд (магнохромиты) идет в химическую промышленность для изготовления различных стойких красок, в кожевенном деле и в приготовлении химических препаратов (хромпиков и др.). Для применения в металлургии магнохромитовые руды требуют добавления железных руд. Низкосортные сплошные руды, бедные Cr2О3 и богатые FeO и Fe2O3, используются также в изготовлении огнеупорных кирпичей.
ГАУСМАНИТ — MnMn2О4. Химический состав. MnO — 62 %, MnO2 — 38 % (Mn — 72 %). Содержит также FeO и Fe2O3.
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр. I41/amd(D194h). а0 = 5,75; с0 = 9,42. Кристаллическая структура того же типа, что и шпинели, но с незначительным тетрагональным искажением. Обычно распространен в виде зернистых агрегатов. Кристаллы встречаются лишь в пустотах. Облик кристаллов близок к октаэдрическому (рис. 155). Угол (001) : (111) — 58°57′, для правильного октаэдра — 54°44′8І). Двойники часты по (112). Весьма характерны полисинтетические двойники, наблюдаемые в полированных шлифах при скрещенных николях в отраженном свете.
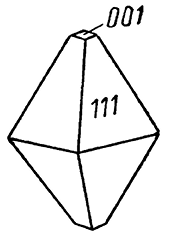
Рис. 155. Кристалл гаусманита
Цвет гаусманита черный. Черта коричневая или красновато-бурая. Блеск у не затронутых окислением кристаллов сильный алмазный или полуметаллический.
Твердость 5. Хрупок. Спайность по {001} довольно совершенная. Уд. вес 4,7–4,9. Немагнитен.
Диагностические признаки. В зернистых агрегатах без микроскопических исследований бывает трудно отличить от других минералов марганца. От браунита отличается меньшей твердостью и по явно красноватой черте. Пиролюзит МnО2 имеет черную черту. Минералы группы псиломелана обладают черной или шоколадно-бурой чертой. От гематита отличим по твердости и по структуре агрегатов.
П. п. тр. не плавится. Перл буры в окислительном пламени окрашивается в фиолетовый цвет. В НСl растворяется с выделением Сl.
Происхождение и месторождения. Гаусманит, аналогично магнетиту, возникает в более восстановительной среде, чем браунит. Он, так же как и браунит, с которым нередко ассоциирует, встречается в некоторых контактово-метасоматических и гидротермальных месторождениях марганца. В тесном парагенезисе с ним обычно наблюдаются минералы, богатые закисью марганца MnO: тефроит (Mn2[SiO4]), манганозит (MnO), родохрозит (Mn(CO3)), марганцовистые гранаты и др. Из нерудных минералов чаще наблюдается барит, но не кварц, с которым обычно ассоциируют браунит и марганцовые силикаты (родонит, бустамит).
В значительных массах гаусманит, также вместе с браунитом, иногда якобситом, магнетитом и другими безводными окислами Mn и Fe, распространен в метаморфизованных осадочных месторождениях марганца (гондитах). В условиях слабого регионального метаморфизма гаусманит образуется в процессе дегидратации гидроокислов марганца, а также в процессе восстановления пиролюзита и браунита. Установлены псевдоморфозы гаусманита по брауниту.
В марганцевых месторождениях России гаусманит как один из главных рудообразующих минералов входит в состав руд Сапальского гидротермального месторождения в мраморизованных известняках (у Нижнего Тагила, Средний Урал). В рудах, кроме того, наблюдаются браунит, магнетит (вероятно, марганцовистый), гематит, родохрозит, сульфиды Fe, железистые хлориты и другие минералы.
В Центральном Казахстане гаусманит встречен в рудах метаморфизованного осадочного месторождения Караджал в ассоциации с браунитом.
В зарубежных странах гаусманит примерно в тех же парагенетических группировках минералов встречается в контактово-метасоматических месторождениях Нордмарк и Лонгбан (Швеция), в жильных месторождениях Ильфельд в Гарце (Германия) и др.
Практическое значение. Гаусманитовые руды, как и браунитовые, используются в черной металлургии для выплавки ферромарганца или для подшихтовки при выплавке чугунов (в зависимости от богатства руд марганцем).
ГАНИТ — ZnAl2O4. Содержит ZnO — 44,3 %, Al2O3 — 55,7 %. Примеси: MgO, FeO, MnO и Fe2O3.
Сингония кубическая; гексаоктаэдрический в. с. а0 = 8,062. Облик кристаллов такой же, как у шпинели. Встречается также в ромбических додекаэдрах и в искаженных кубах. Отдельные кристаллы иногда достигают больших размеров. Двойники образуются по шпинелевому закону, по (111).
Цвет ганита темно-зеленый, серовато-зеленый до черно-зеленого. Черта серая. Полупрозрачен. Блеск стеклянный. N = 1,78–1,82.
Твердость 7,5–8. Хрупок. Спайность по {111} неясная. Уд. вес 4–4,6. Похож на многие другие минералы группы шпинели.
Диагностические признаки. Принадлежность данной шпинели к ганиту можно предположить по повышенному удельному весу, показателю преломления и парагенезису с цинковыми минералами, но без паяльной трубки и химического анализа доказать невозможно.
П. п. тр. не плавится. С содой на угле дает налет ZnO. Кислоты и щелочи не действуют.
Происхождение и месторождения. Встречается сравнительно редко в некоторых пегматитах и контактово-метасоматических месторождениях среди мраморизованных известняков вместе с другими минералами того же происхождения, в том числе цинксодержащими. Отдельные находки относятся также к сильно измененным породам, например тальковым сланцам.
В России ганит известен в скарнах месторождения Солонго (Бурятия), на юго-западе Кольского полуострова (Вуориярви) и в Холоднинском месторождении (Северное Прибайкалье).
Ганит встречен в Алтын-Тау (на северо-востоке Каракалпакии в Узбекистане), в редкометалльных гранитных пегматитах Зеленой Могилы (Западное Приазовье, Украина) и др.
В существенных количествах он наблюдался в известном оригинальном по парагенезису марганцевых и цинковых минералов месторождении Франклин в Нью-Джерси (США) в ассоциации с цинкитом, франклинитом и др. Близ месторождения Фалун (Швеция) он был обнаружен в тальковых сланцах. Встречается также в алмазных россыпях Бразилии.
ФРАНКЛИНИТ — (Zn, Mn)Fe2O4. Сингония кубическая иногда содержит также FeO и Мn2О3. По физическим свойствам во многом похож на магнетит. Непрозрачен. Черта красновато-бурая. Слегка магнитен. Уд. вес 5,07–5,22. N = 2,36. Не плавится. С бурой в окислительном пламени дает красновато-фиолетовое стекло (реакция на марганец). На угле с содой образует налет ZnO. Растворим в НСl, причем в случае содержания Мn2О3 выделяется хлор.
В значительных количествах встречается в известном контактово-метасоматическом месторождении Франклин в Нью-Джерси (США). В ассоциации с ним среди кальцифиров присутствуют: цинкит, виллемит (Zn2[SiO4]), кальцит, реже ганит, аксинит, марганцевые силикаты, апатит и другие минералы.
После минералов семейства шпинели рассматривается минерал, имеющий лишь формульное сходство со шпинелями, но относящийся к вполне самостоятельному структурному типу.
ХРИЗОБЕРИЛЛ — ВеАl2О4. От греч. хризос — золото. Разновидности: хромсодержащий — драгоценный камень I категории александрит изумрудно-зеленой окраски, при рассматривании в свете электрической лампы приобретает фиолетово-красный цвет; цимофан — желто-зеленая разновидность с системой полых микроканалов, приводящих к эффекту «кошачьего глаза».
Химический состав. BeO — 19,8 %, Аl2О3 — 80,2 %. Всегда присутствуют примеси: Fe2O3 (3,5–6 %), иногда TiO2 (до 3 %) и Cr2О3 (до 0,4 %), с чем связана изумрудно-зеленая окраска александрита.
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Пр. гр. Pbnm. а0 = 5,47; b0 = 9,39; с0 = 4,42. Кристаллическая структура. Еще Е. С. Фе-доров, создавая классификацию кристаллов по внешним формам, установил, что хризоберилл по структуре должен быть тождественным минералам группы оливина. Рентгенометрические исследования полностью подтвердили его выводы: расположение ионов в элементарной ячейке совершенно аналогично таковому в форстерите (Mg2[SiO4]). Ионы кислорода расположены фактически по принципу плотнейшей гексагональной упаковки; ионы бериллия, так же как и ионы кремния в форстерите (см. рис. 279), окружены четырьмя ионами кислорода, а ионы алюминия — шестью. Пониженная координация бериллия позволяет считать, что он играет в соединении более кислотную функцию, чем алюминий. Облик кристаллов толстотаблитчатый, иногда коротко- или длиннопризматический. Близкая к гексагональной плотнейшая упаковка ведущих ионов кислорода обусловливает псевдогексагональное отношение осей а и b, поэтому кристаллы по своим углам и развитию граней носят нередко псевдогексагональный облик (рис. 156). Особенно это бросается в глаза (рис. 157) на характерных для александрита тройниках по (130). На гранях {001} часто наблюдается штриховатость параллельно оси а, по которой легко узнать тройниковое срастание индивидов (см. рис. 157). В сплошных зернистых массах хризоберилл до сих пор не наблюдался.
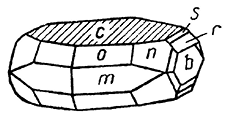
Рис. 156. Псевдогексаго нальный кристалл хризоберилла.
с {001}, o {111}, m {110}, b {010}, n {121}, s {021}, r {031}
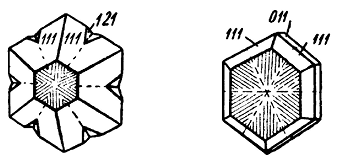
Рис. 157. Тройники прорастания по (130) со штриховкой на гранях {001}
Цвет хризоберилла обычно желтый или зеленовато-желтый, спаржевый; редко бесцветный. Лишь хромсодержащая разность (александрит) обладает изумрудно-зеленой окраской, а при электрическом освещении — фиолетово-красной. Блеск стеклянный, в изломе жирный. Ng = 1,753, Nm = 1,747 и Np = 1,744.
Твердость 8,5. Хрупок. Спайность по {110} ясная, по {001} и {010} несовершенная. Излом раковистый. Уд. вес 3,5–3,84.
Диагностические признаки. Встречается исключительно в кристаллах, весьма характерных по своей форме, существенно отличной от берилла, по высокой твердости и окраске.
П. п. тр. не плавится. В кислотах не растворяется. Разлагается лишь при сплавлении порошка с КОН или KHSO4. Сплав, смоченный азотно-кислым кобальтом, при прокаливании дает характерное синее окрашивание.
Происхождение и месторождения. Этот сравнительно редкий минерал обычно распространен в пегматитах или в контактово-метасоматических образованиях на границе ультрабазитов или базитов с гранитными интрузивами. В зоне окисления весьма устойчив. Встречается в россыпях, иногда в виде окатанных галек. Отдельные экземпляры кристаллов александрита достигают порой нескольких сантиметров в поперечнике.
Самая замечательная среди когда-либо найденных группа из 22 крупных кристаллов и мелких тройниковых сростков александрита хранится в Минералогическом музее им. А. Е. Ферсмана Академии наук РАН в Москве. Хризоберилл обычно наблюдается в ассоциации с изумрудом, полевыми шпатами, апатитом и другими минералами слюдяных, хлоритовых и тальковых сланцев, обычно в контактовых оторочках гранитных пегматитов.
В России хризоберилл (в том числе александрит) с середины XIX в. добывается в Изумрудных копях (Средний Урал) в грейзенезированных серпентинитах, превращенных в бериллиеносные слюдиты. В Карелии (близ г. Кемь) у бывш. хутора Половина спаржево-зеленый хризоберилл образует стрелкообразные двойники в кварце среди хлоритизированного амфиболита на контакте с гранитным пегматитом. В грейзенизированных диопсид-магнетитовых скарнах Люппико (Северное Приладожье) хризоберилл находится с хлоритом, даналитом и флюоритом. Отмечен также в пегматитах Кондаковского месторождения в Енисейском кряже (Красноярский край).
Из иностранных укажем на месторождения в штатах Минас-Жерайс и Байя (Бразилия), где хризоберилл в ассоциации с топазом, горным хрусталем, шпинелью, гранатом, турмалином и другими минералами встречается в пегматитовых жилах среди гнейсов и слюдяных сланцев, а также в россыпях на островах Цейлон и Мадагаскар.
Практическое значение. Красиво окрашенные прозрачные разности употребляются как драгоценные камни, вставляемые в украшения.
В эту группу входят соединения типа АХ2, кристаллизующиеся в тетрагональной сингонии: двуокиси Ti, Sn, Mn, Ge и Pb. Из них TiO2 в природе известна в трех полиморфных модификациях, носящих особые названия, а MnO2 — по крайней мере в двух модификациях. По некоторым данным, и соединение SnO2 является диморфным.
Все относящиеся сюда главные минералы не связаны друг с другом парагенетически и образуются в различных условиях. Двуокись олова отчасти встречается в условиях, аналогичных условиям, при которых образуется TiO2, но в основном при геологических процессах ведет себя все же обособленно. MnO2 и PbO2 образуются в совершенно других условиях, почти исключительно при экзогенных процессах минералообразования.
Замечательной особенностью химического состава рутила (а также брукита и анатаза) является то, что в них в виде изоморфных примесей могут присутствовать Nb5+ и Та5+, но совместно с Fe2+.
Химическая формула для таких разновидностей выражается в следующем виде: Ti3-3хNb2хFe2+хO6. Из этой формулы видно, что два иона Nb5+и один Fe2+ могут заменять три иона Ti4+ с сохранением общего заряда заменяемых ионов: Fe2+ 2Nb5+ > 3Ti4+. Так как размеры ионных радиусов всех этих ионов примерно одного порядка (см. рис. 142), то кристаллическая структура минерала будет оставаться однотипной. Лишь размеры ячейки будут несколько возрастать соответственно размерам ионных радиусов Nb5+, Та5+ и Fe2+ (или Mn2+). Таким образом, богатые танталом разновидности рутила представляют изоморфные ряды TiO2, вернее Ti3O6, идущие в направлении тетрагональных (FeTa2)О6 или (MnTa2)О6 (т. е. минералов, называемых ферротапиолитом и мангантапиолитом), кристаллизующихся в структуре так называемого трирутилового типа (упорядочение металлов приводит к утроению параметра с по сравнению с ячейкой рутила).
Следует указать, что соединение FeTa2O6 диморфно и кристаллизуется как в тетрагональной (ферротапиолит), так и в ромбической (ферротанталит) сингониях. Кристаллическая структура ромбической модификации соединений такого состава (колумбитов и танталитов) является производной от структуры ромбической модификации TiO2 (брукита).
Есть и другой предполагаемый механизм вхождения Nb и Ta в структуру рутила, с компенсацией зарядов трехвалентным железом: Fe3+(Nb5+,Ta5+) → 2Ti4+. В этом случае конечными членами изоморфных рядов для рутилов с Nb, Ta и Fe будут Fe3+NbO4 и Fe3+TaO4.
РУТИЛ — TiO2. Название происходит от лат. rutilus — красноватый. Он является наиболее устойчивой модификацией TiO2 как при высоких, так и при низких температурах.
Химический состав. Ti — 60 %. Химические анализы показывают, что в нем часто присутствуют примеси других элементов: Fe в виде закиси или окиси, иногда Sn4+ (до 1,5 %), изредка Cr3+, V3+ и некоторые другие. Богатая FeTiO3 (в виде твердого раствора) разность называется нигрином. Минеральные виды, сохраняющие неупорядоченный структурный тип рутила и содержащие Nb5+ или Та5+ одновременно с Fe2+ (или Fe3+) в количестве, превосходящем Ti, называются ильменорутилом и стрюверитом соответственно.
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр. P42/mnm(D144h). a0 = 4,58; с0 = 2,95. Кристаллическая структура рутила, как типичная, изображена на рис. 158. Она отличается некоторыми особенностями от ранее разобранных плотноупакованных структур оксидов, таких как корунд. Если в кристаллической структуре типа корунда листы плотнейшей упаковки ионов кислорода располагаются перпендикулярно тройной оси, а в структуре типа шпинели — параллельно граням октаэдра (т. е. также перпендикулярно тройным осям), то в кристаллической структуре типа рутила, как показал Н. В. Белов, направления плотнейшей упаковки в виде колонок параллельны главной (четверной) оси кристаллов рутила. Каждый ион Ti окружается шестью ионами кислорода, располагающимися по углам почти правильного октаэдра.
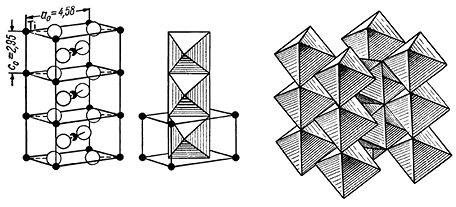
Рис. 158. Кристаллическая структура рутила:
а — в изображении центров ионов (черные кружки — титан, полые — кислород);
по вертикали расположены три элементарные ячейки рутила;
б — в изображении октаэдров TiO6 (центральная колонка)
ионы титана располагаются внутри октаэдров;
в — общий вид структуры в установке с вертикальной
четверной осью (по Н. В. Белову)
Такие октаэдры в кристаллической структуре рутила вытянуты вдоль оси с в виде прямолинейных колонок (рис. 158б), чем и обусловливается игольчатый или шестоватый облик кристаллов с направлениями плоскостей спайности параллельно вытянутости индивидов. Характерно, что в структуре рутила, в отличие от других модификаций TiO2, каждый октаэдр TiO6 имеет по два ребра, общих с соседними октаэдрами (рис. 158б). Поскольку колонки плотно упакованных ионов кислорода, вытянутых вдоль четверной оси рутила, в сущности отвечают одному из трех возможных направлений в плоскости гексагональной плотнейшей упаковки, то не случайно, что для минералов группы рутила мы имеем коленчатой формы двойники и тройники срастания (рис. 160) с углом, образуемым отдельными индивидами, близким к 120° (т. е. соответственно направлениям гексагональной сетки). Таким путем могут возникнуть даже кольцеобразные шестерники. Это же обстоятельство лежит в основе закономерных (под углом 120°) нарастаний тончайших иголочек или призматических кристалликов рутила на базальном пинакоиде {0001} гематита (см. рис. 148), ильменита, слюд и других минералов, грани которых представлены плоскостями плотнейшей упаковки ионов кислорода.
Облик кристаллов рутила чрезвычайно характерен: призматический, столбчатый до игольчатого. Обычные формы: {100}, {110}, {101}, {111}, изредка {001}. Часто наблюдается штриховатость вдоль главной оси с. Типичные формы кристаллов изображены на рис. 159. Очень часты двойники коленчатой формы (рис. 160) с плоскостью срастания (011). Плоские сетчатые (под 60°) сростки двойников игольчатого рутила называют сагенитом. Как было указано, распространены закономерные срастания кристалликов рутила с кристаллами гематита, причем четверная ось рутила совпадает с одной из горизонтальных двойных осей гематита. Игольчатые волосовидные кристаллы рутила иногда наблюдаются в виде пучков, заключенных в прозрачных кристаллах кварца («кварц-волосатик»).
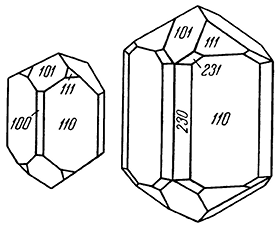
Рис. 159. Кристаллы рутила
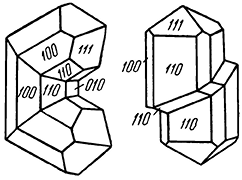
Рис. 160. Двойники рутила
Цвет рутила обычно темно-желтый, серый, бурый, оранжевый, красный и черный (нигрин). Бесцветные или бледноокрашенные разности исключительно редки. Черта желтая, светло-бурая. Блеск алмазный до металловидного (для непрозрачных черных разностей). Ng = 2,903 и Nm = 2,616.
Твердость 6. Хрупок. Спайность по {110} совершенная, по {100} средняя. Уд. вес 4,2–4,3.
Диагностические признаки. Весьма характерны тетрагональные призматического облика кристаллы и коленчатые двойники. Смешать можно с минералами, похожими по облику кристаллов: с цирконом (Zr[SiO4]), обладающим более высокой твердостью (7–8), и касситеритом (SnO2), для которого характерен высокий удельный вес. Волосовидные кристаллы рутила можно принять иногда за турмалин, отличающийся по оптическим константам.
П. п. тр. не плавится и не изменяется. В кислотах не растворяется. С фосфорной солью реагирует на титан (стекло в восстановительном пламени становится фиолетовым).
Происхождение и месторождения. Рутил в природе образуется в различных условиях. Изредка он наблюдается как составная акцессорная часть изверженных пород (сиенитов, реже гранитов). В небольших количествах он встречается в пегматитах и некоторых гидротермальных месторождениях в ассоциации с кварцем, минералами титана и железа (ильменитом, гематитом, магнетитом), иногда с корундом, силикатами и другими минералами. Известны редкие находки его в виде новообразований в экзогенных продуктах разложения титановых минералов, изредка в осадочных породах, а также месторождениях боксита. Однако гораздо чаще он образуется при метаморфических процессах в результате преобразования титансодержащих минералов, выделяясь в виде самостоятельных зерен в гнейсах, слюдяных сланцах, амфиболитах, наждаках и других породах; для эклогитов рутил является индикаторным минералом.
Весьма эффектны его игольчатые и волосовидные кристаллы в жилах альпийского типа, нередко заключенные в кристаллы горного хрусталя и гематита; часто он наблюдается в сопровождении брукита и анатаза.
В зоне окисления химически устойчив и нередко встречается в россыпях в виде окатанных зерен и галек.
В России рутил в виде крупных кристаллов известен в ряде месторождений: в слюдяных сланцах в Слюдоруднике в Вишневых горах, в пегматитовых жилах Ильменских гор, на Приполярном Урале (гора Неройка, Парнук) в жилах альпийского типа и в других местах. Кроме того, он часто встречается в россыпях, особенно на Среднем Урале, в Тиманском крае и в Центральной России. В ближнем зарубежье отмечается в месторождении наждака Семиз-Бугу (Центральный Казахстан) с корундом и в виде прекрасно образованных кристаллов в пустотах кварцевых жил Капуджука (Зангезурский хребет, Армения).
Из иностранных отметим месторождения Северной Каролины (США), где встречаются замечательные кристаллы рутила различного облика.
Практическое значение. Добываемый из комплексных титан-циркониевых россыпей, употребляется для выплавки ферротитана, применяемого в производстве некоторых стойких при ударе сортов стали, в керамике, в качестве бурой краски, в радиотехнике — как детектор, для изготовления титановых белил и др. О применении металлического титана см. ильменит.
БРУКИТ — TiO2. Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Пр. гр. Pabc (D152h). a0 = 9,16; b0 = 5,44; с0 = 5,14. Кристаллическая структура в несколько идеализированном виде представлена на рисунке 161а в проекции на плоскость (100), являющуюся плоскостью плотнейшей гексагональной упаковки ионов кислорода. На рисунке 161б изображены вышележащие (над плоскостью чертежа) слои ионов кислорода (ср. цифры в кружках).
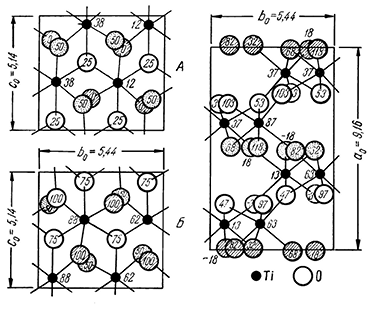
Рис. 161. Кристаллическая структура брукита
(в несколько идеализированном виде):
а и б — два участка структуры в проекции на (100);
нижний располагается над верхним
(ионы кислорода, помеченные цифрой 50, являются общими);
справа — структура в проекции на (001) с действительным
положением ионов кислорода и титана
Если наложить нижний рисунок на верхний, то нетрудно убедиться в том, что в направлении оси а в целом мы имеем комбинацию гексагональной и кубической упаковок (топазовую упаковку): ионы кислорода «75» располагаются не над ионами «25», как следовало бы для плотнейшей гексагональной двуслойной упаковки, а так, как это имеет место в кубических плотнейших упаковках. Ионы Ti лежат между листами ионов кислорода в шестерном окружении, образуя зигзагообразные цепочки октаэдров в каждом слое плотнейшей упаковки. В отличие от структуры рутила эти октаэдры здесь имеют по три общих ребра. В соответствии со структурой находится и уплощенный по (100) облик кристаллов (рис. 162), причем четыре грани призмы (021), параллельной оси α, и пинакоиды {001} образуют почти правильный шестиугольник в разрезе. Изредка встречаются изометричные кристаллы дипирамидального облика (арканзит). Характерна также вертикальная штриховка на гранях.
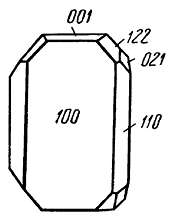
Рис. 162. Кристалл брукита
Цвет брукита желто- или красно-бурый до черного. В тонких пластинах просвечивает. Черта бесцветная до серовато- или буровато-желтой. Блеск алмазный. Ng = 2,741, Nm = 2,586 и Np = 2,583. В некоторых образцах наблюдается очень сильная дисперсия показателей преломления, а в связи с этим меняется положение плоскости оптических осей для разных длин волн.
Твердость 5–6. Спайность по {110} несовершенная. Уд. вес 3,9–4 (меньше, чем рутила, но больше, чем анатаза). При прокаливании он увеличивается и становится равным удельному весу рутила (очевидно, происходит перестройка кристаллической структуры).
Месторождения. Превосходные кристаллы брукита у нас встречаются в Атлянской золотоносной россыпи близ Миасса и в жилах альпийского типа в ряде мест Приполярного Урала (гора Неройка).
АНАТАЗ — TiO2. Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр I41/amd(D194h). a0 = 3,73; с0 = 9,37. Кристаллическая структура характеризуется плотнейшей кубической упаковкой ионов кислорода с вертикальной четверной осью (рис. 163). Координационные числа те же, что для рутила (6 : 3), но геометрические формы координации искаженные. Это обусловливается тем, что октаэдры TiO6 сочетаются друг с другом таким образом, что имеют четыре общих ребра.
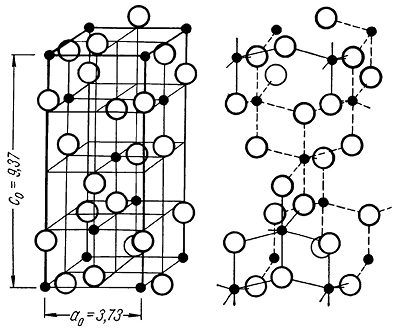
Рис. 163. Кристаллическая структура анатаза:
а — элементарная ячейка, б — связи между Ti и О
Кристаллы обладают характерным дипирамидальным обликом (рис. 164), причем дипирамида {011} острее дипирамиды {012}, близкой по форме к октаэдру. Реже встречаются кристаллы призматической и таблитчатой формы.
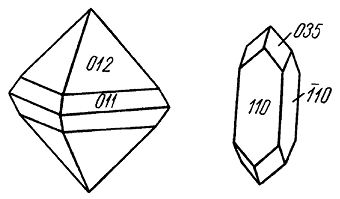
Рис. 164. Кристаллы анатаза
Цвет серый, синий, реже желтый, иногда коричневый, черный. Черта бесцветная. Блеск алмазный. Nm = 2,55 и Nр = 2,49.
Твердость 5–6. Спайность совершенная по {001} и {011}, чем отличается от рутила. Уд. вес 3,9 (меньше, чем рутила и брукита). П. п. тр. не плавится. В кислотах не растворяется.
Встречается в пегматитах и кристаллических сланцах (хлоритовых, слюдяных). Хорошо образованные кристаллы нередко наблюдаются на кварце в жилах альпийского типа в Швейцарских Альпах, Бразилии, на Северном и Приполярном Урале. Минерал химически устойчив, встречается в россыпях — Атлянская россыпь на Южном Урале, около Миасса и в других местах.
КАССИТЕРИТ — SnO2. От греч. касситерос — олово. Синоним: оловянный камень. Касситерит фактически является единственным промышленно важным минералом олова. Химический состав. 78,8 % Sn (по химической формуле). Почти постоянно присутствуют примеси. Во многих случаях, особенно в касситеритах из пегматитовых месторождений, обнаруживаются Fe2O3, Ta2O5, Nb2O5, TiO2, MnO, FeO, изредка ZrO2 и WO3. Все эти разновалентные металлы, подобно тому как это встречается в некоторых разностях рутила, по всей вероятности, присутствуют в виде изоморфных примесей или продуктов распада твердых растворов.
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр. Р42/тпт(D144n). а0 = 4,72; с0 = 3,17. Искусственно ромбические кристаллы SnO2 (с уд. весом 6,7) были получены Добрэ.
Кристаллическая структура идентична структуре рутила. Облик кристаллов. В виде хорошо образованных и сравнительно часто наблюдаемых кристаллов касситерит встречается в пустотах. Кристаллы обычно мелкие, но изредка достигают крупных размеров — до 10 см (несколько килограммов весом). Чаще всего они имеют дипирамидальный, пирамидально-призматический (рис. 165) или столбчатый облик, иногда игольчатый. В пегматитах обычно встречаются кристаллы дипирамидального облика и нередко в виде двойников. Вкрапленные зерна в грейзенах и гранитах часто обладают неправильными очертаниями. Неправильные формы свойственны также зернам касситерита, образовавшимся метасоматическим путем при эндогенном окислении станнина и других сернистых соединений олова. Двойники кристаллов очень часты и, подобно двойникам рутила, имеют коленчатый вид (рис. 166).
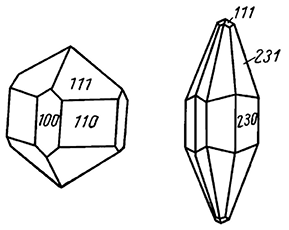
Рис. 165. Кристаллы касситерита
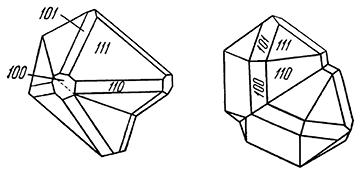
Рис. 166. Двойники касситерита
Агрегаты. Сплошные зернистые массы встречаются редко. Обычно наблюдается в виде вкраплений кристалликов или неправильной формы зерен. В пустотах высокотемпературных гидротермальных жил он иногда обнаруживается в виде друз хорошо образованных кристаллов. Так называемый деревянистый касситерит встречается в виде желваков и концентрически-зональных почковидных и гроздевидных форм; иногда обладает тонким параллельно-волокнистым строением. Под микроскопом в этих случаях нередко можно наблюдать, что отдельные зоны сложены то скрытокристаллическими микроагрегатами, то явнозернистыми, столбчатыми, радиально ориентировочными индивидами.
Цвет. Примесями Fe, Nb, Та и Mn касситерит обычно окрашен в темно-бурые оттенки до смоляно-черного цвета, причем в тонких шлифах часто наблюдается кристаллически-зональное и секториальное строение отдельных кристаллов и зерен, обусловленное чередованием зон с различной степенью интенсивности окраски. Совершенно бесцветные разности очень редки. На крупных кристаллах зональность от черного и бурого до почти бесцветного может наблюдаться невооруженным взглядом. Черта у темных разностей обычно слабоокрашенная в буроватые оттенки. Блеск алмазный, в изломе — смоляной, слегка жирный. Грани кристаллов иногда матовые. Непрозрачные черные разности обладают даже полуметаллическим блеском. Ng = 2,09 и Np = 1,99. Одноосный. Иногда встречающиеся оптически двуосные разности, возможно, обладают кристаллической структурой, близкой к ромбической, но скорее всего аномальная двуосность вызвана внутренними напряжениями, возникшими в связи с резкой зональностью.
Твердость 6–7, наиболее мягкие — темноокрашенные разности. Хрупок. Спайность несовершенная, иногда ясная по {110}. Излом часто раковистый. Уд. вес 6,8–7. Прочие свойства. Немагнитен. Черные разности, обогащенные железом, все же обладают электромагнитными свойствами.
Диагностические признаки. По форме кристаллов, двойникам и цвету похож на рутил, а светлоокрашенные разности — также на циркон. Существенно отличается от них по удельному весу, твердости (у циркона 7–8) и характерному слегка жирному или смоляному блеску в изломе и сильному алмазному на гранях. В тонких шлифах мелкие зерна касситерита можно принять за циркон, двупреломление у которого значительно ниже.
П. п. тр. не плавится, но с тремя объемами соды на угле, при быстром дутье, в резко восстановительном пламени получаются мелкие ковкие корольки олова и белый налет SnO2. Кислоты не действуют. Если положить на касситерит каплю HCl и прикоснуться к нему кусочком цинка (или лучше специально изготовленной цинковой иглой), то через некоторое время под восстанавливающим влиянием бурно выделяющегося водорода на нем образуется металлический налет олова, блестящий после протирки на сукне (очень характерная для касситерита, почти всегда удающаяся реакция «оловянного зеркала»).
Происхождение и месторождения. Месторождения касситерита генетически связаны с кислыми изверженными породами, преимущественно гранитами.
В самих гранитах касситерит устанавливается очень редко, и то главным образом в грейзенизированных участках, т. е. превращенных под влиянием пневматолитовых агентов (F, Cl, В и др.) в слюдисто-полевошпато-кварцевую породу с топазом, флюоритом, цинвальдитом (литиевой слюдой), турмалином и другими минералами. Полагают, что при высоких температурах олово переносится в виде летучих соединений SnF4 и SnCl4, которые впоследствии гидролизуются с выпадением SnO2. Установлено также, что щелочные растворы, содержащие сероводород, в восстановительной среде весьма активны в отношении переноса олова.
Очень неравномерно распространенные скопления касситерит образует в пегматитовых жилах, связанных с оловоносными интрузиями. Касситерит, в отличие от гидротермальных месторождений, часто содержит Nb, Та, Fe и другие металлы. В парагенезисе с ним присутствуют: кварц, слюды, альбит, турмалин, иногда колумбит, берилл, сподумен и т. д. Касситерит встречается также в некоторых контактово-метасоматических месторождениях в тесной ассоциации с различными сульфидами, что указывает на отложение его в гидротермальную стадию процесса.
Жильные гидротермальные месторождения касситерита являются гораздо более важными в промышленном отношении. Из них главное значение имеют типы жил: 1) кварцево-касситеритовые; 2) сульфидно-касситеритовые. В первом типе, кроме преобладающего кварца и касситерита, обычно присутствуют: турмалин, белая слюда, полевые шпаты, вольфрамит, в небольших количествах арсенопирит, пирит, иногда флюорит, топаз, берилл и другие минералы. Касситерит встречается главным образом вкрапленным в кварцевую массу и в пустотах в виде кристаллов, иногда достигающих крупных размеров. Во втором типе месторождений, имеющих важное значение в ряде районов России, касситерит ассоциирует преимущественно с сульфидами: в одних случаях главным образом с пирротином и отчасти со сфалеритом, халькопиритом, станнином; в других — преимущественно со сфалеритом и галенитом и, наконец, в третьих — с малораспространенными различными сульфидами, среди которых видную роль играет висмутин (боливийский тип). Из нерудных минералов, кроме кварца, в существенных количествах встречаются черные турмалины, очень часто железистые хлориты и карбонаты.
В зонах окисления оловорудных месторождений касситерит исключительно устойчив. Этим объясняется его нахождение в россыпях.
Касситерит экзогенного происхождения, образующийся при разрушении сульфидов олова, в виде пористых и землистых масс встречается в зонах окисления.
На территории России месторождения касситерита распространены главным образом в Восточной и особенно в Северо-Восточной Сибири.
Укажем на некоторые наиболее типичные примеры месторождений различных формаций.
1. Представителем оловоносных пегматитов является Завитинское месторождение (к юго-востоку от оз. Байкал, в районе слияния pек Ингоды и Онона), где они залегают в краевых частях гранитного массива. Пегматитовые жилы здесь местами сильно изменены пневматолитовыми процессами, обусловившими оруденение. Измененные (грейзенизированные) участки их содержат розовый турмалин, лепидолит, гранат, касситерит и зеленый турмалин.
2. К числу контактово-метасоматических месторождений из находящихся в России относятся мелкие месторождения в Питкяранте (Южная Карелия), где касситерит наблюдался с сульфидами меди и железа в кварц-карбонат-диопсид-гранатовых скарнах. К этому типу относятся месторождения Такфонское и Майхура в Зеравшанском хребте (Средняя Азия, Таджикистан), где среди скарновых образований с пирротином, арсенопиритом и халькопиритом встречаются касситерит, станнин и висмутин.
3. Примером кварцево-касситеритовой формации является Ононское месторождение (ст. Онон, Забайкалье), где имеется ряд ветвящихся кварцевых жил, пересекающих осадочные породы. Руды представлены здесь кварцевыми массами, в которых касситерит ассоциирует с белой слюдой, топазом, флюоритом, арсенопиритом, пиритом и другими минералами. К этому же типу относятся многочисленные месторождения Кавалеровского рудного района в Приморье, месторождения Иультин на Чукотке и Бутугычаг в верховьях Колымы.
4. К касситерито-сульфидным месторождениям относятся Хапчерангинское (Восточное Забайкалье) и Восток-2 (Приморье). Касситерит ассоциирует в них с различными сульфидами: арсенопиритом, пирротином, сфалеритом, вюртцитом, галенитом, халькопиритом, а также железистыми хлоритами, карбонатами и кварцем.
5. Гидротермальные месторождения с колломорфным касситеритом, образовавшиеся в близповерхностных условиях, представлены Джалиндинским и другими месторождениями в Восточной Сибири. Касситерит обычно ассоциирует с кварцем, нередко гематитом, иногда флюоритом, топазом и др.
Из месторождений зарубежных стран большой известностью пользуется Малайская оловоносная провинция (Бирма, Западный Таиланд, весь Малайский полуостров и южные острова — Бангка, Биллитон и др.), где широко распространены крупные касситеритсодержащие россыпи, образующиеся при разрушении коренных (главным образом пегматитовых и кварцево-касситеритовых) жил. В пегматитах Туркестанского хребта (Таджикистан) находится с кварцем, альбитом и лепидолитом. Великолепные кристаллы и двойники наблюдаются в пустотах кварцевых жил в топаз-цинвальдитовых грейзенах (цвиттерах) в Хорни Славков в Рудных горах (Чехия). В Боливии распространены кварцевые жилы с касситеритом, вольфрамовыми минералами, различными сульфидами, флюоритом и турмалином, а также сульфидно-касситеритовые месторождения.
Практическое значение. Касситеритовые руды представляют собой единственный вид сырья, из которого в промышленных масштабах добывается олово. Последнее имеет следующие применения: 1) для производства белой жести; 2) для легкоплавких, трудноокисляемых сплавов с медью (бронзы), цинком, медью и свинцом (латуни), припоя (со свинцом) и др. 3) для лужения медной посуды; 4) для изготовления оловянной фольги (станиоля); 5) в керамике (для красок, эмали) и для других целей.
8. Группа колумбита — танталита
Сюда включаются сложные оксиды с составами, отвечающими формулам вида АВ2O6 и (B,A)O2, где А — Fe2+, Mn2+, Mg, иногда Fe3+; B — Nb, Ta, иногда Ti, W и Sn. Здесь будут совместно рассмотрены минералы группы колумбита — АВ2O6 и их разупорядоченные аналоги (B, A)O2.
КОЛУМБИТ-ТАНТАЛИТ. В группе колумбита насчитывается шесть минеральных видов. Ферроколумбит FeNb2O6 образует непрерывные изоморфные ряды по первой позиции до манганколумбита MnNb2O6 и по второй позиции до ферротанталита FeTa2O6, по обеим позициям — до мангантанталита MnTa2O6; между двумя последними видами существует разрыв смесимости. Известны также чрезвычайно редкие магнотанталит MgTa2O6 и магноколумбит MgNb2O6. Название ниобиевых видов происходит от старого американского названия элемента ниобия — колумбий; остальных — по составу.
Из разупорядоченных аналогов известны иксиолит (Ta, Nb, Sn, Fe, Mn, W)O2 и ашанит (Nb, Ta, Fe, Mn)O2.
Химический состав очень непостоянный. Даже в одном и том же месторождении содержания Fe и Mn, так же как и содержания Nb и Ta, колеблются в широких пределах. Любопытно, что танталиты встречаются либо почти чисто марганцовистые, либо чисто железистые (промежуточные разности редки). Иногда в незначительных количествах содержат примеси Sn (до 1–2 %, реже до 9 % в танталитах и часто — в иксиолите), W и Ti. Однако в отличие от других тантало-ниобатов в них отсутствуют примеси таких крупных катионов, как Na, Ca, U, Th, редкие земли и иттрий.
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L33PC. Пр. гр. Pbcn (D142h). a0 = 5,08; b0 = 14,24 (у разупорядоченных b0 = 4,75); с0 = 5,73. Кристаллическая структура производная от структуры брукита (см. рис. 161). В упорядоченных структурах ионы Nb, Та и Sn занимают октаэдрические позиции на местах Ti в двух слоях пустот плотнейшей упаковки кислорода, далее следует слой Mn, Fe, W (также в октаэдрах); период такой катионной укладки в три слоя приводит, в сочетании с двухслойной упаковкой кислорода, к полному повторению структуры лишь на шестой слой. При разупорядочении катионные слои теряют различия и повторение наступает, как и у брукита, через два слоя, что понижает параметр решетки b0 втрое по сравнению с этим параметром упорядоченных фаз. Облик кристаллов пластинчатый по (010), таблитчатый, иногда короткостолбчатый (рис. 167). Наиболее обычные формы: пинакоиды {100}, {010}, {001}, призма {110}, дипирамида {111} и др. Двойники наблюдаются по (201), нередко пластинчато-сердцевидные и характеризующиеся перистой штриховкой (рис. 168). Описаны закономерные срастания колумбита с самарскитом.
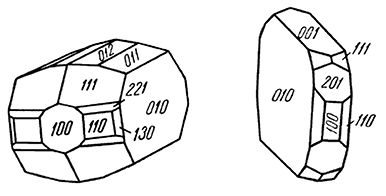
Рис. 167. Кристаллы колумбита
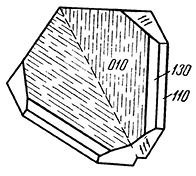
Рис. 168. Двойник колумбита
Цвет черный или буровато-черный до светлого оранжево-красного (мангантанталит и магнотанталит). Черта бледная желто-красная или красновато-бурая (у танталитов) до красновато-черной и коричневой до серой с оливковым оттенком. Блеск полуметаллический у колумбитов до алмазного у танталитов. Непрозрачны, за исключением просвечивающих мангантанталита и магнотанталита.
Твердость 6. Хрупкие. Спайность по {100} довольно ясная, излом зернистый. Уд. вес 5,15–8,2, увеличивается по мере увеличения содержания Ta (рис. 169). Прочие свойства. Колумбит является проводником электричества, железосодержащие минералы группы могут проявлять слабую магнитность.
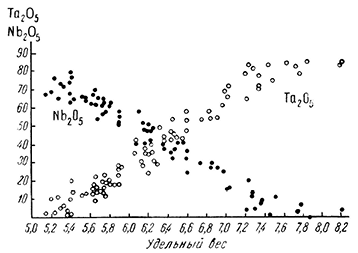
Рис. 169. Зависимость между содержанием Та2О5
и Nb2О5 и удельным весом колумбитовтанталитов (по А. И. Гинзбургу)
Диагностические признаки. По внешним признакам распознать колумбит и танталит очень трудно. Их можно смешать: 1) с ильменитом (отличие по цвету черты, облику кристаллов и отрицательным реакциям на Nb и Ta); 2) с вольфрамитом, обладающим более совершенной спайностью по {010} и меньшей твердостью; 3) с ортитом, имеющим меньший удельный вес (3,2–4,2) и светлую черту; 4) с самарскитом, эшинитом, эвксенитом и другими ниобатами и танталатами, содержащими редкие земли и радиоактивные элементы, от которых без данных спектрального и радиометрического анализа, а также микрохимических реакций отличить их трудно, тем не менее большинству из названных минералов, в отличие от колумбитов, свойствен раковистый излом и смоляной блеск.
П. п. тр. не плавятся. В кислотах нерастворимы. Колумбит после сплавления с КОН и обработки разбавленной НСl и H2SO4 при прибавлении металлического Zn дает устойчивую синюю окраску. Танталит после сплавления с KHSO4 и обработки НСl дает желтый раствор и тяжелый белый осадок, также приобретающий ярко-синий цвет при прибавлении Zn; однако при разбавлении водой синяя окраска исчезает.
Происхождение и месторождения. Обычно встречается в редкометалльных пегматитовых жилах в ассоциации с различными минералами, образующимися в более поздние стадии пегматитового процесса: альбитом, кварцем, мусковитом, турмалином, бериллом, эльбаитом, цирконом, вольфрамитом, касситеритом, иногда самарскитом, монацитом и др.
Будучи относительно устойчивыми в зоне окисления минералами, они встречаются в россыпях.
В России ферроколумбит и иксиолит известны на месторождениях Елаш (Восточный Саян) и Вишняковское в Иркутской области, в копях пегматитов Ильменских гор (Южный Урал). Ферроколумбит отмечается также в месторождениях Бирая (Патомское нагорье) и Томтор (Анабарское плато), где распространен в корах выветривания карбонатитового массива. Мангантанталит и ферроколумбит, совместно с кварцем, альбитом, сподуменом, лепидолитом и эльбаитом, отмечается в пегматитах Вороньих тундр (Кольский полуостров). Манганколумбит обнаружен в редкометалльно-слюдоносном пегматите Пиртима (Северная Карелия) с кварцем, мусковитом, альбитом и амазонитом и в месторождении Улугтанзек в Туве с везувианом и криолитом. Магноколумбиты выявлены в жильных карбонатитах Вишневых гор (Южный Урал). Магнотанталит находится в редкометалльных пегматитах Липовки (Средний Урал) с альбитом, кварцем, петалитом, лепидолитом и эльбаитом, также он был зафиксирован в россыпи р. Санарки (Южный Урал).
Ферротанталит проявлен в Огневке в Калбинском хребте (Восточный Казахстан). Мангантанталит с кварцем, альбитом, эльбаитом, лепидолитом находится в пегматитовых жилах Мургабского района на Восточном Памире (Таджикистан) и в пегматитовых полях Нуристана (Северный Афганистан). Из других иностранных месторождений также известны: месторождение около Мосса, Крагерё и Финбо (Норвегия), месторождения около Лиможа (Франция), а также месторождение Ивигтут (Гренландия), где встречены прекрасно образованные кристаллы, и др. Особого упоминания заслуживают богатые по запасам месторождения плато Джос (Нигерия, Африка), связанные с развитием мощной коры выветривания по гранитам с высоким содержанием акцессорного колумбита.
Практическое значение. В случае значительных скоплений этих минералов они могут иметь промышленное значение как источник ниобия и тантала, используемых в производстве особых сортов сталей и для других целей.
ПИРОЛЮЗИТ — MnО2. От греч. пирос — огонь, люзиос — уничтожающий (употребляется в стеклоделии для уничтожения зеленого оттенка стекла). Синоним: полианит (так называли явнокристаллические разности).
Химический состав. Mn — 63,2 %. В тонкозернистых и скрытокристаллических массах, обычно в виде механических примесей, присутствуют: Fe2O3, SiO2, Н2О и т. д.
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Пр. гр. Р42/тпт(О144h). а0 = 4,38; с0 = 2,85. Кристаллическая структура аналогична структуре рутила. В кристаллах встречается редко (только в пустотах). Они имеют игольчатый или шестоватый облик. Пиролюзит обычно наблюдается в сплошных кристаллических или скрытокристаллических, часто порошковатых, сажистых массах, частью в псевдоморфозах по почковидным агрегатам псиломелана.
Цвет пиролюзита стально-серый, в дисперсных массах — черный. Иногда синеватая металлическая побежалость. Черта черная. Блеск металлический до полуметаллического. Непрозрачен.
Твердость у кристаллических индивидов 5–6; в агрегатах снижается до 2 (в зависимости от пористости и рыхлости). Очень хрупок. Спайность совершенная по {110}, весьма характерна для пиролюзита. Уд. вес 4,7–5.
Диагностические признаки. От других черных марганцевых минералов, обладающих черной чертой, отличается сильным блеском, характерной для него спайностью, хрупкостью и сравнительно низкой твердостью.
П. п. тр. не плавится. Выделяя часть кислорода (до 12 % весовых), переходит в низшие окислы и буреет. При нагревании до 500 °С не изменяется, в интервале 550–650 °С, как установлено рентгенометрическими исследованиями, происходит диссоциация с образованием β-браунита (кубической модификации); при дальнейшем нагревании при температурах 940–1100 °С β-браунит переходит в устойчивый при высоких температурах гаусманит.
В НСl растворяется с выделением хлора. Это явление широко используется в химической промышленности. С бурой и фосфорной солью в окислительном пламени дает фиолетовое стекло; при восстановлении оно становится бесцветным.
Происхождение и месторождения. Сравнительно редко образуется в гидротермальных месторождениях марганца, и лишь при условии явно окислительной среды, зато широко распространен на земной поверхности как высший природный окисел марганца в прибрежных фациях осадочных месторождений. Является наиболее устойчивым окислом марганца в зоне окисления. В этих условиях в конце концов в него переходят все марганцевые минералы, содержащие марганец в низших степенях окисления. Поэтому нередки псевдоморфозы пиролюзита по манганиту, вернадиту, псиломелану, гаусманиту и др. Вследствие своей хрупкости в россыпях наблюдается крайне редко. Постоянно встречается во всех так называемых марганцевых шляпах, т. е. в зонах окисления, а также в ряде осадочных месторождений.
На территории России известен в Сапальском (Средний Урал), Полуночном (Северный Урал) и Мозульском (Красноярский край) месторождениях. Из числа крупнейших в мире осадочных месторождений на территории ближнего зарубежья необходимо отметить Чиатурское (Грузия), в котором пиролюзит слагает оолитовые стяжения (рис. 170) и, кроме того, в виде скрытокристаллических мягких агрегатов образует псевдоморфозы по оолитам манганита (на выходах пластов на поверхность), Никопольское (Украина), где он иногда слагает более крупные шаровидные конкреции с концентрически-зональным строением (обычно в псевдоморфозах по манганиту).

Рис. 170. Оолиты пиролюзита с порошковатым
родохрозитом в интерстициях (Чиатури, Грузия)
Из иностранных месторождений следует отметить зоны окисления метаморфизованных месторождений Индии, Золотого Берега (Западная Африка) и др. Хорошо образованные кристаллы были установлены в месторождении Платген (Чехия).
Практическое значение. Чисто пиролюзитовые руды используются для самых различных целей: 1) в производстве сухих электрических батарей; 2) в изготовлении для той же цели искусственно активированных продуктов; 3) в стекольном деле для обесцвечивания зеленого стекла; 4) при изготовлении химических препаратов, употребляемых в медицине и для других целей; 5) в производстве специальных противогазов для защиты от окиси углерода, катализаторов типа гопкалита для очистки от вредных примесей выхлопных газов автомобильных двигателей и пр.; 6) в технике при производстве олифы, масел, воска, в кожевенном деле при выделке хромовой кожи, в фотографии, в производстве красок и т. д. Для целей производства сухих батарей содержание двуокиси марганца в руде должно быть не ниже 80 %.
Перовскит (CaTiO3) по химической формуле вполне тождествен ранее рассмотренному ильмениту, кристаллизующемуся в структуре, типичной для корунда, но существенно отличается по кристаллической структуре. Это обусловлено тем, что ион Са2+ обладает значительно большим радиусом, чем ионы Mg2+, Fe2+ и Мn2+.
Последнее обстоятельство отражается и на ассоциации элементов, входящих в минералы группы перовскита.
Прежде всего, в виде изоморфных аналогов Са в некоторых минералах встречаются трехвалентные редкие земли: Се, La, а также Y, что вполне естественно (при условии замены Ca2+ на равновеликие ионы Na1+).
Затем, точно так же как и в группе рутила, Ti4+ частично или в значительной мере может заменяться Nb5+ или Та5+, но при условии, что общий заряд всех катионов не будет нарушен, т. е. вместо Са2+ мы тогда должны иметь одновалентные катионы. Действительно, в этих случаях в виде изоморфной примеси к Са2+ появляется равновеликий ион Na1+. При этом кристаллическая структура соединения сохраняется. Например, луешит NaNbO3 обладает той же кристаллической структурой, что и перовскит; места Са2+ занимаются Na1+, а на местах Ti4+ располагаются ионы Nb5+. В небольших количествах в виде изоморфной примеси к Са иногда присутствует U4+ и Th4+.
ПЕРОВСКИТ — CaTiO3. Назван так в честь графа Л. А. Перовского (1792–1856), минералога-любителя.
Химический состав. CaO — 41,1 %, TiO2 — 58,9 %. В незначительных количествах в виде примеси присутствуют Fe (до 2 %), иногда Cr, Al, Nb (дизаналит) и TR (кнопит).
Сингония по внешним формам кубическая. Однако оптически обычно анизотропен и характеризуется миметическим строением и двойниковыми решетками на гранях, что свидетельствует о его превращении в более низкотемпературную ромбическую модификацию (из минералов группы лишь таусонит SrTiO3 обладает кубической симметрией). Кристаллическая структура, идеализированная, изображена на рис. 171. В центре куба располагается Са, по вершинам Ti и в серединах ребер О. Титан при этом находится в октаэдрической координации; связанные вершинами октаэдры [TiO6] образуют каркас состава TiO3, отвечающий структуре синтетического ReO3, но заряженный отрицательно. В кубооктаэдрических пустотах каркаса находятся компенсирующие его заряд катионы кальция. Как показал Н. В. Белов, в кристаллической структуре перовскита, построенного по принципу плотнейшей упаковки, катионы кальция, будучи относительно крупными по своим размерам, сами принимают участие в плотнейшей укладке анионов кислорода. При этом характерно, что в разрезе вдоль (001) ионы О2– и ионы Са2+ в шахматном порядке чередуются друг с другом, подобно тому как это мы имеем в структуре NaCl. В этом случае становится понятным, почему кристаллы перовскита обладают кубической формой и спайностью по кубу.
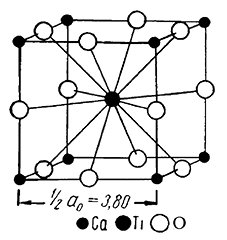
Рис. 171. Кристаллическая структура перовскита
Облик кристаллов. Нередко встречающиеся кристаллы, иногда довольно крупные, имеют кубический облик. На гранях куба наблюдаются штриховки параллельно ребрам куба (рис. 172), являющиеся, по-видимому, результатом двойникования при превращении в ромбическую модификацию. Встречается также в почковидных образованиях, в которых различимы мелкие кубики.
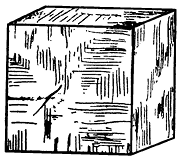
Рис. 172. Кристалл перовскита
Цвет перовскита серовато-черный, красновато-бурый, оранжево-желтый и светло-желтый. Черта белая или серовато-желтая. Блеск алмазный. N = 2,34.
Твердость 5,5–6. Спайность по кубу ясная до средней. Уд. вес 3,97–4,04.
Диагностические признаки. Очень характерен кубический облик кристаллов, грани которых покрыты перпендикулярно ориентированными короткими штрихами (параллельно ребрам). От других похожих на него по цвету и твердости минералов отличается очень слабо окрашенной или белой чертой.
П. п. тр. не плавится. Разлагается только кипящей H2SO4 или после сплавления с KHSO4.
Происхождение и месторождения. Крупных скоплений перовскит обычно не образует. В виде вкраплений он встречается в некоторых щелочных базальтах (мелилитовых, лейцитовых и др.), иногда в титаномагнетитовых и хромитовых месторождениях. Хромсодержащий перовскит встречен в Сарановском хромитовом месторождении (Урал). Лучшие находки кристаллов перовскита были сделаны в оригинальных по происхождению (в связи с основными изверженными породами) контактово-метасоматических месторождениях Назямских и Шишимских гор в Златоустовском районе (Урал) — в известных Ахматовской, Николае-Максимилиановской, Мельниковской и других копях, весьма интересных по парагенетическим группировкам минералов: эпидот, клинохлор, магнетит, хондродит, Ti-клиногумит, хёгбомит и др. Особенно крупные кристаллы перовскита встречались в Мельниковской копи в виде метакристаллов в хлоритовых сланцах и мраморизованных известняках. Они образовались также в полых трещинах в ассоциации с кристаллами хлорита, магнетита, титанита, гранатов и других минералов. С магнетитом, титанитом, кальцитом и эгирин-диопсидом крупные октаэдрические кристаллы перовскита находятся в клинопироксенитах щелочно-ультраосновного массива Африканда (Кольский полуостров). Обогащенный ниобием перовскит (дизаналит) встречен в карбонатитовых жилах на горе Моговид близ Ковдора (запад Кольского полуострова). Присутствует в карбонатитах Тажеранского щелочно-ультраосновного комплекса (Прибайкалье). Перовскит распространен и в ряде иностранных месторождений, из которых упомянем месторождения долины Церматт (Швейцария).
Самостоятельного практического значения не имеет, кроме ниобийсодержащего дизаналита.
ЛОПАРИТ — (Ce,Na,Ca)(Ti,Nb)O3. Впервые описан И. Г. Кузнецовым на Кольском полуострове и назван в честь русского наименования коренного населения полуострова — лопари.
Химический состав непостоянный. Согласно имеющимся анализам, содержит (в %) TiO2 — 39,2–40, TR2O3 — 32–34, (Nb,Ta)2O5 — 8–10, CaO — 4,2–5,2, Na2O — 7,8–9, SrO — 2–3,4, К2О — 0,2–0,7, UO2 в сотых долях, TiO2 — 0,2–0,5, SiO2 0,2–0,7, а в измененных разностях, кроме того, Н2О — до 3,5 %.
Сингония кубическая (вероятно, ромбический псевдокубический); гексаоктаэдрический в. с. 3L44L366L29PC. Кристаллическая структура подобна структуре перовскита. Облик кристаллов. Лопарит встречается преимущественно в виде кубических кристаллов, иногда притупленных гранями {111} (рис. 173), обычно очень мелких (1–2 мм, изредка достигающих 1,5 см в поперечнике). Эти кристаллы почти всегда сдвойникованы по флюоритовому закону (рис. 174).
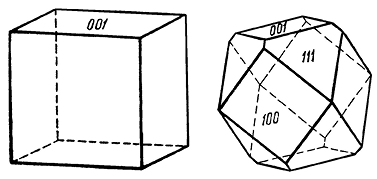
Рис. 173. Кристаллы лопарита
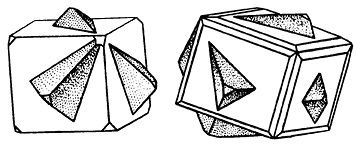
Рис. 174. Двойники лопарита
Цвет лопарита черный или серовато-черный. Черта коричнево-бурая. Блеск полуметаллический. В тонких шлифах просвечивает буровато-красным цветом. N = 2,24. Наблюдаются оптические аномалии.
Твердость 5,5–6. Спайность отсутствует. Излом неровный. Уд. вес 4,75–4,89.
Диагностические признаки. Кроме цвета, черты и твердости весьма характерны двойники прорастания по флюоритовому закону, слабая радиоактивность.
П. п. тр. не плавится. Порошок лопарита с содой на угле сплавляется с трудом. Раствор сплава в НСl при кипячении с оловом окрашивается в фиолетовый цвет (реакция восстановления титана); затем появляется голубая окраска (реакция на ниобий). В присутствии олова перл фосфорной соли в восстановительном пламени имеет желтый цвет; по охлаждении окрашивается в фиолетовый цвет (реакция на титан). В кислотах не растворяется. Разлагается вполне HF. Легко сплавляется с KHSO4.
Происхождение и месторождения. Лопарит известен как второстепенный минерал щелочных магматических пород. Он встречается также во многих пегматитовых жилах, связанных с щелочными породами в виде сконцентрированных вкраплений или включений мелких кристалликов в полевых шпатах, эвдиалите (силикат натрия и циркония сложного состава) и других минералах. В парагенезисе с ним обычно встречаются полевые шпаты (микроклин, альбит), нефелин, эгирин, эвдиалит, титанит и некоторые другие минералы. Кристаллы лопарита, особенно крупные, часто содержат включения окружающих минералов; они развились метасоматическим путем, т. е. являются метакристаллами.
В виде более или менее равномерно рассеянных кристалликов он распространен в малиньитах — темных мелкозернистых обогащенных эгирином (NaFe[Si2O6]) и калишпатом нефелиновых сиенитах Ловозерских тундр (Кольский полуостров); здесь малиньиты слагают значительные по площади горизонты и даже при малой мощности обеспечивают запасы Nb на многие годы вперед. Известен и в щелочных сиенитах массива Коргередаба (Тува).
Практическое значение. Лопарит представляет интерес как источник ниобия, редких земель, тантала, титана и других элементов. Ниобий в виде феррониобия в последнее время приобрел большое значение в металлургии качественных сталей и в изготовлении жароупорных сплавов с алюминием, никелем и другими металлами. Добавка феррониобия к сталям придает им ряд замечательных свойств: 1) предохраняет их от воздушной закалки; 2) повышает упругость и гибкость; 3) значительно улучшает сварочные свойства, придает свойства жароупорности, кислотоупорности и пр. Из ниобиевых (так же как и из танталовых) сплавов важное значение получили сверхтвердые сплавы высокого качества для изготовления буров, сверл, пилок, применяемых при резке твердых сталей, а также в производстве часовых пружин. Кроме того, ниобий и тантал употребляются для изготовления нитей в специальных электрических лампах. Тантал применяется также в электронике при изготовлении мощных радиоламп, как заменитель платины, иридия и др. О применении редких земель см. монацит.
Здесь объединены минералы, хотя и близкие по химическому составу к группе перовскита, но отличающиеся по химическим формулам, в частности по наличию дополнительных анионов. Из многочисленных представителей этой группы опишем пирохлор и микролит и, кроме того, здесь же опишем эшинит и самарскит.
ПИРОХЛОР — (Na,Ca...)2(Nb,Ti...)2O6[F,OH,O], МИКРОЛИТ — (Na,Ca...)2(Ta, Nb, Ta, Ti...)2O6[F,OH]. Название образовано от греч. пирос — огонь, хлорос — зеленый (некоторые разновидности перед паяльной трубкой становятся желтовато-зелеными).
Разновидности, обогащенные ураном и торием и находящиеся в метамиктном состоянии, содержат значительные количества Н2О (7–14 %), лишены щелочей и несколько обеднены окисью кальция, при этом титан в своей позиции обычно доминирует (этому случаю соответствует минеральный вид бетафит). В метамиктных разностях сохраняются внешние кубические или октаэдрические формы кристаллов, иногда с кривоплоскостными гранями, как бы оплавленными.
Химический состав очень непостоянный. Содержания отдельных компонентов вообще для изоморфного ряда пирохлор — микролит колеблются (в %) в следующих пределах:
|
Nb2O5 … 63–0; |
Na2O … 1–6; |
(Ce,La)2O3 … 2–13,3; |
|
Ta2О5 … 0–77; |
K2O … 0–1,4; |
(Y, Er)2O3 … 0–5,1; |
|
TiO2 … 2–13,5; |
CaO … 4–18,1; |
SnO2 … 0–4; |
|
ThO2 … 0–5; |
MnO … 0–7,7; |
ZrO2 … 0–5,7; |
|
UO2 … 0–11,4; |
FeO … 0–10; |
WO3 … 0–0,3; |
|
UO3 … 0–15,5; |
Fe2O3 … 0–9,7; |
H2O … 0–6. |
Кроме того, иногда присутствуют: Sb2O5, MgO, PbО (очевидно, как продукт радиоактивного распада), HfO2, SiO2, Al2O3, SrO, BeO, CuO, Bi2O3, GeO2 и др.
Как видим, главные изменения в химическом составе этих минералов выражаются в колебании содержаний Nb2O5 и Та2О5. Выделяется большое число редких минеральных видов по доминирующим атомам во внекаркасной позиции, таким как Ba, Sr и Pb.
Сингония кубическая; гексаоктаэдрический в. с. 3L44L366L29PC. Пр. гр. Fd3m(О7h). a0 = 10,35. Кристаллическая структура. Образцы, не подвергшиеся метамиктному распаду (бедные радиоактивными элементами), обладают кубической кристаллической структурой, основанной на дефектной, слегка искаженной кубической упаковке. Отсутствие части анионов придает структуре черты каркасной постройки. Редкие металлы и титан располагаются в вершинно связанных октаэдрах, тогда как щелочные и щелочноземельные металлы сосредоточены в крупных полостях, используя вакансии в анионной упаковке. Облик кристаллов октаэдрический (рис. 175). Кристаллы иногда достигают 5 см в поперечнике. Нередко октаэдрические кристаллы притуплены гранями куба. Встречается также в сплошных массах и иногда в колломорфных выделениях. Наблюдались закономерные сростки с цирконом по плоскостям (111), причем грань октаэдра пирохлора совпадает с гранью тетрагональной дипирамиды {111} циркона.
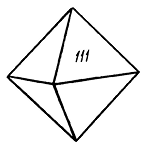
Рис. 175. Кристалл пирохлора
Цвет пирохлора темно-бурый, красновато-бурый, желтовато-зеленый, изредка буровато-черный; по мере перехода к микролиту светлеет, становясь постепенно бледно-оранжевым, желтым до лимонно-желтого (микролит), бетафит обычно темно-бурый, черный. С поверхности вследствие изменения иногда образуются светло-желтые каемки (превращение в оптически анизотропный минерал, ближе не изученный). Черта желтовато-белая до светло-бурой или красновато-желтой. Блеск алмазный, жирный или смолистый (у метамиктных разностей). Полупрозрачен или просвечивает. N = 2,13–2,27 (у метамиктных разностей снижается до 1,96). Твердость 5–5,5. Хрупок. Спайность практически отсутствует. Уд. вес 4,03–4,36. Танталовые разности обладают большим удельным весом (до 4,9). Прочие свойства. Иногда обладает сильной радиоактивностью. Измененные разности при нагревании дают вспышку (при температуре около 500 °С).
Диагностические признаки. Характерны октаэдрический облик кристаллов, цвет, жирный алмазный блеск, раковистый излом. Характерна также связь со щелочными изверженными породами (нефелиновыми сиенитами и сиенитовыми пегматитами). Очень похож на циркон, с которым иногда находится в срастании, и на шеелит, от которого отличается по твердости и отсутствию спайности.
П. п. тр. с большим трудом сплавляется в черновато-бурый шарик. Некоторые разности при нагревании становятся желтовато-зелеными. С бурой дает стекло красновато-желтое в окислительном пламени и темно-красное в восстановительном. В крепкой H2SO4 и HF разлагается.
Происхождение и месторождения. Встречается в пегматитах нефелиновых сиенитов в ассоциации с полевыми шпатами, главным образом альбитом, иногда с цирконом, эгирином, амфиболом, биотитом, апатитом, ильменитом, сфеном, кальцитом и другими минералами, образующимися в более позднюю флюидно-гидротермальную стадию пегматитообразования (месторождения Вишневых гор, Южный Урал). Нередко наблюдается характерное окрашивание тесно срастающегося с ним альбита в коричневато-желтый цвет. Пирохлор характерен также для карбонатитовых массивов: например, Белая Зима (Восточный Саян) и Татарка (Енисейский кряж), где встречается с кальцитом, флогопитом, фторидо-карбонатами TR — бастнезитом и паризитом. Микролит в виде мелких кристаллов известен в гранитных пегматитах Мурзинки (Южный Урал), где нарастает одним из последних на альбит и лепидолит. Стронциопирохлор в виде псевдоморфоз по лопариту обнаружен в альбитизированном пегматите нефелиновых сиенитов с цирконом и Mn-ильменитах в Ловозерских тундрах. В редкометалльно-амазонитовых пегматитах горы Плоская (гряда Кейвы, Кольский полуостров) встречаются кубооктаэдры плюмбомикролита до 5 см в ребре. Бетафит отмечен в Пичехоле (нагорье Сангилен, Тува) в щелочных пегматитах с мозандритом, лопаритом, торитом и бастнезитом. В виде темно-бурых до черных октаэдров бетафит наблюдался с астрофиллитом, галенитом и полилитионитом в гранулированном кварце осевых зон щелочно-гранитных пегматитов массива Дараи-Пиоз (Алайский хребет, Таджикистан).
Установлены позднейшие превращения пирохлора во вторичный продукт в виде псевдоморфоз по октаэдрическим кристаллам пирохлора. Характерно, что эти псевдоморфозы иногда имеют трещины вспучивания и сами кристаллы при этом обладают несколько искаженным октаэдрическим обликом. Этот вновь образующийся минерал оптически изотропен. Цвет светло-желтый. N около 2,1.
Как новообразование пирохлор иногда наблюдается в агрегате ильменита, возникающего, очевидно, при эндогенном разложении ильменорутила — (Ti,Fe,Nb)O2.
Из зарубежных месторождений назовем лишь очень крупное по запасам: Тапира (штат Серра да Канастра, Бразилия).
Практическое значение. В случае значительных по размерам и запасам месторождений представляет промышленный интерес как сырье ниобия, тантала и урана. О применении ниобия см. лопарит.
ГРУППА ЭШИНИТА — (TR,Ca,Th,Fe...)(Nb,Ta,Ti)2O6. Название дано И. Я. Берцелиусом от греч. эсхине — стыд (при проведении химического анализа не удалось разделить содержащиеся в этом минерале компоненты). По составу эшиниты являются титано-тантало-ниобатами редких земель и кальция.
Группа содержит восемь минеральных видов, выделяемых по преобладающим элементам в первой и второй позициях. В титандоминантных видах по преобладающему редкоземельному элементу различаются эшинит-(Ce), эшинит-(Nd) и эшинит-(Y), ранее известный под названием «приорит». Существуют два Nb-доминантных редкоземельных вида: ниобоэшинит-(Ce) и ниобоэшинит-(Nd). Известны два вида с преобладанием Ca в первой позиции и различным заполнением второй: виджеццит (Ca,TR...)(Nb,Ta)2O6 и ринерсонит (Ca,TR...)(Ta,Nb)2O6; редкоземельным аналогом последнего служит танталэшинит-(Y).
Между перечисленными видами по большей части наблюдается совершенный изоморфизм.
Сингония ромбическая. Структура ленточно-координационная субкаркасная. Кислородные октаэдры с Ta, Nb связаны в вытянутые вдоль оси с цепочки через общие вершины, пары таких цепочек через общие горизонтальные ребра связаны в ленты, которые имеют общие вершины с другими лентами. В межленточных трубообразных полостях располагаются катионы редких земель. Кристаллы уплощенно-призматические, иногда в длину достигают 12 см (рис. 176). Цвет черный, коричнево-бурый. Черта темно-бурая до коричневой. Блеск алмазный, жирный. Разности, подвергшиеся метамиктному распаду, изотропны. N = 2,26.
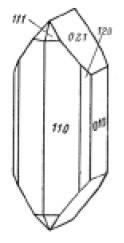
Рис. 176. Кристалл эшинита
Твердость 5–6. Излом раковистый. Уд. вес 5,16–5,23. П. п. тр. не плавится, но вспучивается. В кислотах, кроме HF, не растворяется.
Минералы группы эшинита встречаются в пегматитах нефелиновых сиенитов в ассоциации с нефелином, полевыми шпатами, биотитом, мусковитом, магнетитом, цирконом и другими минералами, а также в карбонатитах. Эшинит-(Ce) и эшинит-(Y) установлены в копях Ильменского заповедника, ниобоэшинит-(Ce) — в Вишневых горах (Южный Урал), а также в Хиттерё (Южная Норвегия) и в других местах. Эшинит-(Y) известен в Абчаде (Прибайкалье), а ниобоэшинит-(Nd) в проявлении Бирая (Патомское нагорье).
САМАРСКИТ — (Y,Er,Fe,U...)4[[Nb,Ta)2O7]3. Сингония ромбическая. Назван по фамилии начальника штаба Корпуса горных инженеров В. Е. Самарского (1803–1870). Химический состав весьма сложен. Содержания главных компонентов колеблются в следующих пределах (в %):
|
Y2O3 … 6,41–14,49; |
Nb2О5 … 27,77–46,44; |
ThО2 … 0–4,23; |
|
Er2O3 … 2,72–13,37; |
Ta2O5 … 1,81–27,03; |
UO2 … 4,02–16; |
|
Ce2O3 … 0,25–3,82; |
TiO2 … 0–1,42; |
PbO … 0–0,98; |
|
La2O3 … 0,37–1,07; |
ZrO2 … 0–2,29; |
CaO … 0,2–3,79; |
|
(Pr, Nd)2O3 … 0,74–4,17; |
SnO2 … 0–0,95; |
FeO … 0–11,15. |
Встречается в призматических, иногда пластинчатых кристаллах с тусклыми гранями (рис. 177). Из граней наиболее часты пинакоиды {100}, {010} и призма {101}. Наблюдаются и неправильной формы зерна, иногда сплошные массы. Интересны закономерные срастания с колумбитом (рис. 178). Известны случаи обрастания кристаллов колумбита самарскитом со всех сторон тонким слоем, причем получаются кристаллы с кажущимся внешним обликом колумбита.
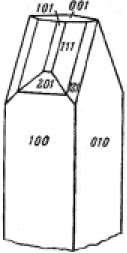
Рис. 177. Кристалл самарскита
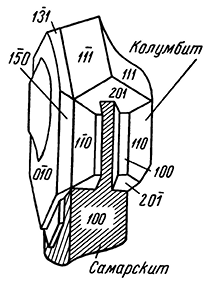
Рис. 178. Ориентированное срастание самарскита
с колумбитом. Увеличено (по Д. П. Григорьеву)
Цвет бархатно-черный, буровато-черный. Черта темная красновато-бурая до черной. Характерен сильный смоляновидный блеск. Почти непрозрачен. В тонких шлифах просвечивает коричневым цветом. N = 2,21–2,25, (для разностей в метамиктном состоянии). Иногда наблюдается сильное двупреломление. Твердость 5–6. Излом раковистый. Уд. вес 5,6–5,8. Сильно радиоактивен.
Из диагностических признаков для самарскита характерны бархатно-черный цвет матовых граней кристаллов, раковистый излом с сильным смоляным блеском.
П. п. тр. слегка оплавляется по краям в черное стекло. В закрытой трубке растрескивается и самораскаляется. С фосфорной солью дает изумрудно-зеленое стекло как в окислительном, так и в восстановительном пламени. Сплавляется с KHSO4. Солянокислый же раствор при кипячении с оловом или цинком окрашивается в голубой цвет (реакция на ниобий).
Встречается в сиенит-пегматитовых жилах Ильменского заповедника на Урале в ассоциации с полевыми шпатами, окрашенными около него в красновато-бурый цвет (результат воздействия продуктов радиоактивного распада элементов самарскита), а также с колумбитом, эшинитом, корундом, монацитом, гранатами, турмалином и другими минералами. Из иностранных можно упомянуть о месторождениях Северной Каролины (с колумбитом) и Мэриленда (США), на о. Мадагаскар (Антанамалаза), около Мосса (Норвегия).
Сюда относятся двуокиси четырехвалентных металлов: U, Th и Zr — уранинит (UO2), торианит (ThO2) и бадделеит (ZrO2). Здесь опишем лишь уранинит.
УРАНИНИТ — UO2. Название дано по составу. Является важнейшим источником урана и радия.
Химический состав встречающихся кристаллов не отвечает написанной формуле1; он является промежуточным между UO2 и UO3 и может достигать U3O8. Наличие в составе уранинита U+6, вероятно, обязано процессу окисления. Содержит Ra, Ас, Po и другие продукты радиоактивных превращений. Как конечный продукт радиоактивного распада U и Th в уранинитах всегда присутствует радиогенный Pb (изотопы Pb206, Pb207 и Pb 208). Содержание его нередко достигает 10–20 %. Однако в урановых рудах часто устанавливается и обычный свинец (за счет включений галенита), содержащий, кроме указанных изотопов, также изотоп Pb204 в постоянном количестве (около 10 %) по отношению к другим изотопам. Некоторые разности уранинита, носящие специальные названия клевеита или нивенита, содержат редкие земли (Се, La, Er...), a также Y. Их количество достигает нескольких процентов (до 12 %). Для крупнокристаллических разностей, встречающихся в пегматитах, характерно содержание Th. Изредка в значительных количествах (до 7,5 %) присутствует Zr. Устанавливаются также газы: Не, Ar, N, СO2 и др. Гелий во всех случаях является результатом радиоактивного распада. Почти постоянно присутствует Н2O, входящая в состав при изменении вещества.
Сингония кубическая; гексаоктаэдрический в. с. Fm3m(О5h). а0 = 5,47. Кристаллическая структура типа флюорита (см. рис. 135). Облик кристаллов кубический с подчиненным развитием граней октаэдра и ромбического додекаэдра (рис. 179). Встречаются октаэдрические, изредка ромбододекаэдрические кристаллы. Размеры их обычно небольшие (иногда до 1 см). Наблюдаются вросшими в породу. Двойники прорастания по флюоритовому закону редки. Агрегаты. Чаще наблюдаются в виде колломорфных почковидных форм сферолитового строения. Такие разности называют урановой смоляной рудой, урановой смолкой, настураном (от греч. слова настое — плотный)2. Наконец, наблюдаются матовые сажистые налеты или порошковатые массы, называемые урановой чернью.
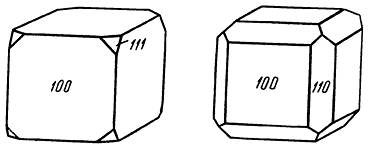
Рис. 179. Кристаллы уранинита
Цвет уранинита черный, иногда со слабым фиолетовым оттенком. В тонких шлифах в проходящем свете непрозрачен или просвечивает темно-бурым, а сильно измененные участки — зеленоватым оттенком. Черта буровато-черная, слегка блестящая. Блеск полуметаллический, чаще типичный смоляной, а у сильно измененных разностей восковой или матовый.
Твердость 5–6, у сильно измененных разностей падает до 3. Хрупок. Излом неровный, приближающийся к раковистому. Уд. вес 10,3–10,6, у сильно измененных разностей ниже. Обычно колеблется от 8 до 10, иногда падает до 6,5 и даже до 4,5. Прочие свойства. Сильно радиоактивен.
Диагностические признаки. Характерны черный цвет, сильный смолистый блеск в изломе, высокий удельный вес и сильная радиоактивность. В окисленных образцах весьма характерна также ассоциация с гуммитами — ярко окрашенными в оранжевые и желтые цвета полиминеральными продуктами разрушения уранинита или урановой смолки.
П. п. тр. не плавится. Значительно окисленные разности уранинита довольно легко растворяются в HNO3, H2SO4 и HF. Соляная кислота растворяет его очень медленно. Наибольшей растворимостью обладают разности, содержащие редкие земли. Перл буры в восстановительном пламени зеленый, в окислительном — желтый. При нейтрализации раствора аммиаком выпадает желтый осадок (NH4)2UO4 — ураната аммония.
Происхождение и месторождения. Среди месторождений уранинита различаются следующие главные генетические типы.
1. Скопления минералов урана в гранитовых и сиенитовых пегматитах, где уранинит встречается сравнительно редко и обычно распределен очень неравномерно в парагенезисе с минералами тория, редких земель, ниобия, тантала (стрюверитом, фергюсонитом, монацитом и др.), а также с турмалином, цирконом, полевыми шпатами, слюдами, иногда в ассоциации с ураноносными углеродистыми соединениями: «тухолитом», «карбураном» и другими минералами неопределенного состава3. Уранинит, образовавшийся в высокотемпературных условиях, как правило, содержит торий и редкие земли. В России уранинит в виде кубических кристаллов до 2 см в ребре отмечен в кварц-плагиоклазовой пегматитовой жиле Хитострова (Северная Карелия).
2. В значительно больших количествах окислы урана распространены в гидротермальных месторождениях. Урановая смолка в месторождениях этого типа ассоциирует иногда с арсенидами Ni и Со (никелином, скуттерудитом, раммельсбергитом,), самородным висмутом, иногда висмутином, самородным мышьяком, самородным серебром, аргентитом, в других случаях — с гематитом, но чаще с карбонатами кальция и железа, черным разложившимся флюоритом и другими минералами. Однако в главной массе урановая смолка образует самостоятельные выделения в карбонатных жилах и прожилках в ассоциации с редкими сульфидами, иногда черным флюоритом и другими минералами.
Из месторождений этого типа широко известно месторождение Яхимов (Чехия), где настуран встречается в карбонатных жилах с мышьяком, серебром, раммельсбергитом. В месторождениях района Джилпин в Колорадо (США) уранинит находится в кварцево-сидеритовых жилах в виде колломорфных выделений в ассоциации с пиритом, халькопиритом, сфалеритом, галенитом, редким самородным висмутом и другими минералами. В золоторудном месторождении Гвадалупе, Чиуауа (Мексика) уранинит наблюдался в кальцитовых жилах с золотом и пиритом.
3. Окислы урана в виде урановой черни образуются также при экзогенных процессах выветривания урановых месторождений в низах зоны окисления или в так называемой зоне цементации (ниже уровня грунтовых вод) в трещинах среди рудного тела или во вмещающих породах и даже в трещинках отдельных минералов. Образование урановой черни объясняют восстановлением в условиях недостатка кислорода растворимых в воде соединений шестивалентного урана, которые с просачивающимися водами достигают зоны цементации. Низшие окислы урана обладают чрезвычайно низкой растворимостью, чем и обусловливается их выпадение из растворов. Урановая чернь наблюдается в виде тончайших пленок, жилок и сажистых скоплений темно-серого или бархатно-черного цвета, иногда с чуть буроватым оттенком. В таких же условиях, но в более широких трещинах могут послойно отлагаться более плотные разности окислов урана с колломорфным строением образующихся черных матовых корок.
Урановая чернь встречается и в некоторых осадочных породах, образование которых происходило в восстановительных условиях, особенно при наличии органических остатков. В ассоциации с ней нередко наблюдаются вкрапления сульфидов железа (пирита и марказита), фосфатов и других минералов. Часто такие осадочные месторождения содержат также повышенные содержания молибдена и ванадия. Следует заметить, что эти месторождения, несмотря на низкое содержание, заключают в себе наибольшие запасы урана.
Уранинит в какой-то мере всегда подвергается позднейшим изменениям независимо от генетического типа и возраста месторождения. Постоянное наличие в его составе высших окислов урана говорит о способности относительно легко окисляться. В зонах окисления он разлагается гораздо легче, чем в эндогенных условиях, и является источником большого числа различных экзогенных минералов урана (в зависимости от условий выветривания, состава первичных руд и поверхностных вод): гидроокислов, сульфатов, карбонатов, уранованадатов, уранофосфатов и ураносиликатов4. Все они обладают яркими желтыми, зелеными или оранжевыми окрасками. Условия их нахождения говорят о том, что соединения урана в зоне окисления подвергаются некоторой миграции. При этом одни участки ее обедняются, другие обогащаются ураном, но в общем значительная часть его все же рассеивается.
Одно из крупных месторождений располагается за Полярным кругом у Большого Медвежьего озера (Канада). Месторождение было обнаружено по ярко окрашенным в желто-оранжевые цвета вторичным урановым минералам, располагавшимся на самой поверхности (возвышенные участки района сглажены ледниками и совершенно не имеют наносов). Многочисленные рудоносные карбонатные и кварцевые жилы, линзы и прожилки, прослеживающиеся на большом протяжении, содержат карбонаты, гематит, урановую смолку, сульфиды и арсениды кобальта и никеля, самородный висмут и более поздние: самородное серебро, аргентит, пирит, халькопирит, галенит, сфалерит и др. Широко развиты колломорфные сферолитовые агрегаты рудных минералов. Месторождение расположено в докембрийских породах. Возраст, определенный разными методами, около 1300 млн лет.
Другое крупное месторождение богатых руд было открыто в провинции Шаба (Демократическая Республика Конго). Оно известно под названиями Казоло и Шинколобве. Оруденение установлено в виде линз и жил в доломитовых породах и сланцах (вдали от гранитных массивов). В составе руд и боковых пород, кроме кварца, принимают участие изредка турмалин, монацит, апатит, затем сульфиды (пирит, линнеит, халькопирит и др.), а также селениды никеля, кобальта и пр. Урановая смолка иногда встречается в очень значительных скоплениях и обычно перекристаллизована в грубозернистые агрегаты. Распространены также кристаллы уранинита. В зоне окисления здесь наблюдались в существенных количествах самые разнообразные вторичные минералы урана: торбернит, беккерелит (Ca(H2O)4)[(UO2)6O2(OH)6] . 2H2O, казолит Pb(UO2)[SiO4] . H2O, соддиит (UO2)2[ SiO4] . 2H2O и др. Возраст его около 610 млн лет.
Практическое значение. Интересно отметить, что уранинитовые руды, получавшиеся попутно с добычей серебра, до момента открытия супругами Кюри радия длительное время использовались лишь для изготовления желтой, оранжевой и черной красок. С 1900-х гг. для той же цели шли урановые отбросы после переработки этих руд на препараты радия. С середины XX в. в связи с разрешением проблемы освобождения и использования колоссальной внутриядерной энергии выявилась исключительная ценность этих руд.
Радий в уранинитовых рудах содержится в количестве нескольких стотысячных долей процента по отношению к массе урана. Получаемые при обработке урановых руд препараты радия имеют разнообразное применение: в медицине при лечении злокачественных опухолей (радоном — продуктом распада радия), для чего применяются специальные приборы, называемые радиопушками; затем гамма-излучение радия используется для просвечивания с целью контроля дефектов в металлических отливках, железобетонных сооружениях и т. п.
Минералы, входящие в это семейство, имеют один и тот же очень простой состав — SiO2. Они представляют собой ряд полиморфных модификаций. По кристаллическому строению эти минералы занимают совершенно особое положение среди окислов. Как мы потом увидим, их кристаллические структуры имеют прямое отношение к силикатам. На этом основании некоторые авторы данную группу минералов рассматривают в разделе силикатов. Но так как кварц по своей химической природе является типичным окислом, то мы, согласно принятой нами установке, должны его рассматривать в этом разделе.
Из относящихся сюда полиморфных модификаций SiO2 четыре главные формы имеют самостоятельные названия: кварц, тридимит, кристобалит и коэсит. Их модификации, связанные переходами второго рода, принято обозначать с приставками греческих букв α и β5. Особняком стоит наиболее высокобарическая модификация кремнезема — стишовит, образующийся при ударах метеоритов о земную поверхность. В природе существует также гидратированный кремнезем — опал SiO2 . nH2O, который мы рассмотрим особо.
Общая картина полиморфных превращений SiO2 изображена на рисунке 180 в виде РТ-диаграммы состояния. Установлен следующий ряд энантиотропных превращений:
|
α-кварц |
↔ |
β-кварц |
↔ |
β-тридимит |
↔ |
α-кристобалит |
↔ |
расплав. |
|
573 °С |
870 °С |
1470 °С |
1713 °С |
Кроме того, для тридимита и кристобалита в области низких температур в сильно переохлажденном состоянии известны также энантиотропные превращения:
|
α-тридимит |
↔ |
β-тридимит и α-кристобалит |
↔ |
β-кристобалит |
|
130 °С |
180–270 °С |
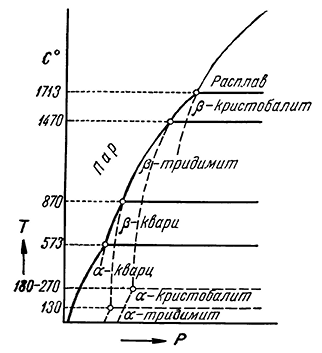
Рис. 180. Однокомпонентная система SiO2. Кривые упругости паров различных
модификаций показаны схематически. При каждой данной температуре более устойчива
та модификация, у которой упругость пара меньше (т. е. кривая ближе к оси ординат)
Кристаллическая структура кварца, как и других полиморфных модификаций, исключая стишовит с октаэдрической координацией кремния, характеризуется той особенностью, что катион Si4+ всегда находится в четверном окружении ионов О2– (рис. 181), расположенных по вершинам тетраэдра. Каждая вершина такого тетраэдра одновременно служит вершиной другого смежного тетраэдра. Таким образом, кристаллические структуры этих минералов состоят как бы из каркасов сцепленных друг с другом тетраэдров. Способ сцепления во всех модификациях один и тот же (через вершины тетраэдров), но ориентировка и общая симметрия в расположении их различны. В целом упаковка ионов кислорода не плотная: в каркасах имеются «пустоты» между тетраэдрами. В низкотемпературных модификациях они обладают малыми размерами, а в высокотемпературных, более «рыхло» построенных модификациях они крупнее. В прямой зависимости от этого находятся и удельные веса, а также показатели преломления.
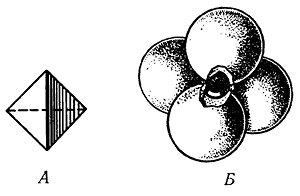
Рис. 181. Кристаллическая структура. а — тетраэдр, поставленный на ребро;
вершины его являются центрами ионов кислорода в тетраэдрической группе SiO4 (б),
внутри которой располагается ион Si4+. Масштаб для а и б один и тот же
Так как каждый ион кислорода является «мостиковым» — общим для двух смежных тетраэдров SiO4, то он всюду располагается между двумя ионами кремния, тогда как каждый ион Si4+ находится в четверной координации ионов кислорода. Отсюда и координационные числа 2 и 4. При рассмотрении тетраэдров SiO4 в рамках второго правила Полинга легко видеть, что каждый положительный ион Si4+ погашает лишь половину отрицательных валентных усилий каждого окружающего его иона О2–, но, так как каждый ион кислорода одновременно принадлежит другому тетраэдру, одновременно погашается и вторая половина его заряда. Таким образом, легко убедиться, что в целом химическая формула соединения будет SiO2.
α-КВАРЦ — SiO2. Эту устойчивую при низких температурах модификацию обычно называют просто кварцем; происхождение названия остается неизвестным. Кварц является одним из наиболее распространенных в земной коре и лучше всего изученных минералов.
Химический состав. Теоретическому составу, очевидно, отвечают бесцветные прозрачные разновидности. Из числа изоморфных примесей следует назвать Al3+, Fe3+, Ti4+. Разности, окрашенные в молочно-белый или другой цвет, в виде механических примесей в разных количествах могут содержать газообразные, жидкие и твердые вещества: СО2, Н2О, углеводороды, NaCl, CaCO3, в ряде случаев включения мельчайших кристалликов рутила, актинолита и других минералов, видимых на глаз.
Сингония. Более высокотемпературная модификация β-кварца кристаллизуется в гексагональной сингонии, гексагонально-трапецоэдрическом в. с. L66L2. Более устойчивая при температурах ниже 573 °С (при атмосферном давлении) модификация α-кварца кристаллизуется в тригональной сингонии, тригонально-трапецоэдрическом в. с. L33L2. Пр. гр. P3121(D43) или P3221(D53) (правая и левая энантиоморфные модификации). a0 = 4,904, с0 = 5,397. Кристаллические структуры довольно просты по структурной схеме. На рисунках 182 и 183 в одинаковом масштабе изображена кристаллическая структура β-кварца и проекции вдоль оси с на плоскость (0001). В каждом тетраэдре SiO4 два кислородных иона располагаются несколько выше, а другие два — несколько ниже, чем ион кремния. Группы тетраэдров лежат в трех слоях на различных высотах; их относительное положение над плоскостью чертежа показано линиями разной жирности и цифрами при кружках (см. рис. 182).
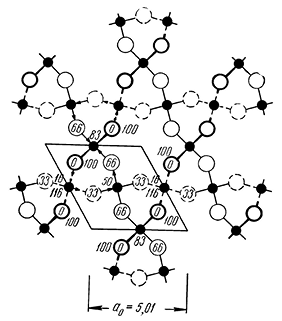
Рис. 182. Кристаллическая структура более высокотемпературной
модификации β-кварца в проекции на плоскость (0001).
Цифры означают относительные высоты ионов над плоскостью чертежа
Как можно заметить на рисунке 183, тетраэдры образуют спирали, каждая из которых закручивается в одну и ту же сторону. Так называемые правые и левые кварцы тем и отличаются, что заворот этих спиралей происходит в правую или в левую сторону. Поворот вокруг шестерной оси на 60° и перенос на одну треть высоты элементарной ячейки вдоль оси с приводят к совпадению с прежней позицией тетраэдров (см. рис. 183).
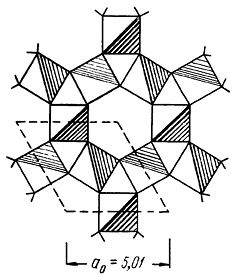
Рис. 183. Та же кристаллическая структура, что и на рисунке 182, но в изображении
в виде тетраэдров. Линиями различной степени жирности
(на затененной стороне тетраэдров) показано относительное положение
этих тетраэдров над плоскостью чертежа. Легко видеть, что тетраэдры, примыкающие
к внутреннему шестиугольнику, расположены по винтовой
оси шестого порядка (по двухходовому винту)
Низкотемпературная модификация α-кварца по своей кристаллической структуре лишь несколько отличается от β-кварца. На рисунке 184 изображены их соотношения в проекции на плоскость (0001), причем показаны лишь ионы кремния. Как видим, при полиморфном превращении высокотемпературной модификации в низкотемпературную происходят небольшие смещения центров кремнекислородных тетраэдров, в результате чего имеет место уплотнение решетки и понижение ее симметрии: шестерные оси превращаются в тройные. При этом тип связи между тетраэдрическими группами не меняется. В процессе превращения не происходит изменений в направлениях заворота спиралей (в правую или левую сторону).
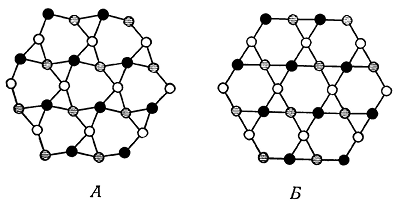
Рис. 184. Соотношения в кристаллических структурах β-кварца (а)
и α-кварца (б). Показаны только ионы кремния, высотное положение
которых отмечено различной степенью затененности кружков
Облик кристаллов. Кристаллы β-кварца, вернее, параморфозы α-кварца по нему, встречающиеся в богатых кремнеземом эффузивных породах (риолитах, кварцевых порфирах и др.) как ранние выделения из жидкой магмы, имеют облик гексагональной дипирамиды, причем грани призмы сильно укорочены или отсутствуют вовсе (рис. 185).
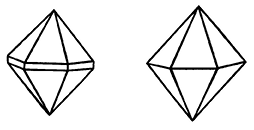
Рис. 185. Кристаллы β-кварца. Гексагональная дипирамида (справа)
в комбинации с гексагональ ной призмой (слева)
Они обычно очень мелки, но в некоторых породах достигают 1–2 см в поперечнике. Низкотемпературный α-кварц в хорошо образованных кристаллах встречается только в пустотах или рыхлых средах. Известны отдельные кристаллы очень крупных размеров, до 1 и даже 40 т весом. Формы кристаллов хотя и весьма разнообразны, но чрезвычайно характерны по присутствию граней призмы m (100), часто с горизонтальной штриховкой, граней ромбоэдров r (10
1) и z (01
1), тригональной дипирамиды s {11
1}, тригонального трапецоэдра х {51
1} и др. (рис. 186). Встречаются индивиды, в которых грани главных ромбоэдров одинаково развиты, и кристаллы в таких случаях принимают облик гексагональной дипирамиды. Будучи протравленными, грани одного ромбоэдра остаются блестящими, другого — становятся матовыми. Фигуры травления также неодинаковы. По положению граней тригонального трапецоэдра {51
1} и дипирамиды {11
1} различают правый и левый кварц (см. рис. 186). Эти грани приурочены к ребрам призмы (через 120°), располагаясь вверху и внизу, но по разные стороны ребра.
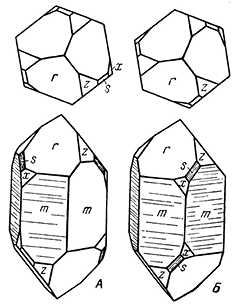
Рис. 186. Левый (а) и правый (б) кварц:
m {100}, r {10
1}, z {01
1}, s {11
1}, х {51
1}
Кроме явнокристаллических модификаций α- и β-кварца известны скрытокристаллические плотные разности, обладающие волокнистым строением: халцедон (волокна вытянуты вдоль одной из осей L2) и кварцин (волокна вытянуты вдоль L3), надежно отличимые друг от друга только по оптическим свойствам (в частности, по знаку удлинения).
Двойники наблюдаются весьма часто и по разным законам.
1. Дофинейские двойники (рис. 187) столь совершенно прорастают друг друга, что похожи на простые кристаллы, от которых они отличаются тем, что грани трапецоэдра х наблюдаются в удвоенном количестве (рис. 188) и выводятся друг из друга поворотом вокруг вертикальной оси не на 120°, а на 60°. Грани призмы обоих индивидов сливаются, а грани ромбоэдра r совпадают с гранями ромбоэдра z (рис. 187). Оптические оси обоих индивидов параллельны, и потому двойниковое строение можно установить только путем травления (рис. 189а). Двойниковые швы извилистые.
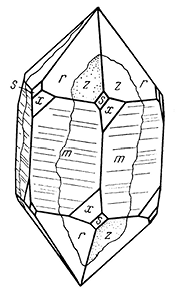
Рис. 187. Дофинейский двойник (схема). Границы между
двумя индивидами заметны по сутурной линии
2. Бразильские двойники (рис. 188) отличаются от дофинейских тем, что в них грани трапецоэдров, наблюдающиеся в двойном количестве, выводятся иначе: отражением в вертикальной плоскости. Двойниковое строение обнаруживается путем травления (рис. 189б). В отличие от строения дофинейских двойников, здесь мы наблюдаем прямолинейные двойниковые швы. Кроме того, бразильские двойники могут быть обнаружены и оптически.
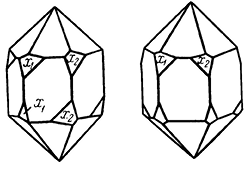
Рис. 188. Дофинейский (а и бразильский (б) двойники (схема)
Рис. 189. Протравленные сечения кристаллов кварца
(перпендикулярно оптической оси):
а — дофинейский двойник; границы индивидов очень неправильные;
б — бразильский двойник с прямыми границами двойниковых индивидов
3. Японские двойники по тригональной дипирамиде {112}; индивиды наклонены друг к другу под углом 84°34′.
Агрегаты. В пустотах широко распространены друзы кристаллов кварца (см. рис. 45), иногда в срастании с кристаллами других минералов. Сплошные же массы кварца представляют зернистые агрегаты. Строение плотных агрегатов легко устанавливается в тонких шлифах под микроскопом при скрещенных николях. Халцедон, обладающий скрытоволокнистым строением, часто наблюдается в виде корок, почковидных форм или сферолитов, но чаще в виде желваков, носящих название кремней. Агаты (кремнистые жеоды) имеют концентрически-зональное строение, обусловленное перемежаемостью различно окрашенных слоев халцедона, иногда кварца. Центральные части жеод нередко сложены кристаллически-зернистым кварцем (см. рис. 47), иногда в виде щеток кристаллов.
Цвет кварца может быть самый различный, но обычно распространены бесцветные, молочно-белые и серые окраски. Прозрачные или полупрозрачные красиво окрашенные разности носят особые названия: 1) горный хрусталь — бесцветные водяно-прозрачные кристаллы; 2) аметист — фиолетовые разности; 3) раухкварц (раухтопаз, уст.) — дымчатые прозрачные разности, окрашенные в сероватые или буроватые тона; 4) морион — кристаллы кварца, окрашенные в черный цвет; 5) цитрин — золотисто-желтые или лимонно-желтые кристаллы. Розовый кварц, не имеющий специального названия, окрашен, по всей вероятности, примесью Ti.
Кроме перечисленных прозрачных разностей кварца наблюдаются явно аллохроматически окрашенные кристаллы кварца благодаря включениям посторонних минералов, также имеющие свои названия: празем — зеленоватый кварц с включениями иголочек зеленого актинолита: авантюрин — желтоватый или буровато-красный кварц с мерцающим отливом, обусловленным мельчайшими включениями слюды, железной слюдки Fe2O3 и др.
Широко распространенный в гидротермальных месторождениях молочно-белый цвет кварцевых масс в одних случаях обязан содержанию в них большого количества микроскопических жидкостей и газов. Почти всегда в жидких включениях наблюдается подвижной пузырек газа, по которому легко узнается жидкость, а иногда даже кристаллики NaCl (рис. 190). При нагревании при определенной температуре эти кристаллики растворяются, затем исчезают пузырьки газа и образуется однородная жидкая фаза. При охлаждении она вновь становится неоднородной. Таким путем можно примерно установить, при какой температуре мог произойти захват этих жидких фаз в процессе кристаллизации кварца. В других случаях молочно-белый цвет кристаллов кварца обусловлен сильной трещиноватостью, возникшей при динамических воздействиях (подобно тому, как совершенно прозрачный лед при ударе молотком в поврежденном месте становится молочно-белым).
Рис. 190. Газовый пузырек и кристаллик галита в капельке
жидкости, включенной в кварц. Увеличено
Халцедон чаще, чем кристаллический кварц, бывает окрашен в самые различные цвета и оттенки: молочно-серый, синевато-черный (сапфирин), желтый, красный, оранжевый (сердолик), коричневый, бурый (сардер), зеленый (плазма), яблочно-зеленый от соединений никеля (хризопраз), зеленый с красными пятнышками (гелиотроп) и др. Агаты или ониксы сложены часто тончайшими различно окрашенными концентрически-зональными или плоскопараллельными слоями халцедона (рис. 191), могут иметь самые различные сочетания оттенков: черного с белым (арабский оникс), бурого с белым (сардоникс), красного с белым (карнеолоникс) и др.

Рис. 191. Агат — концентрически зональный халцедон
Блеск кварца стеклянный, на изломе — слегка жирный, халцедона — восковой до матового. Оптические константы. Кварц оптически одноосный, положительный. Ng = 1,553 и Nm = 1,544. Он обладает способностью вращать плоскость поляризации в ту или другую сторону в зависимости от того, имеем ли мы дело с правым или левым кварцем.
Твердость 7. Спайность у большинства индивидов кварца отсутствует или весьма несовершенная по ромбоэдру. У кристаллов с высокой степенью совершенства кристаллического строения (так называемых моноблоков) спайность по ромбоэдру средняя до ясной. Излом раковистый. Уд. вес 2,5–2,8, для чистых разностей 2,65; β-кварц, обладающий менее плотной упаковкой, имеет несколько меньший удельный вес. Прочие свойства. Кварц способен пропускать ультрафиолетовые лучи. Обладает свойством пьезоэлектризации: под влиянием механических напряжений в нем возникают электрические заряды. Электрическими осями являются двойные, причем тот конец каждой двойной оси, который упирается в ребро, срезанное гранями трапецоэдра, электризуется отрицательно, а противоположный конец — положительно. Температура плавления кварца 1713 °С. При застывании расплава легко образуется кварцевое стекло (аморфный кварц), обладающее рядом особых свойств (кислотоупорностью, низким коэффициентом расширения, способностью пропускать ультрафиолетовые лучи и др.).
Диагностические признаки. Кристаллы кварца легко узнаются по характерным для них формам и штриховке, поперечной к удлинению. Кварц в плотных агрегатах устанавливается по высокой твердости, раковистому излому и отсутствию спайности.
Халцедон от похожих на него минералов (опала, смитсонита — Zn[CO3], скрытокристаллического флюорита и др.) отличается главным образом по твердости. Легко отличим также по оптическим свойствам.
П. п. тр. не плавится. С кислотами не реагирует, за исключением HF, с которой легко образует летучее соединение — SiF4. Поддается влиянию щелочей. На халцедон сильно действует КОН.
Происхождение и месторождения. Кварц, будучи широко распространен в природе, входит в состав самых различных по генезису горных пород и рудных месторождений.
1. Во многих интрузивных и эффузивных кислых изверженных породах он, так же как и полевые шпаты и слюды, является существенной составной частью (в гранитах, гнейсах, кварцевых породах и др.). Порфировые кристаллы кварца в кислых эффузивных породах обладают кристаллически-зональным строением, часто содержат включения вулканического стекла.
2. В крупных кристаллах (раухтопаз, морион, аметист и др.) он встречается в пустотах среди пегматитов также в ассоциации с полевыми шпатами, мусковитом, иногда топазом, бериллом, турмалином и другими минералами. Часто наблюдаются закономерные срастания его с крупными индивидами калиевых полевых шпатов — ортоклаза или микроклина, напоминающие в приполированных штуфах еврейские письмена. Характерно, что все эти включения кварца в каждом данном кристалле полевого шпата оптически ориентированы одинаково.
3. Как постоянный жильный минерал, и притом в значительных массах, кварц распространен в чрезвычайно многочисленных на земном шаре гидротермальных месторождениях в ассоциации с самыми различными минералами: касситеритом, вольфрамитом, золотом, молибденитом, пиритом, халькопиритом, турмалином, кальцитом, хлоритами и др. Почти всегда кварц содержит микроскопические включения газов, жидкостей и твердых минеральных веществ.
Агаты и ониксы в виде миндалин (секреций) самых различных форм и размеров широко распространены во многих эффузивных горных породах — мелафирах, базальтах, андезитах и др. (измененных пузыристых лавах). Образование их связано с проникновением концентрированных водных растворов кремнезема в заключительный этап гидротермальной деятельности среди этих пород.
4. При экзогенных процессах кварц и халцедон в виде тонкозернистых агрегатов образуются при просачивании и кристаллизации из холодноводных растворов кремнезема. При этом известны случаи образования в пустотах кристаллов кварца, например в трещинах среди окремненных приповерхностных процессах тех или иных пород (известняков, серпентинитов и др.).
Зато гораздо шире в этих условиях образуется халцедон. Наблюдались случаи его отложения после опала в пустотах между колломорфными выделениями последнего. Наиболее широко халцедон распространен в виде кремней в известняках, а также желваков в коре выветривания, напоминающих по внешнему виду миндалины и жеоды однородного халцедона гидротермального происхождения в изверженных эффузивных породах.
5. При метаморфических процессах кварц в значительных массах образуется при обезвоживании опалсодержащих осадочных пород с образованием так называемых яшм и слоистых роговиков (чрезвычайно тонкозернистых кварцевых и кварцево-халцедоновых пород).
Однако наибольший интерес как с минералогической, так и с практической точки зрения представляют жилы альпийского типа, образующиеся в линзовидных трещинах, возникающих при метаморфизме и рассланцевании горных пород (см. рис. 60). В больших пустотах и трещинах («хрустальных погребах»), лишь частично выполненных минеральным веществом, стенки бывают усеяны наросшими прекрасно образованными, нередко крупными кристаллами кварца в сопровождении хлоритов, полевого шпата, рутила, брукита, кальцита и др. Эти жилы и сами кристаллы обладают многими характерными особенностями. Кристаллы горного хрусталя имеют самую различную ориентировку по отношению к стенкам пустот. Установлено, что эта ориентировка находится в зависимости от ориентировки породообразующих зерен кварца, обнаженных в стенках боковой породы и явившихся затравками для крупных кристаллов, выросших в пустоте. Кристаллы горного хрусталя с ненарушенным деформациями монокристаллическим строением (моноблоки) обладают наилучшими пьезоэлектрическими свойствами.
При процессах выветривания кварц является химически стойким минералом и потому накапливается в виде обломочных зерен в россыпях и осадочных породах (песчаниках, кварцитах).
Псевдоморфозы кварца были установлены по самым различным минералам: кальциту, бариту, гипсу, полевым шпатам, оливину и т. д., а также по животным и растительным остаткам.
Месторождения чрезвычайно многочисленны; укажем в качестве примеров лишь некоторые.
Из месторождений в России, представляющих большой минералогический интерес, следует отметить издавна известные Мурзинские, Липовские, Шайтанские и другие пегматитовые копи (к северо-востоку от Екатеринбурга), содержащие друзы великолепных кристаллов горного хрусталя, дымчатого кварца и аметиста в ассоциации с полевыми шпатами, турмалином, лепидолитом и др. Гидротермальные жилы с горным хрусталем высокого качества имеются на месторождении Астафьевское (Южный Урал). «Альпийские жилы» с кварцевым пьезосырьем известны на Приполярном Урале (Додо, Неройка, Пеленгичей). Пегматитовые жилы с морионом и аметистом распространены в хребте Адун-Чилон (Забайкалье) и в других местах. Месторождения кварцевых жил с горным хрусталем известны также на Алдане (Перекатное). Хороший аметист находится в долине р. Кедон (Магаданская область) и в проявлении Обман (Алдан), цитрин — в Ольховичном месторождении (Приполярный Урал).
Сургучно-красные слоистые яшмы как поделочные камни распространены в Примагнитогорском районе (Урал). Широкой известностью пользуются равномерно окрашенная в зеленовато-серый цвет калганская яшма и разнообразные по рисункам яшмы Орского района (Ю. Урал).
Хорошие агаты встречаются на Тимане (Чаицын мыс), на Охотском побережье (Ольское плато), на Камчатке (мыс Теви) и на Чукотке (бассейны рек Рывеем и Каненмывеем). Месторождения цветных халцедонов (сердолик, сардер) и агатов известны в виде богатых аллювиальных россыпей в Приамурье (Норское и Бурундинское).
Месторождения так называемого технического агата встречаются в Закавказье в Ахалцихском и других районах. В Армении известно Иджеванское месторождение поделочного агата. Генетически они связаны с покровами эффузивных пород.
Из иностранных месторождений благородных разновидностей кварца следует упомянуть о месторождениях Бразилии в Минас-Жерайс и Уругвая (главным образом аметист), Мадагаскара (горный хрусталь), Швейцарских Альп и т. д. Все эти месторождения большей частью представлены пегматитовыми или кварцевыми жилами альпийского типа. Лучшие агаты известны в месторождениях Индии, Бразилии, Уругвая, Германии (Оберштайн, Рейнланд и др.).
Практическое значение. Применение кварца и халцедона разнообразно.
1. Прозрачные красиво окрашенные разности этих минералов применяются в качестве поделочных камней для украшений.
2. Бесцветные горные хрустали употребляются для изготовления оптических приборов.
3. В точной механике некоторые разности этих минералов (особенно технический агат) широко используются для изготовления подпятников в механизмах, опорных призм, часовых камней и т. д.
4. В радиотехнике для изготовления пьезокварцевых пластинок как элементов стабилизаторов частот радиоволн, резонаторов и т. д. употребляются совершенно однородные недвойникованные кристаллы, обладающие ярко выраженными пьезоэлектрическими свойствами (моноблоки горного хрусталя); для этих целей пригодны кристаллы размерами не менее 3,5 см между противоположными гранями призмы. В настоящее время кристаллы пьезокварца в больших объемах выращиваются искусственно из растворов в щелочах; в качестве шихты при выращивании используется по возможности беспримесный природный кварц, требования к такому сырью также чрезвычайно высоки.
5. Из плавленого кварца изготовляется химическая посуда, отличающаяся огнеупорностью и кислотоупорностью, а также кварцевые лампы, применяющиеся в медицине для лечения ультрафиолетовым светом, для которого кварц (один из немногих минералов) прозрачен.
6. В стекольно-керамической промышленности для варки стекла и выделки фарфора и фаянса применяются чистые маложелезистые (до 0,002 %) кварцевые пески.
7. Применяется для производства карбида кремния — карборунда (SiC), обладающего высокой твердостью (выше, чем у корунда) и применяемого в качестве первоклассного абразивного материала.
8. Тонкие кварцевые пески применяются в пескоструйных аппаратах для полировки поверхностей металлических и каменных изделий, а также для распиловки горных пород и ряда других целей.
9. Песчаники, состоящие из сцементированных окатанных зерен кварца, и их метаморфизованные разности — кварциты (горные породы) служат строительным материалом.
ТРИДИМИТ — SiO2. От греч. тридимос — тройной (назван вследствие часто наблюдаемых тройников). Более высокотемпературная модификация — β-тридимит гексагональной сингонии в области неустойчивых состояний легко переходит в более низкотемпературную, близкую к ней по кристаллической структуре модификацию — α-тридимит ромбической сингонии. При атмосферном давлении α-тридимит с течением времени способен переходить в устойчивую форму — α-кварц. Превращение β-тридимита в β-кварц, т. е. модификацию хотя и гексагональной сингонии, но весьма существенно отличающуюся по кристаллической структуре, происходит гораздо медленнее и сопровождается значительным изменением объема и удельного веса (уд. вес β-кварца 2,51, β-тридимита — 2,26).
Кристаллы α-тридимита, более устойчивого при низких температурах, наблюдаются в виде псевдогексагональных пластинок (рис. 192) или чаще тройников (рис. 193) с углом между пластинками 35°18′. Встречаются также розетковидные или черепитчатые агрегаты. Цвет α-тридимита белый, серовато-белый; иногда он бесцветный. Блеск стеклянный. Ng = 1,473, Nm = 1,470 и Np = 1,469. Твердость 6–7. Спайность несовершенная. Уд. вес 2,3.
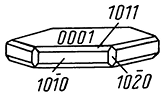
Рис. 192. Кристалл тридимита
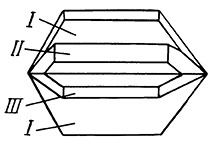
Рис. 193. Тройник тридимита
Встречается преимущественно в пустотах кислых эффузивных пород: в трахитах в Зигенгебирге (Германия), андезитах в Сан-Кристобале (Мексика), в продуктах извержений Везувия и т. д.
КРИСТОБАЛИТ — SiO2. Название дано по местности Сан-Кристобал (Мексика). Полиморфные модификации: более высокотемпературная — β-кристобалит кубической сингонии и низкотемпературная — α-кристобалит. Этот последний относится к тетрагональной сингонии, являясь в то же время псевдокубическим.
Кристаллы β-кристобалита обладают октаэдрическим обликом (рис. 194), реже они имеют кубическую или скелетную форму. Встречаются двойники по (111). Цвет молочно-белый. Блеск стеклянный. Nm = l,49. Твердость 7. Уд. вес 2,27.
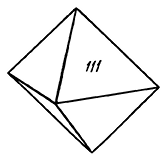
Рис. 194. Кристалл кристобалита
Легко получается при образовании кварцевого стекла, а также кристаллизуется при обжиге динасовых кирпичей. Встречается в быстро остывших эффузивных породах, часто совместно с α-тридимитом: в андезитах Сан-Кристобала (Мексика), лавах Майна в Рейнланде (Германия), Йеллоустонском парке (США) — в виде шариков (сферолитов) до 1 мм в обсидиане (вулканическом стекле), а также в пустотах, иногда с наросшими пластинками тридимита на кристалликах кристобалита.
Известны и другие способы образования β-кристобалита, а именно при воздействии базальтовой магмы на кварцсодержащие осадочные породы (песчаники). Кристобалит в этих случаях образуется за счет кварца при высокой температуре. Подобные образования (бухиты) описаны, например, в глинистых песчаниках поздненеогенового возраста в Западной Грузии.
ОПАЛ — SiO2 . aq. Типичный твердый гидрогель. Происхождение названия неизвестно. Разновидности по физическим признакам: 1) благородный опал, обладающий опалесценцией; 2) гидрофан — легкая разновидность, сильно пористая, мутная в сухом состоянии и прозрачная в воде; 3) гиалит — сталактитовые образования или шарики сферолитового строения.
Химический состав очень непостоянный. Содержание воды колеблется от 1 до 5, крайне редко достигая 34 %. Часть воды все опалы способны терять при высушивании в эксикаторе. Особенно быстро потеря ее происходит в первые дни (рис. 195). При нагревании одни опалы отдают главную часть воды до 100 °С, другие — выше этой температуры (100–250 °С). Причины этой различной прочности связи воды полностью не выяснены.
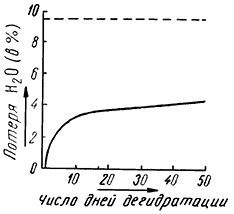
Рис. 195. Кривая обезвоживания опала (над H2SO4)
Внутреннее строение опалов является весьма своеобразным: опал построен из полимеризованных нитей аморфного кремнезема с фрагментами более правильной структуры кварца, а нередко и тридимита. Нити свернуты или собраны в глобулы — шаровидные образования выдержанного размера диаметром порядка 1000 Å. Глобулы в свою очередь регулярным образом уложены в упаковку, по конфигурации близкую к плотнейшей кубической, иногда — гексагональной; в промежутках между глобулами размещается вода, которая их дополнительно связывает. Получающаяся регулярная структура по масштабу периодичности отвечает длинам волн видимого света и способна вызвать интерференционные явления, обеспечивающие столь ценимый в ювелирно-поделочных опалах эффект опалесценции.
Морфологические особенности. Обычно наблюдается в плотных стеклоподобных массах с натечной внешней формой. Является главной составной частью некоторых организмов, слагая панцири диатомей, спикули губок, скелеты радиолярий, отчасти некоторых фораминифер и мшанок, для которых коллоидные растворы (золи) кремнезема служат пищей. Благодаря наличию кремнезема скелеты этих организмов в большинстве случаев прекрасно сохраняются в ископаемом состоянии даже в древнейших отложениях. Гидроокислы кремнезема входят также в состав соломы злаков, твердых узловатостей в хвощах и особенно узлов бамбука и других растений, поглощающих золи кремнезема из почвы своими корнями. Золи кремнезема способны пропитывать отмершие стволы деревьев и, отлагая опал, полностью их замещать с сохранением всех деталей строения («деревянистый опал»).
Цвет. Сам по себе опал бесцветен. Благодаря различным примесям, особенно содержащим железо и другие хромофоры, он бывает окрашен в различные оттенки желтого, бурого, красного, зеленого и черного цветов. Блеск стеклянный (у пористых масс восковой или матовый). Для полупрозрачных разностей характерна цветовая игра — опалесценция (происхождение названия этого явления связано именно с этим минералом). N = 1,40–1,46.
Твердость 5–5,5 (у разностей, очень бедных водой, поднимается до 6). Хрупок. Уд. вес 1,9–2,5 (зависит от содержания воды и количества адсорбированных тяжелых веществ).
Диагностические признаки. Для плотных опалов характерны стеклообразный вид и натечные формы масс, сплошные корки. По внешним признакам опал имеет много общего с халцедоном. Он отличается меньшей твердостью и содержанием воды.
П. п. тр. не плавится, но часто сильно растрескивается. В закрытой трубке выделяет воду. В кислотах не разлагается. Довольно легко растворяется в КОН и HF. Обезвоженный опал растворяется в соде с шипением (вследствие выделения СО2).
Происхождение и месторождения. Опал нередко отлагается из гидротермальных источников и гейзеров в вулканических областях в виде накипи (кремнистый туф, гейзерит), иногда в виде белых просвечивающих натеков с перламутровым отливом. Распространен также в пустотах и трещинах среди эффузивных горных пород, иногда в виде жеод и миндалин.
Однако в главной массе он образуется в экзогенных условиях при разложении силикатов в процессе выветривания самых различных по составу горных пород, но чаще ультраосновных. Кремнезем, освобождающийся при распаде кристаллических структур силикатов, переходит первоначально в золь, при коагуляции которого выпадает в зоне элювия в виде желваков натечной формы или отлагается метасоматическим путем, часто совместно с гидроокислами железа, алюминия и других элементов, на различных коренных горных породах.
Огромные массы опала образуются осадочным путем в виде пластов в процессе коагуляции приносимых речными водами золей кремнезема в прибрежных зонах морских бассейнов. К ним принадлежат так называемые опоки, трепелы, диатомиты, кизельгур (кремневая мука) и т. д., представляющие собой рыхлые или тонкопористые, иногда более или менее крепкие породы, на поверхности часто превращенные в мелоподобные массы вследствие механического действия замерзающей воды, пропитывающей их.
Следует упомянуть, наконец, об окаменяющей роли растворов кремнезема при метасоматозе растительных остатков и, в частности, стволов деревьев. Каким бы путем ни образовался опал, он в конце концов постепенно переходит в халцедон или кварц.
Осадочные опалсодержащие породы (опоки, трепелы и диатомиты) особенно широким распространением пользуются в неогеновых мелководных отложениях в Ульяновской, Саратовской и других областях европейской части России, а также вдоль восточного склона Уральского хребта и в других местах. Из иностранных месторождений следует упомянуть о месторождениях Богемии, Италии, Ливии (Триполи, откуда происходит название трепел) и др. Месторождения благородных опалов известны на южном склоне Карпат, близ Кошице (в пустотах изверженной породы — андезита), в Австралии — Новый Южный Уэллс и Квинсленд (в песчаниках, занимающих огромную площадь) и в других местах.
Практическое значение. Благородные опалы употребляются как поделочные камни. Трепел применяется для полировки металлов, камней и для других целей. Кизельгур идет на изготовление фильтров, керамики, выделку легких кирпичей и на другие цели.
Обобщение. Таким образом, все природные модификации, за исключением опала и лешательерита (аморфного кварцевого стекла), характеризуются кристаллическими структурами, представляющими собой каркасы кремнекислородных тетраэдров, соединенных друг с другом вершинами, т. е. каждый ион кремния окружен четырьмя ионами кислорода, а каждый ион кислорода связывает два иона кремния. Отличие в структурах заключается в пространственной ориентировке этих тетраэдров и в самом узоре каркаса. Особенности кристаллических структур обусловливают и физические свойства минералов (табл. 9).
Таблица 9. Важнейшие свойства различных модификаций SiO2
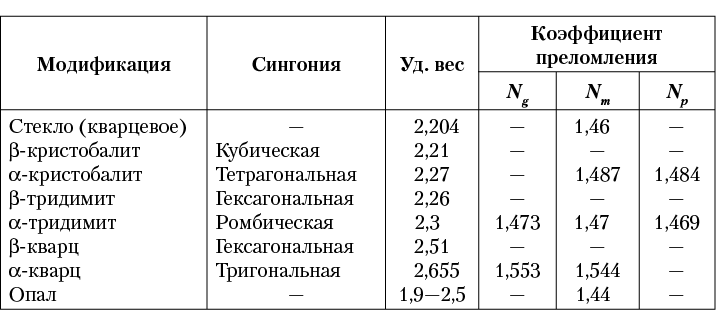
1 Напомним из химии, что уран с кислородом дает следующие соединения: UO2 — закись урана, называемую также двуокисью черного цвета, и UO3— аморфную трехокись урана желтого цвета.
2 Более употребителен давно укоренившийся термин «урановая смолка», рентгенограмма которой сходна с рентгенограммой уранинита.
3 По микроскопическим исследованиям, «тухолит» и «карбуран» как самостоятельные соединения не существуют, а представляют механические смеси углеродистого вещества с уранинитом.
4 Аморфные продукты изменений уранинита в виде налетов или корок яркокрасного, оранжевого и желтого цвета называли гуммитом. Исследования показали, что это вещество представляет собой смесь оранжевокрасного кюрита (гидрата урана и свинца) и желтого соддиита (силиката урана).
5 Некоторые авторы, в частности П. Ниггли, Ф. Ринне, А. Е. Ферсман и др., придерживались обратного обозначения: более низкотемпературную модификацию αкварц они обозначали как βкварц, αкристобалит — как βкристобалит и т. д.

