Общие замечания. В этом последнем разделе неорганических минералов мы рассмотрим сложные соединения, с химической точки зрения представляющие собой соли различных кислородных кислот. По количественному составу этот раздел является наибольшим — к нему относятся почти две трети всех известных минералов. Этим определяется значение указанных соединений в минералогии.
Господствующее положение среди них занимают силикаты. Весьма многочисленны также сульфаты и фосфаты. Все они в земной коре распространены, естественно, только в твердом состоянии и являются продуктами химических реакций, протекающих в самых различных геологических условиях.
Мы не будем подробно останавливаться на характеристике химических особенностей кислородных солей вообще. Они детально разбираются в курсах химии, и природные соли ничем принципиально от них не отличаются.
Напомним лишь, что среди солей прежде всего различают соли безводные и водные (т. е. содержащие в своем составе молекулы Н2О). Среди тех и других важно также различать:
1) кислые соли (например, NaHCO3 — нахколит, кислый карбонат натрия), т. е. соли, содержащие вместо одного металлического катиона протон Н+1. В природных условиях кислые соли встречаются сравнительно редко;
2) нормальные, или средние, соли, пользующиеся наибольшим распространением в природе. Примеры: Са[СО3] — кальцит (известковый шпат), Ca[SO4] . 2H2O — гипс;
3) основные соли, т. е. соли, содержащие в своем составе ионы гидроксила [ОН]1–, нейтрализующие избыточный положительный заряд катионов. Эти соли широко распространены в природе. Примерами могут служить: Cu2[CO3][OН]2 — малахит и Al2[SO4][ОН]4 . 7Н2О — алюминит.
В основных солях анион [ОН]1–, как это устанавливается на целом ряде примеров, может быть частично или полностью заменен другими анионами, чаще всего равновеликим анионом F1–, иногда O2– и Cl1– (без изменения общей структуры соединения). Все такие соли, включая и соли с OH, мы будем называть солями с добавочными анионами.
Двойные и более сложные соли как определенные соединения от простых солей отличаются тем, что катионы или анионы или те и другие вместе представлены разными ионами, изоморфно не замещающими или ограниченно замещающими друг друга. Примеры: CaMg[CO3]2 — доломит, Na6Mg2[CO3]4[SO4] — тихит и др.
В солях переменного состава имеет место как изовалентный, так и гетеровалентный изоморфизм. В последнем случае всегда устанавливается уравновешивание положительных и отрицательных зарядов в соединениях. Примеры: (Mn,Fe)[CO3] — Fe-родохрозит, Са5[PO4,SiO4,SO4]3[F,ОН] — силико-сульфатный фторапатит (вилькеит) и др.
Кристаллохимические особенности соединений. Характерной особенностью кристаллохимии кислородных солей является наличие в их кристаллических структурах комплексных анионов: [NO3]1–, [СО3]2–, [SO4]2–, [РО4]3– и т. д. Катионы, располагающиеся в центрах этих групп, обладают малыми размерами ионных радиусов, высокими зарядами (рис. 206) и ковалентно связаны с ионами кислорода.
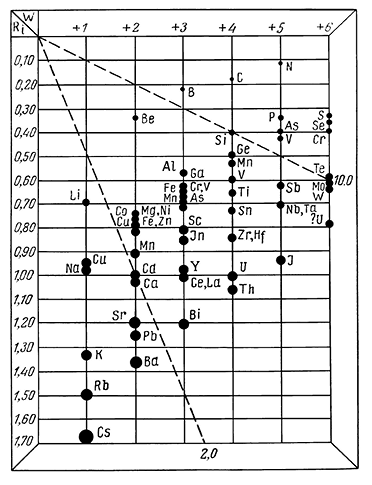
Рис. 206. Диаграмма главнейших катионов,
распространенных в природных соединениях
Очень важно обратить внимание в этих группах на прочность связи ионов кислорода с центральным катионом, определяемую так называемой электростатической валентностью, т. е. величиной заряда, приходящегося от катиона на каждый окружающий его ион кислорода. Так, в комплексном анионе [NO3]1–, состоящем из N5+ и трех окружающих ионов О2–, каждый кислород получает пай заряда 5 : 3, в анионе [СО3]2– эта величина составляет 4 : 3, анионе [SO4]2– — 6 : 4, анионе [РО4]3– — 5 : 4 и т. д.
Как видим, это отношение всюду превышает 1 (т. е. больше половины валентности кислорода уходит на связь с центральным катионом), и только для [ВО3]3– и [SiO4]4– оно равно 1. Это означает, что ионы кислорода прочнее связаны с малыми катионами внутри комплексов, чем с катионами, расположенными в кристаллических структурах вне комплексных анионов. В этом отношении кислородные соли весьма существенно отличаются от сложных окислов, для которых величины электростатической валентности связи между катионами и окружающими их ионами кислорода всегда меньше 1.
Таким образом, комплексные анионы представляют собой прочно связанные в одно целое компактные группы, участвующие в кристаллических структурах как самостоятельные структурные единицы. Самостоятельность их подчеркивается тем, что эти группы не распадаются и при растворении солей. От простых анионов они существенно отличаются по форме и, естественно, по размерам. Анионы типа XO4 имеют тетраэдрическую координацию и по форме близки к изометрическим телам. Анионы типа ХO3 обладают формой плоских треугольников (СО3, ВО3), реже тупых пирамид (AsO3 и др.), в которых ионы кислорода «сидят» по углам треугольника, а связывающий их катион — над центром этого треугольника.
Кроме простых по конфигурации комплексных анионов, как мы потом увидим, существуют и более сложные радикалы. Характерно, что они свойственны боратам и силикатам, т. е. солям наиболее слабых кислот.
Соли других, более сильных кислот характеризуются кристаллическими структурами с типичной ионной связью, подобно тому, как это имеет место в галогенидах, с той только разницей, что роль простых анионов здесь играют комплексные анионы. Поэтому неудивительно, что они по ряду физических свойств очень близко напоминают минералы, относящиеся к хлоридам и фторидам.
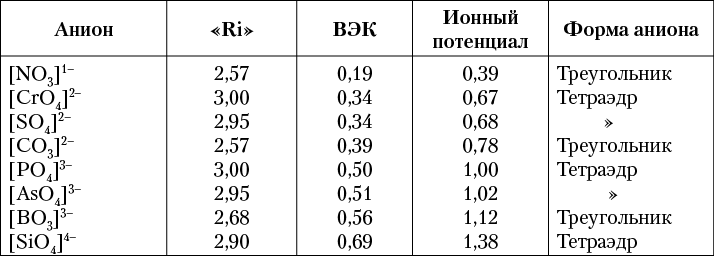
Список главнейших простых по строению комплексных анионов, распространенных в природных кислородных солях, приведен в таблице 10 в порядке увеличения значений ВЭКов или ионных потенциалов. Там же приведены и размеры анионов в виде ионных «радиусов» (по А. Е. Ферсману). Необходимо заметить, что в буквальном смысле о каких-либо радиусах комплексных анионов не может быть и речи. Приведенные в таблице значения получены А. Е. Ферсманом путем расчета и сугубо приблизительны. Однако для общих соображений о свойствах минералов эти ориентировочные величины являются полезными, особенно если учесть, что такие свойства, связанные с энергией кристаллической структуры, как твердость, плавкость, летучесть, относительная растворимость и др., мы практически расцениваем по очень грубым шкалам.
Таблица 10. Комплексные анионы важнейших
природных кислородных солей
В более наглядной форме приведенные в таблице значения показаны на диаграмме (рис. 207). Для сравнения нанесены в виде полых кружков также одновалентные простые анионы ранее рассмотренных галогенидов и двухвалентные простые анионы, входящие в состав окислов, сульфидов, селенидов и теллуридов.
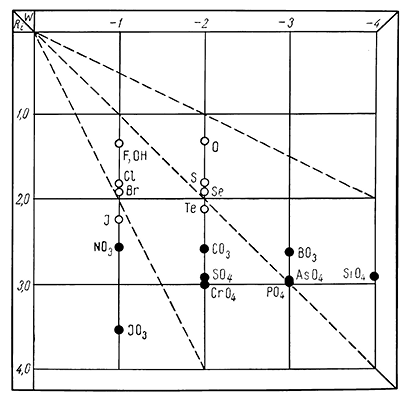
Рис. 207. Приблизительные размеры комплексных анионов
(черные кружки) в сравнении с размерами простых анионов,
распространенных в природных соединениях
Так как подавляющая масса кислородных солей представляет собой типичные ионные соединения, то естественно, что устойчивость кристаллических структур в значительной мере должна зависеть от соотношений размеров катионов и анионов как структурных единиц. Для кислородных солей эти соотношения невозможно выразить в каких-либо цифровых значениях, так как размеры комплексных анионов мы не можем выразить в радиусах в силу того, что они по своей конфигурации существенно отличаются от шаровой формы, которую мы условно приписываем простым ионам.
Однако не может быть никакого сомнения в том, что такие изометрические комплексные анионы, как [SO4]2–, [PO4]3– , [SiO4]4– и др., по своим размерам должны быть существенно больше, чем простые анионы (например, O2–). Поэтому не случайно эти анионы в простых соединениях типа АХ (где X представлен комплексным анионом) наиболее устойчивые кристаллические структуры дают только в сочетании с крупными катионами. Эти соединения действительно являются труднорастворимыми, трудноплавкими и труднолетучими. Обратимся к примерам.
Двухвалентный анион [SO4]2– в соединениях типа АХ (т. е. с соотношением катион : анион, равным 1 : 1) образует следующие наиболее устойчивые соединения (сульфаты): BaSO4 — барит и PbSO4 — англезит, т. е. в сочетании с самыми крупными двухвалентными катионами (см. колонку двухвалентных катионов на рис. 206). С этой точки зрения понятной становится также изоморфная примесь Ra2+ и Ва2+, устанавливаемая иногда в баритах (ионный радиус Ra2+ несколько больше, чем Ва2+). Неудивительно, что в зонах окисления урановых месторождений, содержащих сульфиды в условиях действия сульфатных вод, концентрация радия по отношению к урану выше, чем это имеет место в зоне первичных руд (соединения шестивалентного урана в этих условиях значительно более растворимы по сравнению с сульфатом радия).
Что касается двухвалентных катионов с малыми ионными радиусами, то они в природных условиях могут образовывать только водные сульфаты, кристаллизующиеся при низких температурах и притом в последние стадии кристаллизации растворов. В большинстве случаев водные соли содержат 2, 4, 6 и 7 молекул H2O. Рентгенометрические исследования соединения Ni[SO4] . 6H2O показали, что катион Ni2+ в кристаллической структуре непосредственно окружен шестью электрически нейтральными (т. е. не погашающими заряд катиона) молекулами воды. Вследствие этого объем таких гидратированных катионов как бы искусственно увеличивается, благодаря чему и становится возможной постройка кристаллической структуры с участием таких крупных анионов, как [SO4]2–. С кристаллохимической точки зрения формулу этого соединения было бы правильнее писать так: [Ni(H2O)6][SO4]. Такие водные соли обладают явно повышенной или высокой растворимостью и легко подвергаются обезвоживанию, причем кристаллические структуры их претерпевают перестройки или вовсе разрушаются.
Интересно отметить, что средний по размерам катион Ca2+ (см. рис. 206) хотя и способен в известных условиях образовать безводный сульфат Ca[SO4] (ангидрит), однако в присутствии воды он переходит в более устойчивое водное соединение Ca[SO4] . 2H2O (гипс)1. Последний, по рентгенометрическим данным, обладает слоистой структурой, в которой молекулы Н2О располагаются между листами, сложенными ионами Са2+ и [SO4]2–. Этим обусловлена весьма совершенная спайность кристаллов гипса в данном направлении.
Если мы перейдем к трехвалентному аниону [РО4]3–, то увидим аналогичную сульфатам картину. Среди трехвалентных катионов (см. рис. 206) наиболее крупными, могущими образовывать с этим ионом устойчивые кристаллические структуры, являются редкие земли (Се...) и La. В природе действительно распространен очень стойкий фосфат редких земель — (Ce,La...) [РО4] (монацит). При разрушении горных пород он как весьма устойчивый химически минерал переходит в россыпи. Не случайно главные концентрации редкоземельных элементов связаны именно с этим минералом. Реже встречается другой, менее стойкий фосфат Y[РО4] (ксенотим). Фосфаты малых трехвалентных катионов (Al, Fe3+, Mn3+) в природе представлены водными солями.
Замечательно, что для аниона [SiO4]4– наиболее стойкими являются соединения с крупными четырехвалентными катионами (Zr4+, Th4+ нередко с изоморфной примесью урана U4+): циркон — Zr[SiO4] и торит — (Th,U)[SiO4].
Кристаллические структуры торита и его разновидностей разрушаются лишь вследствие радиоактивного распада. Циркон, не содержащий радиоактивных элементов, — весьма стойкий минерал, свидетельством чего является широкая распространенность его в виде окатанных зерен в россыпях и осадочных образованиях самых различных возрастов. В виде этого минерала выделяется главная масса циркония в земной коре. Лишь в магмах, бедных кремнеземом и богатых щелочами, он способен образовывать другие минералы.
Классификация кислородных солей. Систематику солей принято давать по кислотным радикалам или, что то же самое, по комплексным анионам. Порядок расположения можно принять тот, который намечается по величинам ВЭКов или ионных потенциалов (см. табл. 10). Рассмотрение кислородных солей вслед за окислами, в частности минералами группы кварца, следовало бы начать с более близких к ним в кристаллохимическом отношении силикатов и боратов и кончить иодатами, т. е. в порядке понижения ионных потенциалов анионов. Однако в целях лучшего усвоения материала мы примем обратный порядок изучения относящихся сюда минералов, исходя из принципа «от простого к сложному» (причем карбонаты рассмотрим до сульфатов).
Таким образом, среди минералов, представляющих кислородные соли, выделим следующие классы.
1. Нитраты.
2. Карбонаты.
3. Сульфаты.
4. Хроматы.
5. Молибдаты и вольфраматы.
6. Фосфаты, арсенаты и ванадаты.
7. Бораты.
8. Силикаты и алюмосиликты.
1 С меньшим количеством молекул Н2О, нежели в предыдущем случае.

